
工业上由废铜屑制硫酸铜晶体的流程如下:

(1)下列溶解铜屑的两种方案中,方案二的优点是 。(答两点即可)
方案一:向铜屑中加入足量的浓硫酸并加热。
方案二:向铜屑中加入少量的银粉再加足量的稀硫酸并通入足量空气。
(2)测定硫酸铜晶体( CuSO4·xH2O)中结晶水数目可通过以下实验步骤确定:
Ⅰ.称取0.4820 g样品置于小烧杯中,加入适量稀硫酸,加热溶解,边搅拌边滴加BaCl2到沉淀完全;
Ⅱ.过滤并洗涤沉淀;
Ⅲ.将盛有沉淀的滤纸包烘干并高温灼烧,再转入高温炉中,一定温度下反复灼烧到恒重,得到BaSO4质量为0.4660 g。
回答下列问题:
①计算CuSO4·xH2O中的x= (要求写出计算过程)。
②步骤Ⅲ中,如果空气不充足和温度过高,可能会有部分沉淀被滤纸中的碳还原为BaS,若其他操作均正确,则x的测定结果将 (填“偏低”、“偏高”或“不变”)。
(1)无需加热、能耗低,无污染性气体SO2 ,耗酸量少或硫酸利用率高(4分答出两点即可,每点2分)
(2)算出SO42-(或BaSO4或CuSO4·xH2O) 为0.002 mol (2分) x = 4.5 (2分)
(3)偏高 (2分)
【解析】
试题分析:(1)方案二的优点是无需加热、能耗低,无污染性气体SO2 ,耗酸量少或硫酸利用率高,形成原电池加快反应速率等;
(2)n(BaSO4)= n(CuSO4)=0.4660÷233=0.002mol,n(H2O)=( 0.4820-0.002×160)÷18=0.009mol ,n(CuSO4):n(H2O)=1:x x = 4.5
若有部分沉淀被滤纸中的碳还原为BaS,则沉淀的质量变少,计算出CuSO4的量变少,水的量偏高,结果偏高。
考点:考查用测定物质组成实验操作及结果分析有关问题。


 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案 高效智能课时作业系列答案
高效智能课时作业系列答案科目:高中化学 来源:2016届江苏省泰州市姜堰区高一上学期期中考试化学试卷(解析版) 题型:选择题
除去镁粉中的少量铝粉,可选用的溶液是
A.盐酸 B.硫酸
C.氯化钠溶液 D.氢氧化钾溶液
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高一上学期期中考试化学试卷(解析版) 题型:选择题
传统的引爆炸药由于其中含Pb,使用时将产生污染,同时其引爆后的剩余炸药还严重危害接触者的人身安全,美国UNC化学教授Thomas J.Meyer等研发了环境友好、 安全型的“绿色”引爆炸药,其中一种可表示为Na2R,爆炸后不会产生危害性残留物。已知10 mL Na2R溶液含Na+的微粒数为N个,该Na2R溶液的物质的量浓度为
A.N×10-2 mol/L B.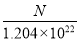 mol/L
mol/L
C.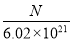 mol/L D.
mol/L D.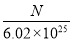 mol/L
mol/L
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高一上学期期中考试化学试卷(解析版) 题型:选择题
下列关于胶体的叙述不正确的是
A.胶体区别于其他分散系的本质特征是分散质的微粒直径在10-9 m~10-7m之间
B.光线透过胶体时,胶体中可发生丁达尔效应
C.用聚光手电筒照射NaCl溶液和Fe(OH)3胶体时,产生的现象相同
D.Fe(OH)3胶体能够吸附水中悬浮的固体颗粒并沉降,达到净水目的
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高一上学期期中考试化学试卷(解析版) 题型:选择题
下列溶液中Cl-浓度最小的是
A.200mL 2mol/L MgCl2溶液 B.300mL 2.5mol/L FeCl3溶液
C.300mL 2.5mol/L NaCl溶液 D.250mL 1mol/L AlCl3溶液
查看答案和解析>>
科目:高中化学 来源:2016届江苏省扬州市高一上学期期末调研测试化学试卷(解析版) 题型:填空题
完成下列填空
(1)向煤中加入适量的 ,可以大大减少燃烧产物中SO2的量。
(2)铝制品具有良好抗腐蚀性的原因是 。
(3)在少量的胆矾晶体中加入3 mL浓硫酸,片刻后变白色,证明浓硫酸具有 性。
(4)区别氯化铁溶液与氢氧化铁胶体的实验名称是 实验。
查看答案和解析>>
科目:高中化学 来源:2016届江苏省扬州市高一上学期期末调研测试化学试卷(解析版) 题型:选择题
氮化铝(化学式为AlN,其中Al为+3价)广泛应用于电子、陶瓷等工业领域。在一定条件下,AlN 可通过反应:Al2O3+N2+3C 2AlN+3CO合成。下列叙述正确的是
2AlN+3CO合成。下列叙述正确的是
A.Al2O3是氧化剂 B.N2被氧化
C.AlN的摩尔质量为41 g D.生成1 mol AlN转移3 mol电子
查看答案和解析>>
科目:高中化学 来源:2016届江苏省宿迁市高一上学期第二次月考化学试卷(解析版) 题型:实验题
某氯化铁样品含有少量FeCl2杂质。现要测定其中铁元素的质量分数,实验按以下步骤进行:
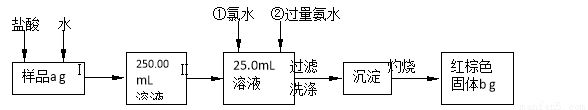
请根据上面流程,回答以下问题:
(1)操作I是配制溶液,所用到的玻璃仪器除烧杯、玻璃棒外,还必须有 、 .(填仪器名称)
(2)下列操作可能使所配溶液浓度偏小的是________________(填写序号)。
①未洗涤烧杯和玻璃棒
②定容时俯视容量瓶的刻度线
③配溶液前容量瓶中有少量蒸馏水
④摇匀后,发现液面低于刻度线后继续加水至凹液面与刻度线相切
(3)请写出加入氯水发生的离子方程式 ,
(4)检验沉淀是否已经洗涤干净的操作是 。
(5)若原样品质量a为50g,加热后红棕色固体质量b为3g,则样品中铁元素的质量分数是 。
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高一下学期学情分析考试化学试卷(解析版) 题型:选择题
元素性质呈周期性变化的决定因素是
A.元素原子半径大小呈周期性变化
B.元素相对原子质量依次递增
C.元素原子最外层电子排布呈周期性变化
D.元素的最高正化合价呈周期性变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com