
【题目】下列实验操作中数据合理的是
A.用10 mL 量筒量取5.2 mL盐酸
B.用广泛pH试纸测得某溶液的pH值为12.5
C.用托盘天平称取25.12gNaCl固体
D.用100 mL容量瓶配制50mL0.1 mol/L的盐酸
科目:高中化学 来源: 题型:
【题目】银锌电池在商业、宇航潜艇、核武器等领域有广泛应用。一种从正极片(含Ag、Ag2O、石墨及Cu等)中回收银的流程如下,下列叙述错误的是
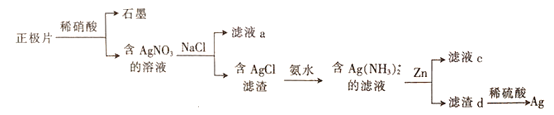
A. 滤液a中含有Na+、Cu2+、H+等阳离子
B. A用氨水溶解时发生的反应为AgCl+2NH3H2O=[Ag(NH3)2]++C1-+2H2O
C. 滤液c可浓缩结晶得到Zn(NO3)2
D. 向滤渣d中加稀硫酸可溶解其中过量的Zn
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业合成氨的反应为N2(g)+3H2(g)![]() 2NH3(g),已知下列化学键的键能:
2NH3(g),已知下列化学键的键能:
化学键 | 键能kJ/mol |
H-H | 436 |
N-H | 391 |
N | 946 |
下列说法正确的是
A. 该反应为吸热反应B. 该反应中反应物的总能量高于生成物的总能量
C. 反应热ΔH=92 kJ·mol-1D. 生成1 mol NH3放出92 kJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )。
A. 增大反应体系的压强,反应速率不一定增大
B. 增大反应物的浓度,能够增大活化分子的百分含量,所以反应速率增大
C. 活化分子的碰撞都是有效碰撞
D. 加入催化剂加快了反应速率,改变了反应吸收或放出的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E、F、G都是短周期的元素,它们的原子序数依次递增。A原子的电子层数与它的核外电子总数相同,而B原子的最外层电子数是次外层的2倍,C的氢化物可使湿润的红色石蕊试纸变蓝,B和D可以形成两种气态化合物,E原子核外电子总数比B的2倍少1,D与F同主族,G的原子半径是本周期元素中最小的。则:
(1)C元素的名称是__________ D元素的符号是____________
(2)B元素的最高价氧化物的电子式是_______________________
(3) G单质与E的最高价氧化物的水化物反应的离子方程式为____________.
(4)运送飞船的火箭燃料有一种液态化合物是由A、C元素组成的,已知该化合物的相对分子质量为32,其中氢元素的质量分数为12.5%,若该化合物与A2D2恰好完全反应,能产生两种无毒又不污染环境的物质,试写出该反应的化学方程式:______________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烯醇(CH2=CH-CH2OH)是一种无色有刺激性气味的液体,是重要的有机合成原料.请回答:
(1)丙烯醇的分子式为_______________;丙烯醇中含有的官能团的名称是________.
(2)0. 3mol丙烯醇与足量金属钠反应,能生成标准状况下的氢气_________________ L.
(3)写出丙烯醇与溴水反应的化学方程式____________________反应类型为____________
(4)丙烯醇与CH3CO18OH发生酯化反应的化方程式为:________________________________________
(5)酯化反应生成的产物在一定条件下可以发生加聚反应得到高分子化合物,其结构简式为_______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有OH﹣ , CO32﹣ , AlO2﹣ , SiO32﹣ , SO42﹣ , K + , Na + , Fe3 + , Mg2 + , Al3 + 等离子,当向溶液中逐滴加入一定物质的量的盐酸时,生成沉淀物质的量与加入盐酸体积的关系如图所示.下列判断正确的是

A.原溶液中一定含有Na2SO4
B.反应后形成的溶液溶质为NaCl
C.原溶液中含有CO32﹣与AlO2﹣的物质的量比为3:4
D.原溶液中一定含有的离子是OH﹣,CO32﹣,SiO32﹣,AlO2﹣,K +
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com