
��12�֣���Դ��ȱ������������ٵ��ش����⡣�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ������ҵ�Ϻϳɼ״��ķ�ӦΪ��CO(g)��2H2(g) CH3OH(g)����H
CH3OH(g)����H
��1����֪���÷�Ӧ��300�棬5MPa���������Է����У���H 0����S 0 ���������������
��2����300�棬5MPa�����£���0.20mol�� CO��0.58mol H2�Ļ���������2L�ܱ�����������Ӧ����Ӧ�����м״������ʵ���Ũ����ʱ��ı仯��ͼ��ʾ��

����0��2min�ڣ���H2��ʾ��ƽ����Ӧ����Ϊ mol��L-1��s-1 ��
����ʽ����300��ʱ�÷�Ӧ��ƽ�ⳣ��K = ��
��300��ʱ����0.50mol CO��1.00mol H2��1.00 mol CH3OH�����ݻ�Ϊ2L���ܱ������У���ʱ��Ӧ�� ��
A�����������ƶ� B�����淽���ƶ� C������ƽ��״̬ D�����ж�
�����д�ʩ�����Ӽ״����ʵ���
A��ѹ��������� B����CH3OH(g)����ϵ�з���
C������He��ʹ��ϵ��ѹǿ���� D���ٳ���0.20mol CO��0.58mol H2
��3���������������䣬ʹ��Ӧ��500���½��У���ͼ�������״������ʵ���Ũ����ʱ��ı仯��ʾ��ͼ��
����������1�����ݷ�Ӧ���ص��֪��SС��0����Ϊ��Ӧ��300�棬5MPa���������Է����У����Ը��ݡ�G����H��T����S��֪��Ӧ�Ƿ��ȷ�Ӧ��
��2���ٷ�Ӧ����ͨ���õ�λʱ����Ũ�ȵı仯������ʾ������ͼ���֪��Ӧ���е�2minʱ�״�
��Ũ�Ȳ��ٷ����仯��ƽ��ʱ�״������ʵ�����0.04mol��������������0.08mol��������0��2min
�ڣ���H2��ʾ��ƽ����Ӧ����Ϊ ��
��
��ƽ��ʱ������Ũ���� ��CO��ƽ��Ũ����
��CO��ƽ��Ũ����
 ,���Ը��¶��µ�ƽ�ⳣ��Ϊ
,���Ը��¶��µ�ƽ�ⳣ��Ϊ ��
��
��300��ʱ����0.50mol CO��1.00mol H2��1.00 mol
CH3OH�����ݻ�Ϊ2L���ܱ������У���ʱ���ǵ�Ũ�ȷֱ�Ϊ0.25mol/L��0.50mol/L����0.50mol/L����Ϊ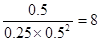 ��4�����Է�Ӧ���淴Ӧ�����ƶ���
��4�����Է�Ӧ���淴Ӧ�����ƶ���
��ѹ�������ѹǿ����ƽ��������Ӧ�����ƶ���ѡ��B�ǽ���������Ũ�ȣ�ƽ��Ҳ������Ӧ��
���ƶ�������He��ʹ��ϵ��ѹǿ�������ʵ�Ũ��û�б仯������ƽ�ⲻ�ƶ����ٳ���0.20mol
CO��0.58mol H2���൱��������ϵ��ѹǿ��ƽ��������Ӧ�����ƶ������Դ���ABD��
��3����Ϊ��Ӧ�Ƿ��ȷ�Ӧ�����������¶�ƽ�����淴Ӧ�����ƶ�������Ӧ���ʻ�ӿ죬����ͼ
��Ϊ

 ����С��ʿ���������ϵ�д�
����С��ʿ���������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��Դ��ȱ������������ٵ��ش����⣮�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ����
��Դ��ȱ������������ٵ��ش����⣮�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ����| 4 |
| 27 |
| 4 |
| 27 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��2012?������һģ����Դ��ȱ������������ٵ��ش����⣮�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ����
��2012?������һģ����Դ��ȱ������������ٵ��ش����⣮�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ����| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |
| c(CH3OH) |
| c(CO)c2(H2) |
| c(CH3OH) |
| c(CO)c2(H2) |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com