

| A、a和b用导线连接时,溶液中SO42-移向Cu极 |
| B、a和b用导线连接时,Cu极反应为:Cu-2e-=Cu2+ |
| C、要使Fe极不被腐蚀,a、b分别连接直流电源负、正极 |
| D、a和b分别接直流电源正、负极,Fe片上有气体产生 |


 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案科目:高中化学 来源: 题型:
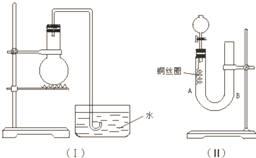 实验室用稀硝酸与铜反应来制备NO气体,如果采用(Ⅰ)装置(烧瓶内加入稀硝酸和铜片,必要时可加热),实验效果不十分理想,因为从观察到的现象不能有力证明反应产物是NO;有人设计了(Ⅱ)装置(橡皮塞下端连有铜丝圈),用来做该实验可以达到满意的效果.根据要求回答下列问题:
实验室用稀硝酸与铜反应来制备NO气体,如果采用(Ⅰ)装置(烧瓶内加入稀硝酸和铜片,必要时可加热),实验效果不十分理想,因为从观察到的现象不能有力证明反应产物是NO;有人设计了(Ⅱ)装置(橡皮塞下端连有铜丝圈),用来做该实验可以达到满意的效果.根据要求回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2CO3溶液中:c(OH-)=c(H+)+c(HCO3-)+c(H2CO3) |
| B、NH4Cl溶液中:c(NH4+)>c(Cl-)>c(H+)>c(OH-) |
| C、c(CO32-)+c(HCO3-)+c(H2CO3)=c(NH4+)+c(NH3?H2O) |
| D、2c(CO32-)+c(HCO3-)-c(Na+)=c(Cl-)-c(NH4+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等物质的量浓度等体积的氨水和盐酸混合后的溶液:c(Cl-)=c(NH4+)>c(H+)=c(OH-) |
| B、浓度为0.1mol?L-1的碳酸钠溶液:c(Na+)═2c(CO32-)+c(HCO3-)+c(H2CO3) |
| C、pH=12的氨水与pH=2的盐酸等体积混合:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| D、浓度为0.1mol?L-1的碳酸钠溶液:c(Na+)+c(H+)=c(OH-)+2c(CO32-)+c(HCO3-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(CN-)>c(Na+)>c(H+)>c(OH-) |
| B、c(Na+)>c(CN-)>c(OH-)>c(H+) |
| C、c(Na+)+c(H+)=c(CN-)+c(OH-) |
| D、2c(OH-)+c(CN-)=2c(H+)+c(HCN) |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、Al3+、Na+、Cl-、N
| ||||||
B、K+、N
| ||||||
C、Na+、K+、Al
| ||||||
D、Na+、K+、N
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| 原子或分子结构、单质或化合物相关信息 | |
| X | 含X元素的物质焰色反应为黄色 |
| Y | 单质为双原子分子.若低温蒸发液态空气,因其沸点较低可先获得Y的单质 |
| Z | Z元素原子易失去2个电子形成8电子结构的离子 |
| M | M元素原子的最外层电子数是K层电子数的3倍,M与X处于同一周期 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com