
| A. | 若混合气体的密度不再改变时,该反应不一定达到平衡状态 | |
| B. | 2min后,加压会使正反应速率增大,逆反应速率减小,平衡正向移动 | |
| C. | 反应过程中A和B的转化率之比为3:1 | |
| D. | 该条件下此反应的化学平衡常数的数值约为0.91 |
分析 A、反应前后气体质量和气体体积发生变化,若混合气体的密度不再改变时,该反应一定达到平衡状态;
B、2min后,加压会使正、逆反应速率都加快,平衡正向移动;
C、将3molA和1molB两种气体混合于固定容积为2L的密闭容器中,反应比和起始量之比相同,所以反应过程中A和B的转化率相同;
D、由图象中的数据,平衡后D生成物质的量为0.8mol,结合化学三段式列式
3A(g)+B(g)?C(g)+2D(s)
起始量(mol) 3 1 0 0
变化量(mol) 1.2 0.4 0.4 0.8
平衡量(mol) 1.8 0.6 0.4 0.8
平衡浓度为c(A)=0.9mol/L,c(B)=0.3mol/L,c(C)=0.2mol/L,D为固体不写入平衡常数计算式.
解答 解:A、反应生成固体D,气体质量和气体体积发生变化,若混合气体的密度不再改变时,该反应一定达到平衡状态,故A错误;
B、2min后,加压会使正、逆反应速率都加快,平衡正向移动,故B错误;
C、将3molA和1molB两种气体混合于固定容积为2L的密闭容器中,反应比和起始量之比相同,所以反应过程中A和B的转化率之比为1:1,故C错误;
D、由图象中的数据,平衡后D生成物质的量为0.8mol,结合化学三段式列式
3A(g)+B(g)?C(g)+2D(s)
起始量(mol) 3 1 0 0
变化量(mol) 1.2 0.4 0.4 0.8
平衡量(mol) 1.8 0.6 0.4 0.8
平衡浓度为c(A)=0.9mol/L,c(B)=0.3mol/L,c(C)=0.2mol/L,D为固体可计算得此反应的化学平衡常数=$\frac{0.2}{0.{9}^{3}×0.3}$=0.91,平衡常数约为0.91,故D正确.
故选:D.
点评 本题考查了化学平衡标志分析,平衡常数概念的计算应用,主要是一些反应速率、化学平衡的因素分析判断,掌握基础是关键,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 使用聚二氧化碳塑料会产生白色污染 | |
| B. | 聚二氧化碳塑料是通过聚合反应制得的 | |
| C. | 聚二氧化碳塑料与干冰互为同分异构体 | |
| D. | 聚二氧化碳塑干冰都属于纯净物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 洗涤沉淀的方法是直接向过滤器中加入适量蒸馏水,然后让水自然流下 | |
| B. | 用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出 | |
| C. | 用100ml量筒量取9.5 mL的液体 | |
| D. | 焰色反应中,观察焰色后应趁热将铂丝插入到稀硫酸中,然后再次灼烧 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
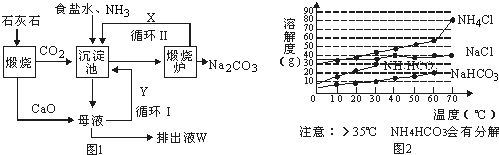
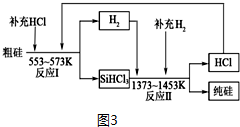
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
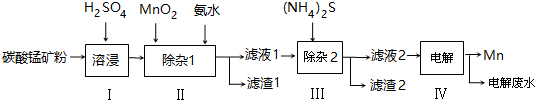
| 物质 | Mn(OH)2 | Co(OH)2 | Ni(OH)2 | MnS | CoS | NiS |
| Ksp | 2.1×10-13 | 3.0×10-16 | 5.0×10-16 | 1.0×10-11 | 5.0×10-22 | 1.0×10-22 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
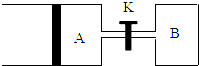 按要求填空:
按要求填空:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com