
ÖĘČ”ĻąĶ¬ĪļÖŹµÄĮæµÄĻõĖįĶ£¬ĻūŗÄĻõĖįĪļÖŹµÄĮæ×ī¶ąµÄ·“Ó¦ŹĒ£Ø £©
A .ĶŗĶÅØĻõĖį B.ĶŗĶĻ”ĻõĖį C.Ńõ»ÆĶŗĶÅØĻõĖį D.Ńõ»ÆĶŗĶĻ”ĻõĖį
.ĶŗĶÅØĻõĖį B.ĶŗĶĻ”ĻõĖį C.Ńõ»ÆĶŗĶÅØĻõĖį D.Ńõ»ÆĶŗĶĻ”ĻõĖį

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
¶ĢÖÜĘŚŌŖĖŲX”¢Y”¢Z”¢W”¢RµÄŌ×ÓŠņŹżŅĄ“ĪŌö“ó£¬Xµ„ÖŹŌŚ°µ“¦ÓėH2¾ēĮŅ»ÆŗĻ²¢·¢Éś±¬ÕØ£¬YĪ»ÓŚµŚIA×壬ZĖł“¦µÄÖÜĘŚŠņŹżÓė×åŠņŹżĻąµČ£¬WŌŖĖŲ×īøßÕż¼ŪÓė×ī µĶøŗ¼ŪÖ®ŗĶĪŖ0£¬RÓėXĶ¬×壬Ōņ
µĶøŗ¼ŪÖ®ŗĶĪŖ0£¬RÓėXĶ¬×壬Ōņ
A£®Ō×Ó°ė¾¶£ŗZ£¾Y£¾X
B£®XÓėRµÄŗĖµēŗÉŹżĻą²ī18
C£®ĘųĢ¬Ēā»ÆĪļĪČ¶ØŠŌ£ŗW£¾R
D£®YÓėZĮ½Õß×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļÄÜĻą»„·“Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
֊ѧ»Æѧ֊ŗܶą”°¹ęĀÉ”±¶¼ÓŠĘ䏏ÓĆ·¶Ī§£¬ĻĀĮŠøł¾ŻÓŠ¹Ų”°¹ęĀÉ”±ĶĘ³öµÄ½įĀŪŗĻĄķµÄŹĒ(””””)
A£®øł¾ŻĶ¬ÖÜĘŚŌŖĖŲµÄµŚŅ»µēĄėÄܱä»ÆĒ÷ŹĘ£¬ĶĘ³öAlµÄµŚŅ»µēĄė±ČMg“ó
B£®øł¾ŻÖ÷×åŌŖĖŲ×īøßÕż»ÆŗĻ¼ŪÓė×åŠņŹżµÄ¹ŲĻµ£¬ĶĘ³öĀ±×åŌŖĖŲ×īøßÕż¼Ū¶¼ŹĒ£«7
C£®øł¾ŻČÜŅŗµÄpHÓėČÜŅŗĖį¼īŠŌµÄ¹ŲĻµ£¬ĶĘ³öpH£½6.8µÄČÜŅŗŅ»¶ØĻŌĖįŠŌ
D£®øł¾Ż½ĻĒæĖįæÉŅŌÖĘČ”½ĻČõĖįµÄ¹ęĀÉ£¬ĶĘ³öCO2ĶØČėNaClOČÜŅŗÖŠÄÜÉś³ÉHClO
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
25”ꏱ£¬¼×ČÜŅŗµÄpHŹĒ4£¬ŅŅČÜŅŗµÄpHŹĒ5£¬¼×ČÜŅŗÓėŅŅČÜŅŗÖŠµÄc£ØOH-£©Ö®±ČĪŖ
A£®10£ŗ1 B£®1£ŗ10 C£®2£ŗ1 D£®1£ŗ2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
»ÆѧĄķĀŪŌŚŌŖĖŲµ„ÖŹ¼°Ęä»ÆŗĻĪļ·“Ó¦ÖŠÓ¦ÓĆ¹ć·ŗ”£
£Ø1£©ŌŚŅ»¶ØĢõ¼žĻĀ£¬æÉÄę·“Ó¦mA nB£«pC ØSH£¬“ļµ½Ę½ŗāדĢ¬”£
nB£«pC ØSH£¬“ļµ½Ę½ŗāדĢ¬”£
¢ŁČōA”¢B”¢C¶¼ŹĒĘųĢ壬Ōö“óŃ¹Ēæ£¬Ę½ŗāĻņÄę·“Ó¦·½ĻņŅĘ¶Æ£¬Ōņm £ØĢī”°“óÓŚ”±”¢”°Š”ÓŚ”±»ņ”°µČÓŚ”±£©n£«p”£
¢ŚĘäĖūĢõ¼ž²»±ä£¬¼ÓČČŗóAµÄÖŹĮæŌö¼Ó£¬Ōņ·“Ó¦ØSH________0£ØĢī”°“óÓŚ”±”¢”°Š”ÓŚ”±»ņ”°µČÓŚ”±£©”£
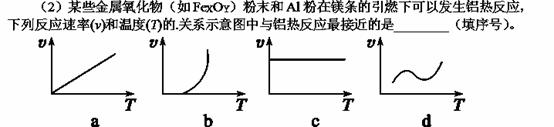 £Ø3£©Ņ»¶ØĪĀ¶ČĻĀ£¬·¢Éś·“Ó¦£ŗFeO(s)£«CO(g)
£Ø3£©Ņ»¶ØĪĀ¶ČĻĀ£¬·¢Éś·“Ó¦£ŗFeO(s)£«CO(g) Fe(s)£«CO2(g) ¦¤H”£ŅŃÖŖøĆ·“Ó¦ŌŚ²»Ķ¬ĪĀ¶ČĻĀµÄĘ½ŗā³£ŹżČēĻĀ±ķ£ŗ
Fe(s)£«CO2(g) ¦¤H”£ŅŃÖŖøĆ·“Ó¦ŌŚ²»Ķ¬ĪĀ¶ČĻĀµÄĘ½ŗā³£ŹżČēĻĀ±ķ£ŗ
| ĪĀ¶Č/”ę | 1000 | 1100 |
| Ę½ŗā³£Źż | 0.68 | 0.50 |
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
¢ŁøĆ·“Ó¦µÄ¦¤H___ 0£ØĢī”°>”±”¢”°<”±»ņ”°£½”±£©”£
¢ŚT”ꏱ£¬½«FeO(s)ŗĶCO(g)ø÷3.0 mol¼ÓČė10 LµÄĆܱÕČŻĘ÷ÖŠ£¬·“Ó¦“ļµ½Ę½ŗāŗ󣬲āµĆCO×Ŗ»ÆĀŹĪŖW1£¬c(CO2) £½0.15mol”¤L£1£¬ŌņĪĀ¶ČT £ØĢī”°øßÓŚ”±”¢”°µĶÓŚ”±”¢”°µČÓŚ”±£©1000£¬ Čō“ĖŹ±±£³ÖĘäĖüĢõ¼ž²»±äŌŁ³äČė2.0 mol CO(g)£¬ŌŁ“ļĘ½ŗāŹ±²āµĆCO×Ŗ»ÆĀŹĪŖW2£¬ŌņW1 £ØĢī”°>”±”¢”°<”±»ņ”°£½”±£©W2”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A£®Ō×Ó×īĶā²ćµē×ÓŹżµČÓŚ»ņ“óÓŚ3µÄŌŖĖŲŅ»¶ØŹĒ·Ē½šŹōŌŖĖŲ
B£®Ō×Ó×īĶā²ćÖ»ÓŠ1øöµē×ÓµÄŌŖĖŲŅ»¶ØŹĒ½šŹōŌŖĖŲ
C£®×īĶā²ćµē×ÓŹż±Č“ĪĶā²ćµē×ÓŹż¶ąµÄŌŖĖŲŅ»¶ØĪ»ÓŚµŚ¶žÖÜĘŚ
D£®Ä³ŌŖĖŲµÄĄė×Ó×īĶā²ćµē×ÓŹżÓė“ĪĶā²ćµē×ÓŹżĻąĶ¬£¬øĆŌŖĖŲŅ»¶ØĪ»ÓŚµŚČżÖÜĘŚ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŌĖÓĆŌŖĖŲÖÜĘŚĀÉ·ÖĪöĻĀĆęµÄĶʶĻÕżČ·µÄŹĒ£Ø £©
A£®īė(Be)ŹĒŅ»ÖÖĒį½šŹō£¬ĖüµÄŃõ»ÆĪļµÄĖ®»ÆĪļæÉÄܾßÓŠĮ½ŠŌ
B£®ķĮµ„ÖŹŹĒŅ»ÖÖÓŠÉ«¹ĢĢ壬ķĮ»ÆĒāŗܲ»ĪČ¶Ø£¬ķĮ»ÆŅųŹĒÄŃČÜÓŚĖ®µÄ°×É«³Įµķ
C£®ĮņĖįļČÄŃČÜÓŚĖ®£¬µ«Ņ×ČÜÓŚŃĪĖį
D£®Īų»ÆĒāŹĒĪŽÉ«”¢ÓŠ¶¾”¢±ČĮņ»ÆĒāĪČ¶ØµÄĘųĢå
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠ¶ŌNa2O2µÄŠšŹöÖŠÕżČ·µÄŹĒ””””
A£®Na2O2ÄÜÓėĖį·“Ӧɜ³ÉŃĪŗĶĖ®£¬ĖłŅŌNa2O2ŹĒ¼īŠŌŃõ»ÆĪļ
B£®Na2O2ÄÜÓėĖ®·“Ó¦£¬ĖłŅŌNa2O2æÉŅŌ×÷ĘųĢåµÄøÉŌļ¼Į
C£®Na2O2ÓėĖ®·“Ó¦Ź±£¬Na2O2ŹĒŃõ»Æ¼Į£¬Ė®ŹĒ»¹Ō¼Į
D£®Na2O2Óė¶žŃõ»ÆĢ¼·“Ó¦Ź±£¬Na2O2¼ČŹĒŃõ»Æ¼ĮÓÖŹĒ»¹Ō¼Į
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Ķ¬Ö÷×åŌŖĖŲĖłŠĪ³ÉµÄĶ¬Ņ»ĄąŠĶµÄ»ÆŗĻĪļ½į¹¹ŗĶŠŌÖŹĶłĶłĻąĖĘ£¬ŅŃÖŖ»ÆŗĻĪļPH4IŹĒŅ»ÖÖĪŽÉ«¾§Ģ壬ŹŌÅŠ¶ĻĻĀĮŠ¶ŌĘäĆčŹöÕżČ·µÄŹĒ£Ø””””£©
A£®PH4IŹĒ¹²¼Ū»ÆŗĻĪļ£¬ŹōÓŚ·Ö×Ó¾§Ģå
B£®PH4I¶ŌČČ²»ĪČ¶Ø£¬ŹÜČČ·Ö½āÉś³ÉĪŽÉ«ĘųĢå
C£®PH4I²»ÄÜÓėNaOH·“Ó¦
D£®PH4IæÉÓÉPH3ÓėHI»ÆŗĻ¶ų³É
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com