
| A. | 氯气是一种具有刺激性气味的无色气体 | |
| B. | 新制氯水可使蓝色石蕊试纸先变红后褪色 | |
| C. | 光照氯水有气泡逸出,该气体是Cl2 | |
| D. | 铁分别与氯气、盐酸反应时得到相同的氯化物 |
分析 A.依据氯气是一种黄绿色气体解答;
B.新制氯水中含有盐酸和次氯酸,依据二者性质解答;
C.次氯酸见光分解生成氧气和氯化氢;
D.铁与氯气反应生成三氯化铁,与盐酸反应生成氯化亚铁.
解答 解:A.氯气是一种黄绿色有刺激性气味的气体,故A错误;
B.新制氯水中含有盐酸和次氯酸,盐酸具有酸性能够使蓝色石蕊试纸变红,次氯酸具有漂白性,能够使变红的试纸褪色,故B正确;
C.次氯酸见光分解生成氧气和氯化氢,氯化氢溶于水,所以逸出的气体为氧气,故C错误;
D.铁与氯气反应生成三氯化铁,与盐酸反应生成氯化亚铁,二者产物不同,故D错误;
故选:B.
点评 本题考查了元素化合物知识,侧重考查氯气、氯水的性质,明确氯水的成分及各种微粒的性质是解题关键,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
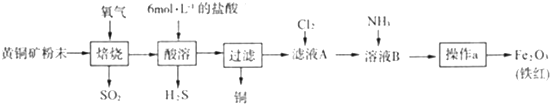
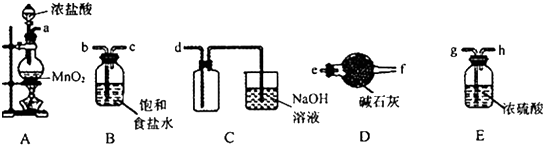
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
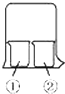 使用如图所示装置进行化学小实验,请填写下列空白:
使用如图所示装置进行化学小实验,请填写下列空白:查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:解答题
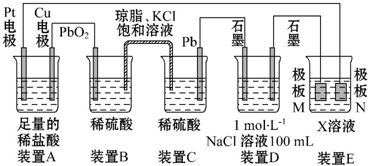
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com