


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:

(1)门捷列夫的突出贡献是( )
A.提出了原子学说 B.提出了分子学说
C.发现元素周期律 D.发现能量守恒定律
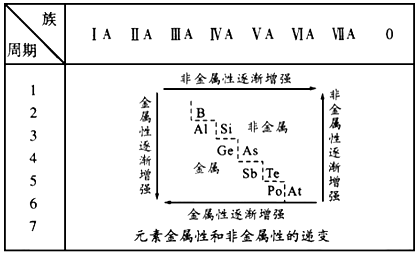
(2)该表变化表明( )
A.事物的性质总是在不断地发生变化
B.元素周期表中最右上角的氦元素是非金属性最强的元素
C.ⅠA族元素的金属性比同周期ⅡA族元素的金属性强
D.物质发生量变到一定程度必然引起质变
(3)按照表中元素的位置,认真观察从ⅢA族的硼到ⅦA族的砹连接的一条折线,我们能从分界线附近找到( )
A.耐高温材料 B.新型农药材料
C.半导体材料 D.新型催化剂材料
(4)据报道,美国科学家制得一种新原子![]() ,它属于一种新元素116号元素(元素符号暂用X代替),关于它的推测正确的是( )
,它属于一种新元素116号元素(元素符号暂用X代替),关于它的推测正确的是( )
A.这种原子的中子数为167 B.它位于元素周期表中第6周期
C.这种元素一定是金属元素 D.这种元素的原子易与氢化合
查看答案和解析>>
科目:高中化学 来源:同步题 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com