
【题目】I、已知A、B、C、D、E、F、G都是中学化学常见的物质,下图中A为淡黄色固体,B、C为溶液,D、G为无色气体,E、F为白色沉淀。
①写出B→C的离子方程式
②写出D和G反应的化学方程式
③写出过量的D通入Ba(OH)2溶液中的离子方程式
II.由X、Y两种元素组成的离子化合物A。在空气中充分灼烧得到含X元素的16g红棕色固体B,并产生能使品红褪色的气体C,将该气体全部通入足量的双氧水中得D溶液,再向D溶液中加入足量的BaCl2溶液,过滤、洗涤、干燥得93.2g固体。
(1)在此过程中,消耗5 mol/L的双氧水的体积至少为 。
(2)将A溶于D的稀溶液中生成E,并产生一种单质和一种气体,则该反应的化学方程式 。
(3)将化合物E隔绝空气充分灼烧,使其分解,生成等物质的量的B、C和另一种化合物,则另一种化合物的化学式是_____________;
【答案】
I、(1)H2SO3+Cl2=4H++SO42-+2Cl-;
(2)2SO2+O2 ![]() 2 SO2
2 SO2
(3)OH-+ SO2 = HSO3-
II、(1)80ml(2)FeS2+H2SO4=H2S↑+S↓+FeSO4(3)SO3
【解析】
试题分析:I、B与硫化氢反应得到淡黄色固体A,考虑A为硫,B与氯气反应得到C,C与硝酸钡反应得到白色沉淀F,且A与无色气体反应得到D,D与水反应得到B,可推知B为H2SO3,A为S,G为O2,D为SO2,C为H2SO4,E为BaSO3,F为BaSO4,
①B→C的离子方程式为:H2SO3+Cl2=4H++SO42-+2Cl-,故答案为:H2SO3+Cl2=4H++SO42-+2Cl-;
②D和G反应的化学方程式为:2SO2+O2![]() 2 SO3,故答案为:2SO2+O2
2 SO3,故答案为:2SO2+O2![]() 2 SO3;
2 SO3;
③过量的D通入Ba(OH)2溶液中的离子方程式为:OH-+SO2=HSO3-,故答案为:OH-+SO2=HSO3-;
II、离子化合物A由X、Y两种元素组成.在空气中充分灼烧得到含X元素的16g红棕色固体B,则B为Fe2O3,X为Fe,产生能使品红褪色的气体C,将该气体全部通入足量的双氧水中得D溶液,再向D溶液中加入足量的BaCl2溶液,得到93.2g固体,该固体为BaSO4,故C为SO2,D为H2SO4,则Y为S,氧化铁的物质的量=![]() =0.1mol,硫酸钡的物质的量=
=0.1mol,硫酸钡的物质的量=![]() =0.4mol,根据原子守恒化合物A中Fe、S原子数目之比=0.1mol×2:0.4mol=1:2,故A为FeS2。
=0.4mol,根据原子守恒化合物A中Fe、S原子数目之比=0.1mol×2:0.4mol=1:2,故A为FeS2。
(1)根据上述分析,氧化铁的物质的量为0.1mol,则同时生成二氧化硫0.4mol,气体SO2通入H2O2中被氧化生成硫酸,反应离子方程式为:SO2+H2O2=2H++SO42-,需要双氧水的物质的量为0.4mol,双氧水的体积=![]() =
=![]() =0.08L=80mL,故答案为:80mL;
=0.08L=80mL,故答案为:80mL;
(2)将FeS2溶于H2SO4的稀溶液中生成E,并产生一种单质和一种气体,应生成硫酸亚铁、硫化氢、硫,该反应的化学方程式为:FeS2+H2SO4=H2S↑+S↓+FeSO4,故答案为:FeS2+H2SO4=H2S↑+S↓+FeSO4;
(3)将化合物FeSO4隔绝空气充分灼烧,使其分解,生成等物质的量的Fe2O3、SO2和另一种化合物,根据原子守恒,则另一种化合物的化学式是SO3;故答案为:SO3。


科目:高中化学 来源: 题型:
【题目】为确定某溶液由以下离子Na+、Mg2+、Ba2+、SO42﹣、I﹣、CO32﹣中的哪几种微粒组成.进行以下实验,分别取样:①用pH计测试,溶液显弱酸性;②加氯水和淀粉无明显现象.为确定该溶液的组成,还需检验的离子是( )
A.Na+ B.SO42﹣ C.Ba2+ D.Mg2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.4gNaOH和1.06gNa2CO3混合并配成溶液,向溶液中滴加0.1mol·L--1稀盐酸。下列图像能正确表示加入盐酸的体积和生成CO2的物质的量的关系是( )
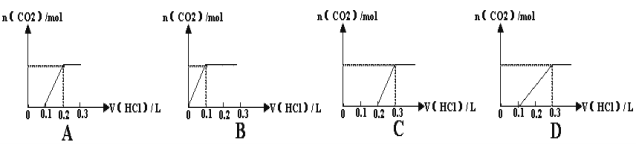
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雷雨天闪电时空气中有臭氧生成,下列说法正确的是( )
A.O2和O3互为同位素
B.O2和O3的相互转化是物理变化
C.等物质的量的O2和O3含有相同的质子数
D.在相同的温度与压强下,等体积的O2和O3含有相同的分子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业制硫酸中的一步重要反应是SO2在400~500 ℃下的催化氧化:2SO2+O2![]() 2SO3,这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法中错误的是( )
2SO3,这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法中错误的是( )
A. 使用催化剂是为了加快反应速率,提高生产效率
B. 在上述条件下,SO2不可能100%地转化为SO3
C. 为了提高SO2的转化率,应适当提高O2的浓度
D. 达到平衡时,SO2的浓度与SO3的浓度相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种重要的有机化工原料有机物X,下面是以它为初始原料设计出如下转化关系图(部分产物、合成路线、反应条件略去)。Y是一种功能高分子材料。

已知:(1)X为芳香烃,其相对分子质量为92
(2)烷基苯在高锰酸钾的作用下,侧链被氧化成羧基:![]()
(3)![]() (苯胺,易被氧化)
(苯胺,易被氧化)
请根据本题所给信息与所学知识回答下列问题:
(1)X的分子式为______________。
(2) 中官能团的名称为____________________;
中官能团的名称为____________________;
(3)反应③的反应类型是___________;已知A为一氯代物,则E的结构简式是____________;
(4)反应④的化学方程式为_______________________;
(5)阿司匹林有多种同分异构体,满足下列条件的同分异构体有________种:①含有苯环;②既不能发生水解反应,也不能发生银镜反应;③1mol该有机物能与2molNaHCO3完全反应。
(6)请写出以A为原料制备![]() 的合成路线流程图 (无机试剂任用)。合成路线流程图示例如下:
的合成路线流程图 (无机试剂任用)。合成路线流程图示例如下:
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知胆矾溶于水时溶液温度降低,室温下将1mol无水硫酸铜制成溶液时放出热量为Q1kJ,又知胆矾分解的热化学方程式为CuSO45H2O(s) = CuSO4(s)+5H2O(l) △H=+Q2 kJ·mol1则Q1、Q2的关系为
A.Q1<Q2 B.Q1>Q2 C.Q1=Q2 D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,美国正在研究用锌电池取代目前广泛使用的蓄电池,它具有容量大、污染小的特点,其电池反应为:2Zn+O2=2ZnO ,其原料为锌、空气和电解质溶液,则下列叙述正确的是
A.锌为正极,空气在负极反应
B.负极还原反应,正极氧化反应
C.负极的电极反应为:Zn-2e-+2OH-=ZnO+H2O
D.电池工作时溶液的pH降低
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com