
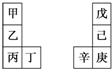
 甲~辛等元素在周期表中的相对位置如表.甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素,下列判断正确的是( )
甲~辛等元素在周期表中的相对位置如表.甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素,下列判断正确的是( )| A. | 丙与庚的原子序数相差3 | |
| B. | 气态氢化物的热稳定性:戊>己>庚 | |
| C. | 乙所在周期元素中,其简单离子的半径最大 | |
| D. | 乙的单质在空气中燃烧生成的化合物只含离子键 |
分析 戊的一种单质(金刚石)是自然界硬度最大的物质,则戊为C,甲与戊的原子序数相差3,则甲的原子序数为6-3=3,即甲为Li,由元素在周期表中的相对位置图可知,乙为Na,丙为K,丁为Ca;丁与辛属同周期元素,由第ⅣA族元素可知,己为Si,庚为Ge,辛为Ga,然后结合元素周期律及元素化合物知识来解答.
解答 解:戊的一种单质(金刚石)是自然界硬度最大的物质,则戊为C,甲与戊的原子序数相差3,则甲的原子序数为6-3=3,即甲为Li,由元素在周期表中的相对位置图可知,乙为Na,丙为K,丁为Ca;丁与辛属同周期元素,由第ⅣA族元素可知,己为Si,庚为Ge,辛为Ga,
A.丙(原子序数为19)与庚(原子序数为32)的原子序数相差13,故A错误;
B.戊、己、庚位于相同主族,同一主族元素从上到下非金属性逐渐降低,则对应的氢化物的稳定性逐渐减小,故B正确;
C.乙为Na,为第三周期,简单离子的半径最大的为S2-,故C错误;
D.乙的单质在空气中燃烧生成Na2O2,为含离子键和非极性共价键的化合物,故D错误;
故选B.
点评 本题侧重位置、结构、性质的关系及元素周期律的考查,为高考常见题型和高频考点,把握金刚石的硬度及甲与戊的原子序数关系推断各元素为解答的关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
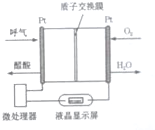
| A. | 电流由O2所在的铂电极流出 | |
| B. | O2所在的铂电极处发生还原反应 | |
| C. | 该电池的负极反应式为CH3CH2OH+3H2O-12e-=2CO2↑+12H+ | |
| D. | 微处理器通过检测电流大小而计算出被测气体中酒精的含量. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、OH-、Cl-、SO42- | B. | H+、NH4+、Al3+、NO3- | ||
| C. | Na+、S2-、Cl-、SO42- | D. | Na+、C6H5O-、CH3COO-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生铁比纯铁容易生锈 | |
| B. | 钢铁的腐蚀生成疏松氧化膜,不能保护内层金属 | |
| C. | 钢铁发生吸氧腐蚀时,正极反应式为:O2+2H2O+4e→4OH- | |
| D. | 为保护地下钢管不受腐蚀,可使其与直流电源正极相连 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硅是制造玻璃、光导纤维的原料 | |
| B. | 纤维素、油脂是天然有机高分子化合物 | |
| C. | 白菜上洒少许福尔马林,既保鲜又消毒 | |
| D. | NOx、CO2、PM2.5颗粒都会导致酸雨 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 镧镍合金能大量吸收H2形成金属氢化物,可作储氢材料 | |
| B. | 石英玻璃、陶瓷都属于硅酸盐产品 | |
| C. | 做衣服的棉、麻、蚕丝的成分都是纤维素 | |
| D. | 牛油和花生油在碱性条件下水解产物相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | A+离子半径小于B+离子半径 | |
| B. | B是其所在主族元素中金属性最强的 | |
| C. | D的氧化物为酸性氧化物,溶于水可制得D的含氧酸 | |
| D. | D与E组成的化合物中,各原子最外层均达到8电子结构 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com