
����Ŀ����ʵ������Ҫ����0.1 mol��L��1NaOH��Һ500mL��
��1�����ݼ�����������ƽ��ȡ������Ϊ__________g������ͼ��ʾ�����У�����������Һ�϶�����Ҫ����_________(�����)����ͼ�����������⣬����������Һ����Ҫ�IJ���������________��
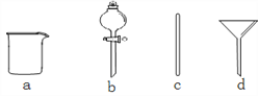
��2������ʱ������ȷ�IJ���˳����(����ĸ��ʾ��ÿ������ֻ��һ��)__________��
A��������ˮϴ���ձ�2�Ρ�3�Σ�ϴ��Һ��ע������ƿ����
B����ʢ��NaOH������ձ��м�������ˮ�ܽ�
C�����ձ�������ȴ����Һ�ز�����ע������ƿ��
D��������ƿ�ǽ����������µߵ���ҡ��
E�����ý�ͷ�ιܼ�ˮ��ʹ��Һ��Һ��ǡ����̶�����
F������������ƿ��С�ļ�ˮ��ֱ��Һ��ӽ��̶�1 cm��2 cm��
��3����������������NaOH��ҺŨ��ƫ�ߵ���_____��
A���ܽ����Һû����ȴ�����¾�ת��
B��ת��ʱû��ϴ���ձ���������
C��������ƿ��ˮ����ʱ�۾�����Һ��
D��ҡ�Ⱥ���Һ����ڿ̶��ߣ��ּ�����ˮ���̶���
II����Ũ����ȡ������Ϊ100 mL��A��B����NaOH��Һ�У��ֱ�ͨ��һ������CO2������������Һ�еμ�0.1 mol/L���ᣬ����CO2�����(��״��)����������������ϵ��ͼ��ʾ��
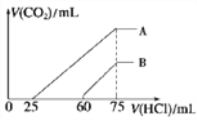
��4����A���߱�����ԭ��Һͨ��CO2���������������ᷴӦ����CO2����������________mL(��״��)��
��B���߱�����ԭ��Һͨ��CO2��������Һ�����ʵĻ�ѧʽΪ______________��
���𰸡�2.0bd500mL����ƿ����ͷ�ι�BCAFEDAC112NaOH��Na2CO3
��������
��1������0.1 mol��L��1NaOH��Һ500mL��Ҫ�������Ƶ�������0.1mol/L��0.5L��40g/mol��2.0g������һ�����ʵ���Ũ����Һ�õ������У�������ƽ��ҩ�ס��ձ���Ͳ����������������ƿ����ͷ�ιܣ�����Ҫ��������©���ͷ�Һ©���������õ��IJ���������500mL����ƿ����ͷ�ιܣ�
��2������һ�����ʵ���Ũ����Һһ�㲽��Ϊ�����㡢�������ܽ⡢��ȴ����Һ��ϴ�ӡ����ݡ�ҡ�ȡ�װƿ�ȣ�������ȷ��˳��Ϊ��BCAFED��
��3��A���ܽ����Һû����ȴ�����¾�ת�ƣ���ȴ����Һ���ƫС����ҺŨ��ƫ�ߣ�A��ȷ��
B��ת��ʱû��ϴ���ձ��������������²���������ģ����ʵ����ʵ���ƫС����ҺŨ��ƫ�ͣ�B����
C��������ƿ��ˮ����ʱ�۾�����Һ�棬������Һ���ƫ�ͣ���ҺŨ��ƫ�ߣ�C��ȷ��
D��ҡ�Ⱥ���Һ����ڿ̶��ߣ��ּ�����ˮ���̶��ߣ�������Һ���ƫ����ҺŨ��ƫ�ͣ�D����
��ѡAC��
��4����CO2+2NaOH=Na2CO3+H2O��CO2+NaOH=NaHCO3��֪��NaOH��Һ��ͨ��һ������CO2����Һ�����ʵ���ɿ�����NaOH��Na2CO3��Na2CO3��Na2CO3��NaHCO3��NaHCO3����
��A���߱�����������CO2����ʱ��������ӦHCO3-+H+=H2O+CO2�����μ�����25mLʱû���������ɣ����ܷ���OH-+H+=H2O��CO32-+H+=HCO3-������ԭ��Һ��ֻ��̼���ƣ�����̼��������Ҫ����������̼���������ɶ�����̼��Ҫ����������ȣ�ʵ������Ҫ��������25mLԶԶС��̼���������ɶ�����̼��Ҫ����������75-25��mL=50mL��˵��ԭ��Һ�е�������Na2CO3��NaHCO3����HCO3-+H+=H2O+CO2����֪�������ᷴӦ����CO2����������0.05L��0.1mol/L��22.4L/mol��0.112L��112mL��
��B���߱�����ԭ��Һͨ��CO2������CO2����ʱ��������ӦHCO3-+H+=H2O+CO2�����μ�����60mLʱû���������ɣ����ܷ���OH-+H+=H2O��CO32-+H+=HCO3-������ԭ��Һ��ֻ��̼���ƣ�����̼��������Ҫ����������̼���������ɶ�����̼��Ҫ����������ȣ�ʵ������Ҫ��������60mLԶԶ����̼���������ɶ�������Ҫ����������75-60��mL=15mL��˵��ԭ��Һ�е�������NaOH��Na2CO3��


 ��һ������Ԫͬ�����ؾ�ϵ�д�
��һ������Ԫͬ�����ؾ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������е����д�ʩ��Ϊ�˸ı仯ѧ��Ӧ���ʵ��ǣ� ��
A.��ʪ�·�����̫����ɹ��
B.��϶�۳��ĵ�����ˮ�������
C.����������Ϳ����
D.��ʳ���ܷ�ã���ֹ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ˮ��Ӧ�����ӷ���ʽ��ȷ���ǣ� ��
A.2Na+3H+�T2Na++H2��
B.Na+H2O�TNa++OH��+H2��
C.2Na+2H2O�T2Na++2OH��+H2��
D.2Na+2H2O�T2Na++O2��+2H2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ü�������NO2��Ⱦ�����о���CH4+2NO2 ![]() N2+CO2+2H2O����1L�ܱ������У����Ʋ�ͬ�¶ȣ��ֱ����0.50molCH4��1.2molNO2�����n(CH4)��ʱ��仯���й�ʵ�����ݼ��±���
N2+CO2+2H2O����1L�ܱ������У����Ʋ�ͬ�¶ȣ��ֱ����0.50molCH4��1.2molNO2�����n(CH4)��ʱ��仯���й�ʵ�����ݼ��±���
��� | �¶� | ʱ��/min n/mol | 0 | 10 | 20 | 40 | 50 |
�� | T1 | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
�� | T2 | n(CH4) | 0.50 | 0.30 | 0.18 | �� | 0.15 |
����˵����ȷ����
A. �����У�0~20min�ڣ�NO2�Ľ�������Ϊ0.0125 mol��L-1��min-1
B. ��ʵ�����ݿ�֪ʵ����Ƶ��¶�T12
C. 40minʱ��������T2Ӧ�������Ϊ0.18
D. 0��10min�ڣ�CH4�Ľ������ʢ�>��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ��ijͬѧ��ƵIJⶨ�к��ȵ�ʵ��װ�á�

��1��ǿ����ǿ���кͷ�Ӧ��ʵ�ʣ��������ӷ�Ӧ��ʾΪ________�� װ����ʹ������ĭ���ϵ�Ŀ����_________��
��2�� ʵ��ʱ��ͬѧ�ȷֱ���50mL�ձ��У�������20mL 2mol/L�������20mL2mol/L��NaOH��Һ���ֱ�����¶ȣ��ֱ�����¶ȵ�Ŀ����________��
��ij�¶�ʱ,��һ��2L���ܱ�������,X��Y��Z�������ʵ����ʵ�����ʱ��ı仯������ͼ��ʾ.����ͼ���������:

��3����Ӧ��ʼ��2min,������Z��ʾ��ƽ����Ӧ����Ϊ_________.
��4���÷�Ӧ�Ļ�ѧ����ʽΪ_________.
��5����X��Y��Z��Ϊ����,2min��Ӧ�ﵽƽ��,��Ӧ��ƽ��ʱ:��ʱ��ϵ��ѹǿ�ǿ�ʼʱ��_________��;��ƽ��ʱ,�����ڻ�������ƽ����Է�����������ʼͶ��ʱ_________(��"����""��С"��"���").
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��X��Y��Z��W�����ڱ��е����λ����ͼ��ʾ������WԪ�ص�ԭ�ӽṹʾ��ͼΪ![]() ��
��
W | X | Y |
Z |
��ش��������⣺
��1��ZԪ����Ԫ�����ڱ��е�λ����___________��
��2��X��Y��Z����Ԫ�ص�ԭ�Ӱ뾶�ɴ�С��˳��Ϊ___________��Ԫ�ط��ű�ʾ����
��3��X��Z��W����Ԫ�ص�����������Ӧˮ�����������ǿ����___________���û�ѧʽ��ʾ����
��4���õ���ʽ��ʾWY2���γɹ��̣�___________��
��5��д��W������Ũ���ᷴӦ�Ļ�ѧ����ʽ��___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£�ij�����м���������̼��ƣ�������ӦCaCO3(s)![]() CaO(s)+CO2(g)���ﵽƽ�⣬����˵����ȷ����
CaO(s)+CO2(g)���ﵽƽ�⣬����˵����ȷ����
A. �������СΪԭ����һ�룬����ϵ�ٴδﵽƽ��ʱ��CO2��Ũ�Ȳ���
B. ���������Ϊԭ����2�����ٴδﵽƽ��ʱ��������ܶȱ��
C. ��CaCO3(s)����������ŷֽ�����CaO(s)��CO2(g)����������H<0
D. ��������ѹǿ���䣬����He��ƽ�����淴Ӧ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ӵ�����ֵΪNA������˵������ȷ����
A. һ��������3.2gSO2������O2��Ӧת�Ƶ�����Ϊ0.1NA
B. 2.9g�춡������������ﺬ��C-H����ĿΪ0.5NA
C. 50mL12mol/LŨ����������MnO2����ת�Ƶ�����0.3NA
D. ��״���£�3.36L���ȼ����к�����ԭ��0.45NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2012��6��16��18ʱ37��24�룬���۾źųɹ����䡣�ɴ���������������̫���ܵ�أ������ڲ������и�Ч��MCFC��ȼ�ϵ�ء���ȼ�ϵ�ؿ�ͬʱ��Ӧ���ˮ������������ȼ��Ϊ�����������Ϊ���ڵ�̼��ء���֪��ȼ�ϵ�ص��ܷ�ӦΪ2H2��O2===2H2O��������ӦΪH2��CO![]() ��2e��===CO2����H2O���������ƶ���ȷ����( )
��2e��===CO2����H2O���������ƶ���ȷ����( )
A.��ع���ʱ��CO![]() ���ƶ�
���ƶ�
B.��طŵ�ʱ�����Ӿ����·��ͨ��������������ͨ�����ĸ���
C.�����ĵ缫��ӦʽΪ4OH����2e��===O2����2H2O
D.ͨ�����ĵ缫Ϊ����������������Ӧ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com