
 AX5(g)在容积为10 L的密闭容器中进行。起始时AX3和X2均为0.2 mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。
AX5(g)在容积为10 L的密闭容器中进行。起始时AX3和X2均为0.2 mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。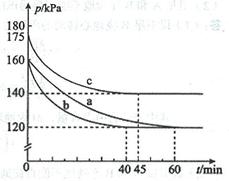
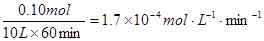 (3 分)
(3 分)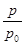 ) (2分) 50%(1分) 40% (1分)
) (2分) 50%(1分) 40% (1分)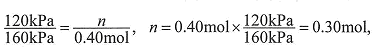
 AX5(g)
AX5(g)
 AX5(g)
AX5(g)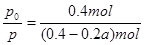 ,化简得α=2(1-
,化简得α=2(1-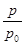 );
);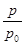 )=2(1-
)=2(1- )=50%;
)=50%;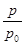 )=2(1-
)=2(1- )=40%。
)=40%。

科目:高中化学 来源:不详 题型:单选题
| A.依据相对分子质量的数据,推测乙醇和丙烷沸点的相对高低 |
| B.依据溶解度的数据,选择用重结晶的方法可将粗苯甲酸提纯 |
| C.依据沸点的数据,判断用分馏的方法从石油中获取汽油和煤油等 |
| D.依据燃烧热的数据、热化学方程式和盖斯定律,可计算一些反应的反应热 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NaOH:固 | B.盐酸:液 | C.NaCl:溶液 | D.H2O:溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.石墨比金刚石稳定 |
| B.金刚石比石墨石稳定 |
| C.1mol石墨比1mol金刚石的总能量高 |
| D.1mol石墨和金刚石完全燃烧时释放的能量石墨比金刚石多 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.ΔH>0表示放热反应,ΔH<0表示吸热反应 |
| B.热化学方程式中的化学计量数只表示物质的量,可以是分数 |
| C.1 mol H2SO4与1 mol Ba(OH)2反应生成BaSO4沉淀时放出的热叫做中和热 |
| D.1 mol H2与0.5 mol O2反应放出的热就是H2的燃烧热 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.由白磷变红磷是吸热反应 |
| B.白磷、红磷都是磷的单质,相互可以自由转化,不吸热,也不放热 |
| C.等质量时,白磷比红磷具有的能量高 |
| D.等物质的量时,断白磷分子中的键比断红磷分子中的键消耗的能量多 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 化学反应 | 平衡常数 | 温度(℃) | |
| 500 | 800 | ||
①2H2(g)+CO(g) CH3OH(g) CH3OH(g) | K1 | 2.5 | 0.15 |
②H2(g)+CO2(g) H2O (g)+CO(g) H2O (g)+CO(g) | K2 | 1.0 | 2.50 |
③3H2(g)+ CO2(g) CH3OH(g)+H2O (g) CH3OH(g)+H2O (g) | K3 | | |
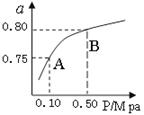
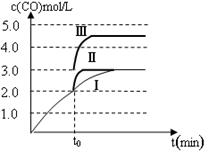
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
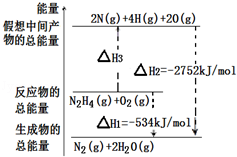
| A.194 | B.391 | C.516 | D.658 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.生成物总能量一定低于反应物总能量 |
B.同温同压下,H2(g)+Cl2(g)=2HCl(g) 在光照和点燃条件下的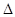 H不同 H不同 |
C.一定条件下,0.5 mol N2和1.5 mol H2置于某密闭容器中充分反应生成NH3气,放热19.3 kJ,其热化学方程式为N2(g)+3H2(g) 2NH3(g) 2NH3(g) 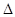 H =-38.6 kJ/mol H =-38.6 kJ/mol |
| D.一定条件下4 HCl(g)+O2(g)=2Cl2(g)+2H2O(g) ,当1 mol |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com