
| A、溶液中粒子浓度大小关系为:c(H+)>c(CH3COO-)>c(CH3COOH)>c(OH-) |
| B、加水稀释到原体积的10倍后溶液pH变为4 |
| C、加入少量乙酸钠固体,溶液pH升高 |
| D、与等体积、pH=3的盐酸比较,跟足量锌粒反应产生的H2一样多 |


 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
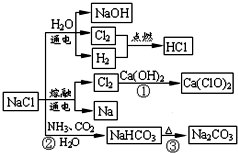
| A、反应②③是侯氏制碱法的原理 |
| B、反应①中的Ca(ClO)2是还原产物 |
| C、常温下干燥Cl2可储存于钢瓶中,所以Cl2与铁不反应 |
| D、图中所示转化反应都是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、NO3-、AlO2-、SO42- |
| B、Na+、Al3+、NO3-、SO42- |
| C、Na+、Mg2+、Cl-、HCO3- |
| D、K+、Cl-、AlO2-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、水电离出的OH-浓度:10c(OH-)甲≤c(OH-)乙 |
| B、溶液的体积:10V甲≤V乙 |
| C、若分别用等浓度的NaOH溶液完全中和,所得溶液的pH:甲≤乙 |
| D、若分别与5mLpH=11的NaOH溶液反应,所得溶液的pH:甲≥乙 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,22.4 L H2O含有的分子数为NA |
| B、500mL1moL/L的盐酸溶液中含有的HCl分子数为0.5NA |
| C、将1L2mol/L的FeCl3溶液制成胶体后,其中含有氢氧化铁胶粒数为2NA |
| D、23gNa与O2在不同条件下反应虽分别生成Na2O和Na2O2,但转移的电子数一定为 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、虚线框中接灵敏电流计,铁被腐蚀,并能将电能转化为化学能 |
| B、虚线框中保持断开状态,铁可能不会被腐蚀 |
| C、虚线框中接直流电源,铁可能不会被腐蚀 |
| D、虚线框中无论接灵敏电流计还是直流电源,铁都会加快腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、需要加热的化学反应都是吸热反应 |
| B、水力发电是将化学能转化为电能的过程 |
| C、某吸热反应能自发进行,因此该反应是熵增反应 |
| D、原电池是将电能转化为化学能的一种装置 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com