
短周期元素X、Y、Z、W、R的化合价与原子序数的关系如图5所示。下列说法正确的是
A.原子半径:Z>Y>X
B.Z和Y形成的化合物是离子化合物
C.气态氢化物的稳定性:Y<R
D.常温下单质W能溶于R的最高价氧化物对应水化物的浓溶液
 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:
氧化还原反应规律是化学学科的重要规律之一。按要求回答下列问题:
(1)被称为万能还原剂的NaBH4溶于水并和水反应:NaBH4+2H2O===NaBO2+4H2↑,此反应中B元素的化合价没有发生变化,则NaBH4中H的化合价为__________,该反应氧化产物是_______,还原产物是____________。
(2)有下列三个反应:
Cl2+FeI2===FeCl2+I2; 2Fe2++Br2===2Fe3++2Br-;
Co2O3+6HCl===2CoCl2+Cl2↑+3H2O
①根据以上方程式可以得到Fe2+、Co2+、Br-、I-还原性由强到弱的顺序为______________;
②1 mol Co2O3能氧化HCl的物质的量是__________________________________
(3)完成并配平下列化学反应方程式:
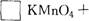



查看答案和解析>>
科目:高中化学 来源: 题型:
CH4和CO2反应可以制造价值更高的化学产品。
(1)250℃时,以镍合金为催化剂,向4 L容器中通入6 mol CO2、6 mol CH4,发生反应:CO2 (g)+CH4(g)  2CO(g)+2H2(g)。平衡体系中各组分的浓度为:
2CO(g)+2H2(g)。平衡体系中各组分的浓度为:
| 物 质 | CH4 | CO2 | CO | H2 |
| 平衡浓度(mol·L-1) | 0.5 | 0.5 | 2.0 | 2.0 |
① 此温度下,该反应的平衡常数K=________(注明单位).
② 已知:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H1 kJ·mol-1
CO(g)+H2O (g)=CO2(g)+H2 (g) △H2 kJ·mol-1
2CO(g)+O2(g)=2CO2(g) △H3 kJ·mol-1
反应CO2(g)+CH4(g)  2CO(g)+2H2(g) 的 △H=_______ kJ·mol-1
2CO(g)+2H2(g) 的 △H=_______ kJ·mol-1
(2)用Cu2Al2O4做催化剂,一定条件下,发生反应: CO2+CH4  CH3COOH, 请回答:
CH3COOH, 请回答:
 ① 温度与催化剂的催化效率和乙酸的生成速率如图。250~300℃时,温度升高而乙酸的生成速率降低的原因是____ _.
① 温度与催化剂的催化效率和乙酸的生成速率如图。250~300℃时,温度升高而乙酸的生成速率降低的原因是____ _.
② 为提高上述反应CH4的转化率,可采取的措施有
_ (写2种)。
③ Cu2Al2O4可溶解在稀硝酸中,被氧化的元素为 ,每消耗3mol Cu2Al2O4时被还原的HNO3为 mol。
(3)Li2O、Na2O、MgO均能吸收CO2,
① 若寻找吸收CO2的其他物质,下列建议合理的是___
a. 可在碱性氧化物中寻找
b. 可在具有强氧化性的物质中寻找
c. 可在ⅠA、ⅡA族元素的氧化物中寻找
② Li4SiO 4可用于吸收、释放CO2, 原理是: 500℃时,CO2与Li4SiO4接触生成Li2CO3;平衡后加热至700℃,反应逆向进行,放出CO2,Li4SiO4再生,该原理的化学方程式_____.
查看答案和解析>>
科目:高中化学 来源: 题型:
单晶硅是制作电子集成电路的基础材料。科学家预计,到2011年一个电脑芯片上将会集成10亿个晶体管,其功能远比我们想象的要大的多,这对硅的纯度要求很高。用化学方法可制得高纯度硅,其化学方程式为 :
①SiO2 + 2C  Si + 2CO ②Si + 2Cl2
Si + 2CO ②Si + 2Cl2 SiCl4
SiCl4
③SiCl4 + 2H2 Si + 4HCl,其中,反应①和③属于( )
Si + 4HCl,其中,反应①和③属于( )
A. 化合反应 B. 分解反应 C. 置换反应 D. 复分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
用下列实验装置或操作进行相应实验,能达到实验目的的是
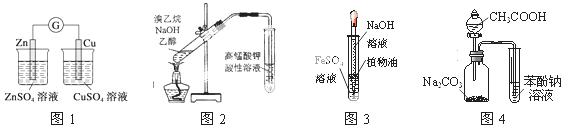
A.用图1装置验证化学能转化为电能
B.用图2所示装置检验溴乙烷与NaOH醇溶液共热产生的乙烯
C.用图3装置制备氢氧化亚铁
D.利用图4装置证明酸性:CH3COOH>H2CO3>苯酚
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度时,向容积为2L的密闭容器中充入一定量的SO2和O2,发生反应:2SO2(g)+O2(g)  2SO3(g)。反应过程中测定的部分数据见下表(表中t1<t2),下列说法正确的是
2SO3(g)。反应过程中测定的部分数据见下表(表中t1<t2),下列说法正确的是
| 反应时间/min | n(SO2)/mol | n(O2)/mol |
| 0 | 0.10 | 0.060 |
| t1 | 0.012 | |
| t2 | 0.016 |
A.反应在0~t1 min内的平均速率为v(SO3)=0.088/t1 mol·L-1·min-1
B.保持其他条件不变,起始时向容器中充入0.10molSO3和0.010 molO2,到达平衡时,n(SO2)=0.012 mol
C.保持其他条件不变,升高温度,平衡时c(SO2)=0.0070mol·L-1,则反应的△H>0
D.相同温度下,起始时向容器中充入0.050molSO2和0.030molO2,达到平衡时SO2转化率小于88%
查看答案和解析>>
科目:高中化学 来源: 题型:
A.【物质结构与性质】
锂—磷酸氧铜电池正极的活性物质是Cu4O(PO4)2,可通过下列反应制备:
2Na3PO4+4CuSO4+2NH3·H2O=Cu4O(PO4)2↓+3Na2SO4+(NH4)2SO4+H2O
(1)写出基态Cu2+的核外电子排布式 ▲ ,上述方程式中涉及到的N、O元素第一电离能由小到大的顺序为 ▲ 。
(2)PO43-的空间构型是 ▲ 。
(3)与NH3互为等电子体的分子、离子有 ▲ 、 ▲ (各举一例)。
(4)氨基乙酸铜的分子结构如图,碳原子的杂化方式为 ▲ 。

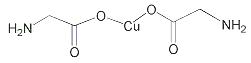
(5)在硫酸铜溶液中加入过量KCN,生成配合物[Cu(CN)4]2-,则1 mol [Cu(CN)4]2-中含有的ơ键的数目为 ▲ 。
(6)Cu元素与H元素可形成一种红色化合物,其晶体结构单元如右图所示。则该化合物的化学式为 ▲ 。
B.【实验化学】
工业上用异丙苯氧化法合成苯酚,其生产流程如下图:

有关物质的性质如下表:
| 物质 | 沸点 | 溶解性 | 主要化学性质 |
| 异丙苯 | 152.4℃ | 不溶于水,易溶于酒精。 | 可被强氧化剂氧化 |
| 苯酚 | 181.8℃ | 微溶于冷水,易溶于热水和酒精等有机溶剂。 | 易被氧化 |
| 丙酮 | 56.2℃ | 易溶于水和有机溶剂 | 不易被氧化 |
(1)检验有机相中是否含有水的方法是 ▲ ;
(2)“操作2”的名称是 ▲ ;
(3)丙酮中常含有苯酚和异丙苯中的一种或者两种有机物杂质,某同学做了如下检验。
| 检验项目 | 实验方案 |
| 检验丙酮中一定存在有机杂质的方法是 ▲ | A. 酸性KMnO4溶液,加热 B. 乙醇,溶解 C. NaOH溶液(酚酞),加热 |
| 检验丙酮中一定含有苯酚的方案是: | 取少许待测液置于试管中,滴加1~2滴FeCl3溶液。预期的实验现象和结论是 ▲ 。 |
(4)为测定某工厂排放的污水中苯酚的含量,进行如下实验:取污水试样10.00mL加水稀释至100mL,加入10.0mL一定浓度的KBrO3和KBr的混合溶液,立即加入5mL盐酸,摇匀后加入1gKI固体(足量),再摇匀,放置5min。用0.01000mol/LNa2S2O3标准溶液滴定至淡黄色,加入1mL淀粉溶液,继续滴定至蓝色刚好褪去,用去Na2S2O3标准溶液14.46mL。同时以水代替污水试样做对比实验,用去Na2S2O3标准溶液38.46 mL。已知上述实验中发生的反应有:
KBrO3+5KBr+6HCl=3Br2+3H2O+6KCl 2Na2S2O3+I2=Na2S4O6+2NaI
则此污水中苯酚的含量(以mg/L表示) ▲ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关气体的叙述中,不正确的是( )
A.一定温度和压强下,各种气体物质体积之比等于分子数之比
B.一定温度和压强下,各种气体物质的密度之比等于摩尔质量之比
C.一定体积和温度下,各种气体物质的物质的量之比等于压强之比
D.气体摩尔体积是指1mol任何气体所占的体积约为22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中不正确的是( )
A. 在共价化合物中也可能含有离子键
B. 非金属之间形成的化学键不一定是共价键
C. 含有共价键的化合物不一定是共价化合物
D. 含有离子键的化合物一定是离子化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com