
ΓΨΧβΡΩΓΩΖ¥”Πa A(g)ΘΪb B(g)![]() c C(g) ΠΛHΘΦ0‘ΎΒ»»ίΧθΦΰœ¬Ϋχ––ΓΘΗΡ±δΤδΥϊΖ¥”ΠΧθΦΰΘ§‘ΎΔώΓΔΔρΓΔΔσΫΉΕΈΧεœΒ÷–ΗςΈο÷ ≈®Ε»Υφ ±Φδ±δΜ·ΒΡ«ζœΏ»γœ¬ΆΦΥυ ΨΘΚ
c C(g) ΠΛHΘΦ0‘ΎΒ»»ίΧθΦΰœ¬Ϋχ––ΓΘΗΡ±δΤδΥϊΖ¥”ΠΧθΦΰΘ§‘ΎΔώΓΔΔρΓΔΔσΫΉΕΈΧεœΒ÷–ΗςΈο÷ ≈®Ε»Υφ ±Φδ±δΜ·ΒΡ«ζœΏ»γœ¬ΆΦΥυ ΨΘΚ
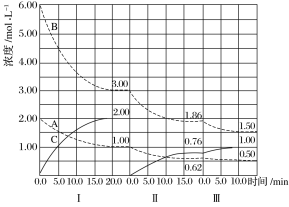
(1)Ζ¥”ΠΒΡΜ·―ßΖΫ≥Χ Ϋ÷–aΓΟbΓΟcΈΣ_____________________________________________ΓΘ
(2)AΒΡΤΫΨυΖ¥”ΠΥΌ¬ vΔώ(A)ΓΔvΔρ(A)ΓΔvΔσ(A)¥”¥σΒΫ–Γ≈≈Ν–¥Έ–ρΈΣ______________ΓΘ
(3)BΒΡΤΫΚβΉΣΜ·¬ ΠΝΔώ(B)ΓΔΠΝΔρ(B)ΓΔΠΝΔσ(B)÷–Ήν–ΓΒΡ «________Θ§Τδ÷Β «________ΓΘ
(4)”…ΒΎ“Μ¥ΈΤΫΚβΒΫΒΎΕΰ¥ΈΤΫΚβΘ§ΤΫΚβœρ________“ΤΕ·Θ§≤…»ΓΒΡ¥κ © «________________________ΓΘ
(5)±»ΫœΒΎΔρΫΉΕΈΖ¥”ΠΈ¬Ε»(T2)ΚΆΒΎΔσΫΉΕΈΖ¥”ΠΈ¬Ε»(T3)ΒΡΗΏΒΆΘΚT2________(ΧνΓΑΘΦΓ±ΓΑΘΨΓ±ΜρΓΑΘΫΓ±)T3Θ§≈–ΕœΒΡάμ”… «_____________________________________________________ΓΘ
ΓΨ¥πΑΗΓΩ1ΓΟ3ΓΟ2 vI(A)ΘΨvΔρ(A)ΘΨvΔσ(A) ΠΝΔσ(B) 19.4% ”“ ¥”ΤΫΚβΜλΚœΈο÷–Ζ÷άκ≥ωΝΥC ΘΨ “ρΈΣΔρΓζΔσΤΫΚβ’ΐœρ“ΤΕ·Θ§ΗΟΖ¥”ΠΈΣΖ≈»»Ζ¥”ΠΘ§Ι ΫΒΈ¬≤≈Ρή ΙΤΫΚβ’ΐœρ“ΤΕ·
ΓΨΫβΈωΓΩ
(1)”…ΆΦΩ…÷ΣΒΎΔώΫΉΕΈΘ§ΤΫΚβ ±Γςc(A)=2mol/L-1mol/L=1mol/LΘ§Γςc(B)=6mol/L-3mol/L=3mol/LΘ§Γςc(C)=2mol/LΘ§≈®Ε»±δΜ·ΝΩ÷°±»Β»”ΎΜ·―ßΦΤΝΩ ΐ÷°±»ΘΜ
(2)vI(A)=![]() =0.05mol/(Lmin)Θ§vΔρ(A)=
=0.05mol/(Lmin)Θ§vΔρ(A)=![]() =0.0253mol/(Lmin)Θ§vΔσ(A)=
=0.0253mol/(Lmin)Θ§vΔσ(A)=![]() =0.012mol/(Lmin)Θ§±»ΫœΩ…“‘ΒΟ≥ω¥πΑΗΘΜ
=0.012mol/(Lmin)Θ§±»ΫœΩ…“‘ΒΟ≥ω¥πΑΗΘΜ
(3)BΒΡΤΫΚβΉΣΜ·¬ ΠΝI(B)=![]() ΓΝ100%=50%Θ§ΠΝΔρ(B)=
ΓΝ100%=50%Θ§ΠΝΔρ(B)=![]() ΓΝ100%=38%Θ§ΠΝΔσ(B)=
ΓΝ100%=38%Θ§ΠΝΔσ(B)=![]() ΓΝ100%=19.4%ΘΜ
ΓΝ100%=19.4%ΘΜ
(4)ΒΎΔρΫΉΕΈC «¥”0ΩΣ ΦΒΡΘ§Υ≤ΦδAΓΔB≈®Ε»≤Μ±δΘ§“ρ¥ΥΩ…“‘»ΖΕ®ΒΎ“Μ¥ΈΤΫΚβΚσ¥”ΧεœΒ÷–“Τ≥ωΝΥCΘ§Φ¥Φθ…Ό…ζ≥…Έο≈®Ε»Θ§ΤΫΚβ’ΐœρ“ΤΕ·ΘΜ
(5)ΒΎΔσΫΉΕΈΒΡΩΣ Φ”κΒΎΔρΫΉΕΈΒΡΤΫΚβΗςΈο÷ ΒΡΝΩΨυœύΒ»Θ§ΗυΨίAΓΔBΒΡΝΩΦθ…ΌΘ§CΒΡΝΩ‘ωΦ”Ω…≈–ΕœΤΫΚβ «’ΐœρ“ΤΕ·ΒΡΘ§ΗυΨίΤΫΚβΩΣ Φ ±≈®Ε»»ΖΕ®¥ΥΤΫΚβ“ΤΕ·≤ΜΩ…Ρή «”…≈®Ε»ΒΡ±δΜ·“ΐΤπΒΡΘ§ΝμΆβΧβΡΩΥυΗχΧθΦΰ»ίΤςΒΡΧεΜΐ≤Μ±δΘ§‘ρΗΡ±δ―Ι«Ω“≤≤ΜΩ…ΡήΘ§“ρ¥Υ“ΜΕ®ΈΣΈ¬Ε»ΒΡ”ΑœλΘ§¥ΥΖ¥”Π’ΐœρΈΣΖ≈»»Ζ¥”ΠΘ§Ω…“‘ΆΤ≤βΈΣΫΒΒΆΈ¬Ε»Θ§ΝμΆβΫαΚœAΒΡΥΌ¬ ‘Ύ»ΐΗωΫΉΕΈΒΡ«ιΩωΘ§»ΖΕ®ΗΡ±δΒΡΧθΦΰ“ΜΕ®ΈΣΫΒΒΆΈ¬Ε»Θ§ΗυΨίά’œΡΧΊΝ–‘≠άμΘ§ΤΫΚβΒΡ“ΤΕ·÷ΜΡήΦθ»θΗΡ±δΘ§≤ΜΡήΒ÷œϊΗΡ±δΘ§“ρ¥Υ¥οΒΫΤΫΚβΚσΈ¬Ε»“ΜΕ®±»ΒΎΔρΫΉΕΈΤΫΚβ ±ΒΡΈ¬Ε»ΒΆΓΘ
(1)”…ΆΦΩ…÷ΣΒΎΔώΫΉΕΈΘ§ΤΫΚβ ±Γςc(A)=2mol/L-1mol/L=1mol/LΘ§Γςc(B)=6mol/L-3mol/L=3mol/LΘ§Γςc(C)=2mol/LΘ§≈®Ε»±δΜ·ΝΩ÷°±»Β»”ΎΜ·―ßΦΤΝΩ ΐ÷°±»Θ§Ι aΘΚbΘΚc=1mol/LΘΚ3mol/LΘΚ2mol/L=1ΘΚ3ΘΚ2ΘΜ
(2)vI(A)=![]() =0.05mol/(Lmin)Θ§vΔρ(A)=
=0.05mol/(Lmin)Θ§vΔρ(A)=![]() =0.0253mol/(Lmin)Θ§vΔσ(A)=
=0.0253mol/(Lmin)Θ§vΔσ(A)=![]() =0.012mol/(Lmin)Θ§Ι AΒΡΤΫΨυΖ¥”ΠΥΌ¬ vΔώ(A)ΘΨvΔρ(A)ΘΨvΔσ(A)Θ§Ι ¥πΑΗΈΣΘΚvΔώ(A)ΘΨvΔρ(A)ΘΨvΔσ(A)ΘΜ
=0.012mol/(Lmin)Θ§Ι AΒΡΤΫΨυΖ¥”ΠΥΌ¬ vΔώ(A)ΘΨvΔρ(A)ΘΨvΔσ(A)Θ§Ι ¥πΑΗΈΣΘΚvΔώ(A)ΘΨvΔρ(A)ΘΨvΔσ(A)ΘΜ
(3)BΒΡΤΫΚβΉΣΜ·¬ ΠΝI(B)=![]() ΓΝ100%=50%Θ§ΠΝΔρ(B)=
ΓΝ100%=50%Θ§ΠΝΔρ(B)=![]() ΓΝ100%=38%Θ§ΠΝΔσ(B)=
ΓΝ100%=38%Θ§ΠΝΔσ(B)=![]() ΓΝ100%=19.4%ΘΜ
ΓΝ100%=19.4%ΘΜ
(4)ΒΎΔρΫΉΕΈC «¥”0
(5)ΒΎΔσΫΉΕΈΒΡΩΣ Φ”κΒΎΔρΫΉΕΈΒΡΤΫΚβΗςΈο÷ ΒΡΝΩΨυœύΒ»Θ§ΗυΨίAΓΔBΒΡΝΩΦθ…ΌΘ§CΒΡΝΩ‘ωΦ”Ω…≈–ΕœΤΫΚβ «’ΐœρ“ΤΕ·ΒΡΘ§ΗυΨίΤΫΚβΩΣ Φ ±≈®Ε»»ΖΕ®¥ΥΤΫΚβ“ΤΕ·≤ΜΩ…Ρή «”…≈®Ε»ΒΡ±δΜ·“ΐΤπΒΡΘ§ΝμΆβΧβΡΩΥυΗχΧθΦΰ»ίΤςΒΡΧεΜΐ≤Μ±δΘ§‘ρΗΡ±δ―Ι«Ω“≤≤ΜΩ…ΡήΘ§“ρ¥Υ“ΜΕ®ΈΣΈ¬Ε»ΒΡ”ΑœλΘ§¥ΥΖ¥”Π’ΐœρΈΣΖ≈»»Ζ¥”ΠΘ§Ω…“‘ΆΤ≤βΈΣΫΒΒΆΈ¬Ε»Θ§ΝμΆβΫαΚœAΒΡΥΌ¬ ‘Ύ»ΐΗωΫΉΕΈΒΡ«ιΩωΘ§»ΖΕ®ΗΡ±δΒΡΧθΦΰ“ΜΕ®ΈΣΫΒΒΆΈ¬Ε»Θ§ΗυΨίά’œΡΧΊΝ–‘≠άμΘ§ΤΫΚβΒΡ“ΤΕ·÷ΜΡήΦθ»θΗΡ±δΘ§≤ΜΡήΒ÷œϊΗΡ±δΘ§“ρ¥Υ¥οΒΫΤΫΚβΚσΈ¬Ε»“ΜΕ®±»ΒΎΔρΫΉΕΈΤΫΚβ ±ΒΡΈ¬Ε»ΒΆΓΘ



| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΦΉΓΪ–ΝΒ»‘ΣΥΊ‘Ύ÷ήΤΎ±μ÷–ΒΡœύΕ‘ΈΜ÷Ο»γΆΦΥυ ΨΓΘΦΉ”κΈλΒΡ‘≠Ή”–ρ ΐœύ≤ν3Θ§Έλ «Ω’Τχ÷–Κ§ΝΩΉνΕύΒΡ‘ΣΥΊΘ§ΕΓ”κ–Ν «Ά§÷ήΤΎ‘ΣΥΊΓΘœ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «Θ® Θ©

A.±ϊ≤ΜΡή”κΥ°ΖΔ…ζΖ¥”Π
B.ΦΚΚΆ¬»ΤχΖ¥”ΠΒΡ≤ζΈο÷Μ”–“Μ÷÷
C.±ϊ”κΗΐΒΡ‘≠Ή”ΚΥΆβΒγΉ” ΐœύ≤ν13
D.““–Έ≥…ΒΡ―θΜ·ΡΛ ηΥ…Θ§≤ΜΡή±ΘΜΛΡΎ≤ψΫπ τ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ(1)≈®Ε»ΨυΈΣ0.01 molΓΛL-1ΒΡ8÷÷»ή“Κ:ΔΌHNO3ΓΓΔΎH2SO4ΓΓΔέCH3COOHΓΓΔήBa(OH)2ΓΓΔίNaOH
ΔόCH3COONaΓΓΔΏKClΓΓΔύNH4Cl,’β–©»ή“ΚpH”…–ΓΒΫ¥σΒΡΥ≥–ρ «(Χν–¥±ύΚ≈)_________ΓΘ
(2)pH=2ΒΡΡ≥ΥαHnA(An+ΈΣΥαΗυ)”κpH=12ΒΡΡ≥ΦνB(OH)mΜλΚœ,«ΓΚΟΖ¥”Π…ζ≥…’ΐ―Έ,ΜλΚœ“ΚpH=8ΓΘ
ΔΌΖ¥”Π…ζ≥…ΒΡ’ΐ―ΈΒΡΜ·―ß ΫΈΣ________ΓΘ
ΔΎΗΟ―Έ÷–____άκΉ”“ΜΕ®ΡήΥ°Ϋβ,ΤδΒΎ“Μ≤ΫΥ°ΫβΒΡάκΉ”ΖΫ≥Χ ΫΈΣ____________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΔώ.A «ά¥Ή‘ ·”ΆΒΡΜυ±ΨΜ·ΙΛ‘≠ΝœΓΘA «ΤχΧ§ΧΰΘ§BΚΆD «…ζΜν÷–ΝΫ÷÷≥ΘΦϊΒΡ”–ΜζΈοΘ§F «ΗΏΖ÷Ή”Μ·ΚœΈοΘ§œύΜΞΉΣΜ·ΙΊœΒ»γΆΦΥυ ΨΘ°
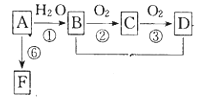
Θ®1Θ©AΖ÷Ή”ΒΡΒγΉ” Ϋ «___ΘΜ
Θ®2Θ©““¥Φ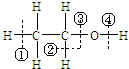 ‘ΎΜ·―ßΖ¥”Π÷–ΕœΦϋΈΜ÷ΟΘΚ““¥Φ‘ΎΆ≠¥ΏΜ·œ¬”κ―θΤχΖ¥”ΠΘ§‘Ύ___ΈΜ÷ΟΕœΝ―ΘΜ
‘ΎΜ·―ßΖ¥”Π÷–ΕœΦϋΈΜ÷ΟΘΚ““¥Φ‘ΎΆ≠¥ΏΜ·œ¬”κ―θΤχΖ¥”ΠΘ§‘Ύ___ΈΜ÷ΟΕœΝ―ΘΜ
Θ®3Θ©–¥≥ωœ¬Ν–Ζ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΘΚ
ΔΌBΓζCΘΚ___ΘΜ
ΔΎAΓζBΘΚ___ΘΜ
Δέ±»AΕύ“ΜΗωΧΦ‘≠Ή”ΒΡ AΒΡΆ§œΒΈοΖΔ…ζΦ”ΨέΖ¥”ΠΒΡΖΫ≥Χ ΫΘΚ___ΓΘ
Δρ.±ΫΚΆ±ΫΒΡΆ§œΒΈο‘ΎΜ·ΙΛ…ζ≤ζ÷–”Π”Ο °Ζ÷ΙψΖΚΓΘ
Θ®1Θ©Ζ÷Ή” ΫΈΣC8H10ΈΣΒΡ±ΫΒΡΆ§œΒΈοΒΡΆ§Ζ÷“λΙΙ”–___÷÷ΘΜ
Θ®2Θ©CH4ΓΔCH2=CH2ΓΔC6H6Β»÷ ΝΩ ±œϊΚΡ―θΤχΉνΕύΒΡΤχΧ§Χΰ «___(ΧνΖ÷Ή” Ϋ)ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ‘ΎCO2÷–Θ§Mg»Φ…’…ζ≥…MgOΚΆCΓΘœ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «Θ® Θ©
A. ‘ΣΥΊCΒΡΒΞ÷ ÷Μ¥φ‘ΎΫπΗ’ ·ΚΆ ·ΡΪΝΫ÷÷Ά§ΥΊ“λ–ΈΧε
B. MgΓΔMgO÷–ΟΨ‘ΣΥΊΈΔΝΘΒΡΑκΨΕΘΚr(Mg2ΘΪ)>r(Mg)
C. ‘ΎΗΟΖ¥”ΠΧθΦΰœ¬Θ§MgΒΡΜΙ‘≠–‘«Ω”ΎCΒΡΜΙ‘≠–‘
D. ΗΟΖ¥”Π÷–Μ·―ßΡή»Ϊ≤ΩΉΣΜ·ΈΣ»»Ρή
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΗΏΟΧΥαΦΊΨΏ”–«Ω―θΜ·–‘Θ§ΙψΖΚ”Ο”ΎΜ·ΙΛΓΔ“Ϋ“©ΓΔ≤…ΩσΓΔΫπ τ÷ΈΝΕΦΑΜΖΨ≥±ΘΜΛΝλ”ρΒ»ΓΘKMnO4ΒΡ÷Τ±Η «“‘Εΰ―θΜ·ΟΧ(MnO2)ΈΣ‘≠ΝœΘ§‘Ύ«ΩΦν–‘Ϋι÷ ÷–±Μ―θΜ·…ζ≥…ΡΪ¬Χ…ΪΒΡΟΧΥαΦΊ(K2MnO4)ΘΜ»ΜΚσ‘Ύ“ΜΕ®pHœ¬K2MnO4ΤγΜ·…ζ≥…Ήœ…ΪKMnO4ΓΘΜΊ¥πœ¬Ν–Έ Χβ
(1)K2MnO4ΒΡ÷Τ±Η
Β―ι≤Ϋ÷η | œ÷œσΜρΫβ Ά |
ΔΌ≥Τ»Γ2.5 gKClO3ΙΧΧεΚΆ5.2gKOHΙΧΧε÷Ο”ΎΧζέαέω÷–Θ§Φ”»»»έ»Ύ | ≤Μ”Ο¥…έαέωΒΡ‘≠“ρ «____________ΓΘ |
ΔΎΖ÷Εύ¥ΈΦ”»κ3gMnO2ΙΧΧε | ≤Μ“Μ¥ΈΦ”»κΒΡ‘≠“ρ «__________________ΓΘ |
(2)KMnO4ΒΡ÷Τ±Η
≥Ο»»œρK2MnO4»ή“Κ÷–Φ”»κ1 mol/L H3PO4»ή“ΚΘ§÷±÷ΝK2MnO4»Ϊ≤ΩΤγΜ·Θ§≈–Εœ»Ϊ≤ΩΤγΜ·ΒΡΖΫΖ® «”Ο≤ΘΝßΑτ’Κ»Γ»ή“Κ”Ύ¬Υ÷Ϋ…œΘ§œ÷œσΈΣ_________________________ΓΘ»ΜΚσ≥Ο»»Ιΐ¬ΥΘ§ΫΪ¬Υ“ΚΒΙ»κ’τΖΔΟσ÷–Φ”»»ΒΫ“ΚΟφ≥ωœ÷ΨßΡΛΘ§≥δΖ÷ά以ΚσΙΐ¬ΥΘ§‘Ύ80ΓφΚφœδ÷–Η…‘ο3hΘ§≤Μ―Γ”ΟΗϋΗΏΈ¬Ε»ΒΡ‘≠“ρ «_____________________________ΓΘ
(3)≤ζΤΖΖ÷Έω
i.≤ΜΆ§pHœ¬≤ζΤΖ÷–KMnO4Κ§ΝΩ
Φ”»κH3PO4ΧεΜΐΘ·mL | »ή“ΚΒΡpH | ≤ζΤΖ÷ ΝΩ | KMnO4÷ ΝΩ | KMnO4÷ ΝΩΖ÷ ΐ |
10.50 | 12.48 | 2.35 | 2.05 | 87.23 |
12.50 | 11.45 | 2.45 | 2.18 | 88.98 |
14.50 | 10.89 | 2.18 | 1.87 | 85.78 |
16.50 | 10.32 | 2.28 | 1.75 | 76.75 |
18.50 | 9.44 | 2.09 | 1.48 | 70.81 |
¥”±μΗώ÷– ΐΨίΖ÷ΈωΘ§‘ΎΤγΜ· ±―Γ‘ώ»ή“ΚΒΡΉνΦ―pH «________________ΓΘ
ii.άϊ”ΟH2C2O4±ξΉΦ»ή“Κ≤βΕ®KMnO4ΒΡ¥ΩΕ»ΓΘ≤βΕ®≤Ϋ÷η»γœ¬ΘΚ
ΔΌ»ή“Κ≈δ÷ΤΘΚ≥Τ»Γ1.000gΒΡKMnO4ΙΧΧε―υΤΖΘ§Ζ≈»κ_____________÷–»ήΫβΘ§»ΜΚσάδ÷Ν “Έ¬Κσ»Ϊ≤ΩΉΣ“ΤΒΫ100mL»ίΝΩΤΩ÷–Θ§Φ”’τΝσΥ°÷ΝΩΧΕ»œΏΓΘ
ΔΎΒΈΕ®ΘΚ“Τ»Γ25 mLKMnO4»ή“Κ”ΎΉΕ–ΈΤΩ÷–Θ§Φ”…ΌΝΩΝρΥαΥαΜ·Θ§”Ο0.1400mol/LΒΡH2C2O4±ξΉΦ»ή“ΚΒΈΕ®Θ§ΖΔ…ζΖ¥”ΠΘΚ2MnO4-ΘΪ5H2C2O4ΘΪ6H+ΘΫ2Mn2ΘΪΘΪ10C02ΘΪ8H2OΘ§Β±»ή“ΚΉœ…ΪΆ …Ϊ«“ΑκΖ÷÷”ΡΎ≤Μ±δ…ΪΦ¥ΈΣ÷’ΒψΘ§ΤΫ––ΒΈΕ®3¥ΈΘ§H2C2O4»ή“ΚΒΡΤΫΨυ”ΟΝΩΈΣ23.90mLΘ§‘ρ―υΤΖ¥ΩΕ»ΈΣ_______________ΘΞ(±ΘΝτ1ΈΜ–Γ ΐ)ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΙΛ“Β…œ÷Τ»Γ±υΨß ·(Na3AlF6)ΒΡΜ·―ßΖΫ≥Χ Ϋ»γœ¬ΘΚ2Al(OH)3+ 12HF+ 3Na2CO3=2Na3AlF6+ 3CO2Γϋ+ 9H2OΘ§ΗυΨίΧβ“βΆξ≥…œ¬Ν–ΧνΩ’ΘΚ
(1) ‘Ύ…œ ωΖ¥”ΠΒΡΖ¥”ΠΈοΚΆ…ζ≥…Έο÷–Θ§ τ”ΎΖ«ΦΪ–‘Ζ÷Ή”ΒΡΒγΉ” Ϋ______Θ§ τ”Ύ»θΥαΒΡΒγάκΖΫ≥Χ Ϋ______ΓΘ
(2)Ζ¥”ΠΈο÷–”–ΝΫ÷÷‘ΣΥΊ‘Ύ‘ΣΥΊ÷ήΤΎ±μ÷–ΈΜ÷ΟœύΝΎΘ§œ¬Ν–Ρή≈–ΕœΥϋΟ«ΒΡΫπ τ–‘ΜρΖ«Ϋπ τ–‘«Ω»θΒΡ «______(―ΓΧν±ύΚ≈)ΓΘ
aΘ°ΤχΧ§«βΜ·ΈοΒΡΈ»Ε®–‘ bΘ°ΉνΗΏΦέ―θΜ·ΈοΕ‘”ΠΥ°Μ·ΈοΒΡΥα–‘
cΘ°ΒΞ÷ ”κ«βΤχΖ¥”ΠΒΡΡ―“Ή dΘ°ΒΞ÷ ”κΆ§≈®Ε»ΥαΖΔ…ζΖ¥”ΠΒΡΩλ¬ΐ
(3)Ζ¥”ΠΈο÷–Ρ≥–©‘ΣΥΊ¥Π”ΎΆ§“Μ÷ήΤΎΓΘΥϋΟ«ΉνΗΏΦέ―θΜ·ΈοΕ‘”ΠΒΡΥ°Μ·Έο÷°ΦδΖΔ…ζΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ______ΓΘ
(4) Na2CO3ΥΉ≥Τ¥ΩΦνΘ§ τ”Ύ______ΨßΧεΓΘΙΛ“Β…œ÷Τ»Γ¥ΩΦνΒΡ‘≠Νœ «______ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩSO2ΓΔNO «¥σΤχΈέ»ΨΈοΘ§NH4NO3ΓΔH2SO4Β» «Υ°ΧεΈέ»ΨΈοΘ§”––ß»Ξ≥ΐ’β–©Έέ»ΨΈο «“Μœν÷Ί“ΣΩΈΧβΓΘ
(1) NOΓΔSO2Ω…“‘œ»―θΜ·Θ§Κσ”ΟΦνΈϋ ’ΓΘΤδ―θΜ·Ιΐ≥ΧΒΡΖ¥”Π‘≠άμ»γœ¬ΘΚ
NO(g)ΘΪO3(g)![]() NO2(g)ΘΪO2(g)ΘΜΠΛH1ΘΫΘ≠200.9 kJΓΛmolΘ≠1
NO2(g)ΘΪO2(g)ΘΜΠΛH1ΘΫΘ≠200.9 kJΓΛmolΘ≠1
SO2(g)ΘΪO3(g)![]() SO3(g)ΘΪO2(g)ΘΜΠΛH2ΘΫΘ≠241.6 kJΓΛmolΘ≠1
SO3(g)ΘΪO2(g)ΘΜΠΛH2ΘΫΘ≠241.6 kJΓΛmolΘ≠1
2SO2(g)ΘΪO2(g)![]() 2SO3(g)ΘΜΠΛH3ΘΫΘ≠196.6 kJΓΛmolΘ≠1
2SO3(g)ΘΜΠΛH3ΘΫΘ≠196.6 kJΓΛmolΘ≠1
‘ρΖ¥”Π2NO2(g)![]() 2NO(g)ΘΪO2(g)ΒΡΠΛHΘΫ____kJΓΛmolΘ≠1ΓΘ
2NO(g)ΘΪO2(g)ΒΡΠΛHΘΫ____kJΓΛmolΘ≠1ΓΘ
(2)ΆΝ»ά÷–ΒΡΝρ―≠ΜΖ»γΆΦΥυ ΨΘ§ΆΝ»ά÷–ΒΡΜΤΧζΩσ(FeS2)‘ΎΙΐ≥ΧΔώ÷–ΜαΉΣΜ·≥…ΝρΥα―«ΧζΚΆΝρΥαΘ§ΗΟΙΐ≥ΧΖΔ…ζΒΡΜ·―ßΖΫ≥Χ ΫΈΣ________________ΓΘ
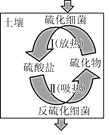
(3)ΒγΫβΖ®≥ΐ»ΞΙΛ“ΒΖœΥ°÷–ΒΡœθΥαοßΒΡΉΑ÷Ο Ψ“βΆΦ»γΆΦΥυ ΨΘ§“θΦΪΒγΦΪΖ¥”Π ΫΈΣ___ΓΘ
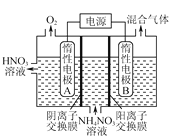
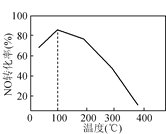
(4)œρΚψ»ίΟή±’»ίΤς÷–≥δ»κ1 mol NOΚΆ2 mol O3Θ§ΖΔ…ζ»γœ¬Ζ¥”ΠΘΚNO(g)ΘΪO3(g)![]() NO2(g)ΘΪO2(g)ΘΜΠΛH<0ΓΘ≤ΜΆ§Έ¬Ε»œ¬Ζ¥”ΠœύΆ§ ±ΦδΚσΘ§ΧεœΒ÷–NOΉΣΜ·¬ ΥφΈ¬Ε»±δΜ·«ζœΏ»γΆΦΓΘΈ¬Ε»ΒΆ”Ύ100Γφ ±Θ§NOΉΣΜ·¬ ΥφΈ¬Ε»…ΐΗΏΕχ‘ω¥σΒΡ÷ς“Σ‘≠“ρ «____ΘΜΒ±Έ¬Ε»ΗΏ ±Θ§O3Ζ÷Ϋβ…ζ≥…Μν–‘ΦΪΗΏΒΡ―θ‘≠Ή”Θ§NOΉΣΜ·¬ ΥφΈ¬Ε»…ΐΗΏΕχΫΒΒΆΘ§Ω…ΡήΒΡ‘≠“ρ”–ΘΚΔΌ______Θ§ΔΎ______ΓΘ
NO2(g)ΘΪO2(g)ΘΜΠΛH<0ΓΘ≤ΜΆ§Έ¬Ε»œ¬Ζ¥”ΠœύΆ§ ±ΦδΚσΘ§ΧεœΒ÷–NOΉΣΜ·¬ ΥφΈ¬Ε»±δΜ·«ζœΏ»γΆΦΓΘΈ¬Ε»ΒΆ”Ύ100Γφ ±Θ§NOΉΣΜ·¬ ΥφΈ¬Ε»…ΐΗΏΕχ‘ω¥σΒΡ÷ς“Σ‘≠“ρ «____ΘΜΒ±Έ¬Ε»ΗΏ ±Θ§O3Ζ÷Ϋβ…ζ≥…Μν–‘ΦΪΗΏΒΡ―θ‘≠Ή”Θ§NOΉΣΜ·¬ ΥφΈ¬Ε»…ΐΗΏΕχΫΒΒΆΘ§Ω…ΡήΒΡ‘≠“ρ”–ΘΚΔΌ______Θ§ΔΎ______ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΩ…ΡφΖ¥”ΠaAΘ®gΘ©+bBΘ®gΘ©cCΘ®gΘ©+dDΘ®gΘ©ΓςHΘ§ΗυΨίΆΦœσ≈–ΕœΘ§œ¬Ν––π ω’ΐ»ΖΒΡ «Θ® Θ©

A.p1ΘΦp2Θ§a+bΘΦc+dΘ§T1ΘΦT2Θ§ΓςHΘΨ0
B.p1ΘΦp2Θ§a+bΘΨc+dΘ§T1ΘΨT2Θ§ΓςHΘΨ0
C.p1ΘΦp2Θ§a+bΘΦc+dΘ§T1ΘΨT2Θ§ΓςHΘΨ0
D.“‘…œ¥πΑΗΨυ≤ΜΕ‘
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΑΌΕ»÷¬–≈ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com