
 CO2��H2(g) ��Ӧ�����вⶨ�IJ������ݼ��±�������t2��t1��:
CO2��H2(g) ��Ӧ�����вⶨ�IJ������ݼ��±�������t2��t1��:| ��Ӧʱ��/min | n(CO)/mol | n(H2O)/ mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | | 0.20 |
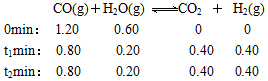
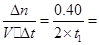 0.20/t1 mol��L��1��min��1
0.20/t1 mol��L��1��min��1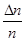 =
=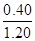 =33.3%
=33.3%

 ͨ��ѧ��Ĭд����ϵ�д�
ͨ��ѧ��Ĭд����ϵ�д� ���ƽ̸�������ѡ����ĩ���100��ϵ�д�
���ƽ̸�������ѡ����ĩ���100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 COOH
COOH CH
CH COO
COO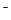 +H
+H ������ ��ƽ�⣬����˵����ȷ���� ( )
������ ��ƽ�⣬����˵����ȷ���� ( )A������ҺpH����ʱ��CH COO COO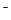 Ũ�ȿ�������Ҳ���ܼ�С Ũ�ȿ�������Ҳ���ܼ�С |
| B���μ�������O.1mol��L��������Һ����Һ��������Ũ�ȼ�С |
| C�����������Ĵ����ƹ��壬ƽ��������Ӧ�����ƶ� |
D������ˮϡ��c(CH COO COO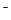 )��c(H )��c(H )/c(CH )/c(CH COOH)��� COOH)��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 N2O4(g) ��H<0���ֽ�һ����NO2��N2O4�Ļ������ͨ�����Ϊ2 L�ĺ����ܱ������У���Ӧ��Ũ����ʱ��仯��ϵ����ͼ��ʾ��
N2O4(g) ��H<0���ֽ�һ����NO2��N2O4�Ļ������ͨ�����Ϊ2 L�ĺ����ܱ������У���Ӧ��Ũ����ʱ��仯��ϵ����ͼ��ʾ��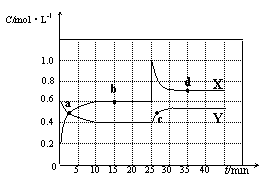
 N2O4(g)��b���ƽ�ⳣ��K(b)= ��
N2O4(g)��b���ƽ�ⳣ��K(b)= �� N2O4(g)��d���ƽ�ⳣ��K(d)��b���ƽ�ⳣ��K(b)�Ĺ�ϵ��
N2O4(g)��d���ƽ�ⳣ��K(d)��b���ƽ�ⳣ��K(b)�Ĺ�ϵ��| A��������� | B����С������� |
| C������һ������NO2 | D������һ������N2O4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 x Q(g) +3R(g)���÷�Ӧ��ƽ��ʱ������2.4mol R�������Q��Ũ��Ϊ0.4 mol/L�������й�������ȷ����
x Q(g) +3R(g)���÷�Ӧ��ƽ��ʱ������2.4mol R�������Q��Ũ��Ϊ0.4 mol/L�������й�������ȷ����| A��xֵΪ2 | B�����������ܶ����� |
| C��ƽ��ʱN��Ũ��Ϊ0.2 mol/L | D��N��ת����Ϊ80% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 z C
z C 2Z(g)+W(g)����H��0���ﵽƽ��ʱ��V��A��=" 1.2a" L��
2Z(g)+W(g)����H��0���ﵽƽ��ʱ��V��A��=" 1.2a" L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2 Z��g�����ﵽƽ��ʱ�������ǵ����ʵ������㣺n��X��+n��Y��= n��Z������Y��ת����Ϊ
2 Z��g�����ﵽƽ��ʱ�������ǵ����ʵ������㣺n��X��+n��Y��= n��Z������Y��ת����Ϊ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
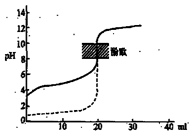
| A����H��0�ķ�Ӧ��������һ�������Է����� |
| B����0.1mol/LNaOH��Һ�ֱ�ζ���ͬ���ʵ���Ũ�Ⱥ���ͬ���������ʹ��ᣬ����ʵ�߱�ʾ���ǵζ���������� |
| C�������£���0.1mol/L��ˮ�У���������NH4Cl���壬��Һ��pH��С |
D�������ܱ������н��еķ�Ӧ3A(g) 2B(g)+C(s)���������������������£��ٳ���һ������A���壬A��ת���ʲ��� 2B(g)+C(s)���������������������£��ٳ���һ������A���壬A��ת���ʲ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 Fe(s)+CO2(g) ��H>0��
Fe(s)+CO2(g) ��H>0��
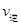 ���<������>����=��������ԭ���� ��
���<������>����=��������ԭ���� ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2SO3 ��H =-196.6kJ/mol����
2SO3 ��H =-196.6kJ/mol����| ���� | �� | �� | �� | �� |
| ��ʼͶ���� | 2m olSO2+1molO2 olSO2+1molO2 | 1molSO2+0.5molO2 | 2molSO3 | 2molSO2+2molO2 |
| ��Ӧ�ų��� ���յ�������kJ) | a | b | c | d |
| ƽ��ʱc��SO3��(mol/L) | e | f | g | h |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com