

| A. | 电解池装置应选择阳离子交换膜 | |
| B. | d 极的电极反应式为:O2+2e-+2H+=H2O2 | |
| C. | 当有16g甲烷参与原电池反应时,可制备4 mol H2O2 | |
| D. | 工作时,a、c电极附近的pH均增大 |
分析 左边甲烷燃料电池a极甲烷为负极,电极反应式为:CH4-8e-+2H2O=CO2+8H+,氧气为正极,右边为电解池,d与负极相连为阴极,O2在阴极得电子放电生成H2O2,电极反应式为:O2+2e-+2H2O=H2O2+2OH-,c与正极相连为阳极,氢氧根离子在阳极放电放出氧气,据此结合选项分析.
解答 解:A、右边为电解池,d与负极相连为阴极,O2在阴极得电子放电生成H2O2,电极反应式为:O2+2e-+2H2O=H2O2+2OH-,所以电解池装置应选择阴离子交换膜,故A错误;
B、d与负极相连为阴极,O2在阴极得电子放电生成H2O2,电极反应式为:O2+2e-+2H2O=H2O2+2OH-,故B错误;
C、左边甲烷为负极,电极反应式为:CH4-8e-+2H2O=CO2+8H+,d与负极相连为阴极,电极反应式为:O2+2e-+2H2O=H2O2+2OH-,根据电子守恒,则当有16g甲烷参与原电池反应时,可制备$\frac{16g}{16g/mol}$×$\frac{8}{2}$=4 mol H2O2,故C正确;
D、a极甲烷为负极,电极反应式为:CH4-8e-+2H2O=CO2+8H+,生成氢离子,c与正极相连为阳极,氢氧根离子在阳极放电放出氧气,消耗氢氧根,所以a、c电极附近的pH均减小,故D错误;
故选C.
点评 本题考查了原电池原理和电解池原理的应用,注意把握原电池正负极的判断以及电极方程式的书写,题目难度不大.


 金钥匙试卷系列答案
金钥匙试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,4.48L辛烷含有的分子数为0.2NA | |
| B. | 0.1 molOD-离子含有的电子、中子数均为 1.0 NA | |
| C. | 一定条件下,0.1 mol N2与0.3mol H2充分反应后得0.1NA个分子 | |
| D. | 总物质的量为0.1mol 的CaO和 CaC2混合物中,所含离子总数为0.2 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯分子中所有原子在同一平面内 | |
| B. | 乙烯分子中含有的官能团是碳碳双键 | |
| C. | 乙烯在一定条件下能与水发生加成反应得到乙醇 | |
| D. | 乙烯能使酸性KMnO4溶液褪色,是因为发生了加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2-甲基戊烷和4-甲基戊烷互为同分异构体 | |
| B. | 分子式为C5H10O2且能与NaHCO3反应的有机物有3种 | |
| C. | 乙醇制备乙烯和乙醇制备乙酸乙酯均为脱水的取代反应 | |
| D. | 苯与液溴在FeBr3作催化剂的条件下发生取代反应,生成溴苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,有关它的说法正确的是( )
,有关它的说法正确的是( )| A. | 它属于芳香烃 | B. | 分子中最多有25个原子共面 | ||
| C. | 分子式为C14H8Cl5 | D. | 1 mol该物质能与6 molH2加成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 8 种 | B. | 12 种 | C. | 24 种 | D. | 28 种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高NH4Cl溶液的温度,其水的离子积常数和pH均增大 | |
| B. | 在有AgI沉淀的上层清液中滴加一定浓度的NaCl溶液,不可能产生白色沉淀 | |
| C. | pH=3的盐酸与pH=11的氨水等体积混合后,溶液中:c(NH4+>c(Cl-)>c(OH-)>c(H+) | |
| D. | 室温下,稀释0.1mol•L-1CH3COOH溶液,溶液的导电能力增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | ①②③④均可与Na、NaOH、H2发生反应,1mol四种物质最多消耗Na、NaOH、H2的物质的量之比依次分别为1:1:1:1、1:2:2:1、4:3:3:5 | |
| B. | ①②③④属同分异构体,分子式为C8H8O3 | |
| C. | 可用银氨溶液或酸性KMnO4溶液区分③④ | |
| D. | ①②③④中所有原子均不可能处于同一平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
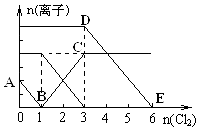 已知:2Fe3++2I-=2Fe2++I2,向1L含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化如图所示.横、纵坐标的单位均为mol.有关说法不正确的是( )
已知:2Fe3++2I-=2Fe2++I2,向1L含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化如图所示.横、纵坐标的单位均为mol.有关说法不正确的是( )| A. | 线段BC代表Fe3+ 物质的量的变化情况 | |
| B. | 原混合溶液中c(FeBr2)=6 mol/L | |
| C. | 当通入Cl22mol时,溶液中已发生的反应可表示为2Fe2++2I-+2Cl2═2Fe3++I2+4Cl- | |
| D. | 原溶液中n (Fe2+):n (I-):n(Br-)=2:1:3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com