
 、
、 、
、 或
或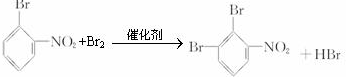 .
.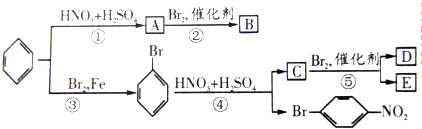
分析 苯与浓硝酸在浓硫酸、加热条件下发生硝化反应生成A为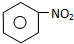 ,与溴发生取代反应,由信息可知,Br取代硝基间位氢原子生成B为
,与溴发生取代反应,由信息可知,Br取代硝基间位氢原子生成B为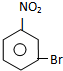 ;
;
苯与溴在催化剂条件下发生取代反应生成溴苯,由信息可知,溴苯与浓硝酸、浓硫酸条件下发生取代反应,硝基取代溴原子邻位、或对位位置氢原子,故C为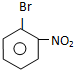 ,C与溴发生取代反应,取代溴原子邻位或对位位置,故生成D、E为
,C与溴发生取代反应,取代溴原子邻位或对位位置,故生成D、E为 、
、 ,据此进行解答.
,据此进行解答.
解答 解:苯与浓硝酸在浓硫酸、加热条件下发生硝化反应生成A为 ,与溴发生取代反应,由信息可知,Br取代硝基间位氢原子生成B为
,与溴发生取代反应,由信息可知,Br取代硝基间位氢原子生成B为 ;苯与溴在催化剂条件下发生取代反应生成溴苯,由信息可知,溴苯与浓硝酸、浓硫酸条件下发生取代反应,硝基取代溴原子邻位、或对位位置氢原子,故C为
;苯与溴在催化剂条件下发生取代反应生成溴苯,由信息可知,溴苯与浓硝酸、浓硫酸条件下发生取代反应,硝基取代溴原子邻位、或对位位置氢原子,故C为 ,C与溴发生取代反应,取代溴原子邻位或对位位置,故生成D、E为
,C与溴发生取代反应,取代溴原子邻位或对位位置,故生成D、E为 、
、 ,
,
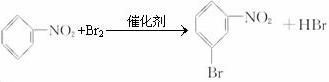
第②步反应为 与溴在催化剂存在条件下反应生成
与溴在催化剂存在条件下反应生成 ,反应的化学方程式为:
,反应的化学方程式为: ;
;
第④步:溴苯与浓硝酸、浓硫酸条件下发生取代反应,硝基取代溴原子邻位、或对位位置氢原子,反应的化学方程式为: ;
;
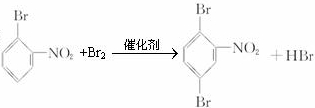
第⑤步:C为 ,C与溴发生取代反应,取代溴原子邻位或对位位置,故生成D、E为
,C与溴发生取代反应,取代溴原子邻位或对位位置,故生成D、E为 、
、 ,反应的方程式为:
,反应的方程式为: 或
或 ,
,
故答案为: ;
; ;
; 或
或 .
.
点评 本题考查有机物的推断,题目难度中等,需要学生对给予的信息进行利用,注意把握题中取代反应的重要信息,较好的考查学生的自学能力,注意积累基础知识,以及知识的综合利用.


 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 醋酸除去水垢中:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 铜和浓硝酸反应:Cu+4H++2NO${\;}_{3}^{-}$═Cu2++2NO2↑+2H2O | |
| C. | 向氨水中通入过量SO2:2NH3•H2O+SO2═2NH${\;}_{4}^{+}$+SO${\;}_{3}^{2-}$+H2O | |
| D. | H2SO4溶液和Ba(OH)2溶液:H++SO${\;}_{4}^{2-}$+Ba2+═BaSO4↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 非自发反应在任何条件下都不能实现 | |
| B. | 自发反应都是熵增大的反应 | |
| C. | 能自发进行的吸热反应一定是熵增大的反应 | |
| D. | 自发反应都是放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3的电离方程式:NaHCO3═Na++H++CO32- | |
| B. | CaCO3的沉淀溶解平衡表达式:CaCO3(s)?Ca2+(aq)+CO32-(aq) | |
| C. | NaHS发生水解的离子方程式:HS-+H2O?S2-+H3O+ | |
| D. | 碳酸的电离方程式:H2CO3?2H++CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol•L-1K2SO4溶液中含有钾离子数为2NA | |
| B. | 0.1mol铁与0.1mol氯气点燃完全反应,转移电子数为0.3NA | |
| C. | 常温常压下,6.4g氧气和臭氧混合气体中含有的原子总数为0.4NA | |
| D. | 1L1mol•L-1氨水中,含有的NH3与NH3•H20分子的总数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 在一密闭容器中发生反应N2+3H2?2NH3,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:
在一密闭容器中发生反应N2+3H2?2NH3,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
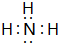 ;分子中既含有极性共价键、又含有非极性共价键的18电子化合物有H2O2、N2H4(写出其中两种的化学式).
;分子中既含有极性共价键、又含有非极性共价键的18电子化合物有H2O2、N2H4(写出其中两种的化学式).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com