
铁在冷的浓硫酸中能发生钝化。某兴趣小组的同学发现将一定量的铁与浓硫酸加热时,观察到铁完全溶解,并产生大量气体。实验室现有下列试剂:0.01 mol/L酸性KMnO4溶液、0.1 mol/L KI溶液、3%H2O2溶液、淀粉溶液、蒸馏水。请你协助他们探究所得溶液和气体的成分。
【提出猜想】
Ⅰ.所得溶液中的金属离子可能含有Fe2+和Fe3+中的一种或两种;
Ⅱ.所得气体中可能含有________中的一种或两种。
| 实验操作 | 预期现象 | 结论 |
验证猜想Ⅰ | 步骤①:取少量0.01 mol/L酸性KMnO4溶液,滴入所得溶液 |
|
|
步骤②:________ |
| 含有Fe3 | |
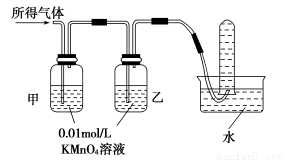
验证猜想Ⅱ | 将所得气体通入如下装置 |
| 含有两种气体 |
【实验探究】
【问题讨论】
有同学提出,若另外选用KSCN溶液,则仅利用KSCN和H2O2两种溶液即可完成猜想Ⅰ的所有探究,判断该方法是否正确并进行评价:_____________________________
【提出猜想】Ⅱ.SO2、H2
溶液紫红色褪去 含有Fe2+(或溶液紫红色不褪去,不含Fe2+)
另取少量所得溶液,滴加KI?淀粉溶液 溶液变为蓝色
甲中KMnO4溶液褪色,乙中KMnO4溶液颜色不变,试管中收集到气体
【问题讨论】 不正确,若溶液中含有Fe3+,则无法检验溶液中是否含有Fe2+
【解析】解答本题时应注意以下三点:
(1)明确实验的目的是验证溶液和气体的成分;
(2)根据溶液中可能存在的离子Fe2+(铁过量)、Fe3+或两者的混合物,选择合适的试剂进行检验;
(3)根据气体的可能成分SO2和H2选择合适的试剂进行检验。
铁与浓硫酸加热时,产生的金属离子可能有Fe2+(铁过量)、Fe3+,产生的气体可能有H2(铁过量)、SO2。Fe2+可以使酸性KMnO4溶液褪色,Fe3+具有氧化性,可把I-氧化成I2可使KI?淀粉溶液变为蓝色;SO2可以使酸性KMnO4溶液褪色,并被其吸收。


科目:高中化学 来源:2014年高考化学一轮复习课后规范训练2-3练习卷(解析版) 题型:填空题
取一定量的酸性KMnO4溶液依次进行下列实验,有关现象记录如下:
①滴加适量H2O2,紫红色褪去,并有气泡产生;
②再加入适量的PbO2固体,固体溶解,溶液又变为紫红色;
③最后通入足量的SO2气体。
请回答下列问题:
(1)KMnO4、H2O2、PbO2氧化性由强到弱的顺序为____________________;
(2)实验③中的现象为_____________________________________________________;
(3)实验①、②中反应的离子方程式分别是__________、________。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练1-3练习卷(解析版) 题型:填空题
“84消毒液”能有效杀灭甲型H1N1病毒,某同学购买了一瓶某品牌“84消毒液”,
并查阅相关资料和消毒液包装说明得到如下信息:
“84消毒液”:含25% NaClO、1 000 mL、密度1.19 g·cm-3,稀释100倍(体积比)后使用。请根据以上信息和相关知识回答下列问题:
(1)该“84消毒液”的物质的量浓度为________mol·L-1。
(2)该同学取100 mL该品牌“84消毒液”稀释后用于消毒,稀释后的溶液中c(Na+)≈________mol·L-1(假设稀释后溶液密度为1.0 g·cm-3)。
(3)该同学参阅该品牌“84消毒液”的配方,欲用NaClO固体配制480 mL含25% NaClO的消毒液。下列说法正确的是________。
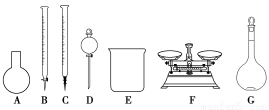
A.如图所示的仪器中,有四种是不需要的,还需一种玻璃仪器
B.容量瓶用蒸馏水洗净后,应烘干才能用于溶液配制
C.利用购买的商品NaClO来配制可能导致结果偏低
D.需要称量的NaClO固体质量为143 g
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练1-2练习卷(解析版) 题型:选择题
用酸性氢氧燃料电池电解饱和食盐水的装置如图所示(a、b为石墨电极,不考虑U形管
中气体的溶解且a上产生的气体全部进入小试管中)。下列说法中错误的是( )
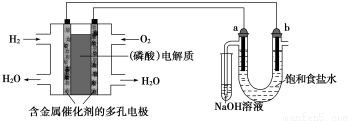
A.同温同压下,燃料电池中参与反应的H2和O2的体积之比为2∶1
B.同等条件下,U形管a、b两端产生的气体的密度之比为35.5∶1
C.燃料电池中消耗0.2 g H2时,U形管中阴极产生的气体为2.24 L(标准状况下)
D.燃料电池中消耗1 mol O2时,小试管中反应转移的电子数约为4×6.02×1023
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练1-2练习卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值。下列叙述正确的是( )
A.1 mol甲醇中含有C—H键的数目为4NA
B.25 ℃,pH=13的NaOH溶液中含有OH-的数目为 0.1NA
C.标准状况下,2.24 L己烷含有分子的数目为0.1NA
D.常温常压下,Na2O2与足量H2O反应,共生成0.2 mol O2,转移电子的数目为0.4NA
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练1-1练习卷(解析版) 题型:选择题
根据以下叙述制备氯化铜:先将浓盐酸用蒸汽加热至80 ℃左右,慢慢加入含有FeO杂质的CuO粉,充分反应,使其溶解。已知:FeS不溶于水,但溶于酸。
溶液中被沉淀离子 | Fe3+ | Fe2+ | Cu2+ |
完全生成氢氧化物沉淀时,溶液的pH | ≥3.7 | ≥9.6 | ≥6.4 |
在除去溶液中的Fe2+时,可采用的方法是( )
A.可直接加碱,调整溶液的pH≥9.6
B.加入纯铜粉,将Fe2+还原为Fe
C.先将Fe2+氧化成Fe3+,再调整溶液pH至3~4
D.通入H2S使Fe2+直接沉淀
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习2-3-2氧化还原反应方程式配平及计算练习卷(解析版) 题型:填空题
氧化还原反应综合应用:氧化还原反应滴定
(1)配平氧化还原反应方程式:
C2O42-+ MnO4-+ H+= CO2↑+ Mn2++ H2O
(2)称取6.0 g含H2C2O4·2H2O、KHC2O4和K2SO4的试样,加水溶解,配成250 mL溶液。量取两份此溶液各25 mL,分别置于两个锥形瓶中。
①第一份溶液中加入酚酞试液,滴加0.25 mol·L-1 NaOH溶液至20 mL时,溶液由无色变为浅红色。该溶液被中和的H+的总物质的量为 mol。
②第二份溶液中滴加0.10 mol·L-1的酸性高锰酸钾溶液。
A.KMnO4溶液在滴定过程中作 (填“氧化剂”或“还原剂”),该滴定过程 (填“需要”或“不需要”)另加指示剂。滴至16 mL时反应完全,此时溶液颜色由 变为 。
B.若在接近终点时,用少量蒸馏水将锥形瓶冲洗一下,再继续滴定至终点,则所测结果 (填“偏大”、“偏小”或“无影响”)。
C.若在达到滴定终点时俯视读数,则所得结果 (填“偏大”、“偏小”或“无影响”)。
③原试样中H2C2O4·2H2O的质量分数为 ,KHC2O4的质量分数为 。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学 题型四 离子反应型专题练习卷(解析版) 题型:选择题
下列表示对应化学反应的离子方程式正确的是( )
A.稀硝酸中加入过量铁粉:Fe+4H++NO3-=Fe3++NO↑+2H2O
B.用铜作电极电解饱和食盐水:2Cl-+2H2O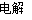 Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
C.向NH4HCO3中滴加少量的NaOH溶液:NH4++OH-=NH3·H2O
D.用氨水溶解Cu(OH)2:Cu(OH)2+4NH3·H2O=[Cu(NH3)4]2++2OH-+4H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com