
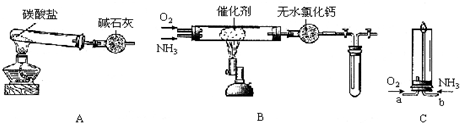
分析 (1)碳酸盐加热分解能产生NH3,只有(NH4)2CO3或NH4HCO3,碱石灰可以吸收酸性气体,并用于干燥氨气;
(2)氨气在催化剂作用下反应生成一氧化氮和水,为放热反应,一氧化氮不稳定,容易与空气中的氧气反应生成红棕色的二氧化氮;由于2NO2(g)?N2O4(g);△H<0,正反应为放热反应,当温度降低时,平衡向正反应方向移动,依次进行判断;
(3)若先通入NH3,NH3在空气中不能点燃,可在纯氧中安静燃烧.
解答 解:(1)碳酸盐加热分解能产生NH3,只有(NH4)2CO3或NH4HCO3,碱石灰可以吸收酸性气体,并用于干燥氨气,所以碱石灰的作用:吸收水和二氧化碳;
故答案为:(NH4)2CO3或NH4HCO3;吸收水和二氧化碳;
(2)将产生的氨气与过量的氧气通到装置B中,用酒精喷灯加热催化剂至红热,熄灭酒精喷灯,反应仍能继续进行,说明反应是放热反应,反应的方程式为4NH3+5O2 $\frac{\underline{催化剂}}{△}$4NO+6H2O,将试管浸入冰水中,由于2NO2(g)?N2O4(g)△H<0,正反应为放热反应,当温度降低时,平衡向正反应方向移动,部分红棕色的NO2转化为无色N2O4,故颜色变浅.
故答案为:放;4NH3+5O2 $\frac{\underline{催化剂}}{△}$4NO+6H2O;浅;2NO2?N2O4 △H<0,降温平衡向正反应方向移动,部分红棕色的NO2转化为无色N2O4;
(3)由于装置C上端开口,要点燃NH3,须先通入O2,后通入NH3,因为若先通入NH3,NH3在空气中不能点燃,NH3逸出会造成污染,反应的化学方程式为4NH3+3O2 $\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O,
故答案为:先通O2,后通NH3;4NH3+3O2 $\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O.
点评 本题考查无机物的性质实验,为信息给予题,为高考常见题型,题目侧重考查氨气的有关性质,做题时注意题中“氨气可在纯氧中安静燃烧…”这一重要信心,结合氨气的性质解答问题,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | SO2具有氧化性,可用于漂白纸浆 | B. | NH4HCO3含有氮元素,可用作氮肥 | ||
| C. | Fe2(SO4)3易溶于水,可用作净水剂 | D. | Al2O3硬度大,可用作耐高温材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
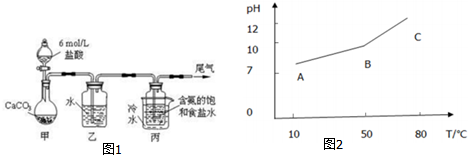
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.16 | 0.143 | 0.102 | 0.099 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | -1 | -2 |
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
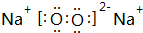 (用电子式表示)
(用电子式表示)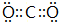 (用电子式表示)
(用电子式表示)查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 油脂分子中都含有碳碳双键 | B. | 葡萄糖分子中含有羟基和醛基 | ||
| C. | 水分子中含有羟基 | D. | 乙酸乙酯分子中含有羧基 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com