
【题目】下列关于苯的叙述正确的是( ) 
A.反应①为取代反应,有机产物浮在上层
B.反应②为氧化反应,反应现象是火焰明亮并伴有浓烟
C.反应③为取代反应,只生成一种产物
D.反应④中1 mol苯最多与3 mol H2发生加成反应,因为苯分子含有3个碳碳双键
科目:高中化学 来源: 题型:
【题目】下列各溶液中的离子,因氧化还原反应而不能大量共存的是 ( )
A.Na+、HCO3-、K+、OH-B.Fe3+、SCN-、NH4+、Cl-
C.Fe2+、H+、SO42-、NO3-D.AlO2-、OH-、Na+、NH4+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石油裂解气用途广泛,由石油裂解气合成生物可降解高聚物J的合成线路如图: 
已知:
i.酯与酯可发生如下酯交换反应:RCOOR'+R″OH ![]() RCOOR″+R'OH ( R、R'、R“代表烃基)
RCOOR″+R'OH ( R、R'、R“代表烃基)
ii.烯烃中,碳碳双键相邻为不稳定结构,碳碳双键易被氧化剂氧化.
(1)A为链状烃,其核磁共振氢谱中有两组峰且面积之比是1:2,则A的名称为 .
(2)B 中所含官能团名称为 .
(3)C→D的反应类型 .
(4)C能与足量的 NaHCO3溶液反应生成C4H2O4Na2 , C的结构简式为 .
(5)D→E的化学方程式是 .
(6)H中不含甲基,H与E形成对称型高聚物J的化学方程式是 .
(7)请完成 B→C 的合理路线 . (无机试剂任选)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】热电厂用碱式硫酸铝[Al2(SO4)3Al2O3]吸收烟气中低浓度的二氧化硫.具体过程如下:
(1)碱式硫酸铝溶液的制备 往Al2(SO4)3溶液中加入一定量CaO粉末和蒸馏水,可生成碱式硫酸铝(络合物,易溶于水),同时析出生石膏沉淀[CaSO42H2O],反应的化学方程式为 .
(2)SO2的吸收与解吸.吸收液中碱式硫酸铝活性组分Al2O3对SO2具有强大亲和力,化学反应为:Al2(SO4)3Al2O3(aq)+3SO2(g)Al2(SO4)3Al2(SO3)3(aq)△H<0.工业流程如图1所示: 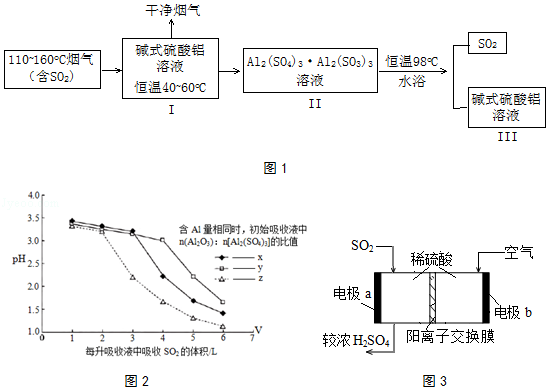
①高温烟气可使脱硫液温度升高,不利于SO2的吸收.生产中常控制脱硫液在恒温40~60oC,试分析原因 .
②研究发现,I中含碱式硫酸铝的溶液与SO2结合的方式有2种:其一是与溶液中的水结合.其二是与碱式硫酸铝中的活性Al2O3结合,通过酸度计测定不同参数的吸收液的pH变化,结果如2图所示:
据此判断初始阶段,SO2的结合方式是 . 比较x、y、z的大小顺序 .
③III中得到再生的碱式硫酸铝溶液,其n(Al2O3):n[Al2(SO4)3]比值相对I中有所下降,请用化学方程式加以解释: .
(3)解吸得到较纯的SO2 , 可用于原电池法生产硫酸如图3. ①电极b周围溶液pH(填“变大”、“变小”或“不变”)
②电极a的电极反应式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组制备氢氧化亚铁沉淀.
实验1 |
| 实验现象 |
液面上方产生白色絮状沉淀,迅速变为灰绿色,振荡,试管壁上有红褐色沉淀生成. |
(1)实验1中产生白色沉淀的离子方程式是 .
(2)为了探究沉淀变灰绿色的原因,该小组同学展开如下探究: ①甲同学推测灰绿色物质为Fe(OH)2和Fe(OH)3混合物.查阅资料后根据调色原理认为白色和红褐色的调和色不可能是灰绿色,并设计实验证实灰绿色物质中不含有Fe(OH)3 , 方案是 .
②乙同学查阅文献:Fe(OH)2在大量SO42﹣存在的情况下形成Fe6(SO4)2(OH)4O3(一种氧基碱式复盐).并设计对比实验证实该假设:向试管中加入 , 再往试管中加入 , 振荡,现象与实验1相同,结论是该假设不成立.
③乙同学继续查阅文献:Fe(OH)2沉淀具有较强的吸附性能,灰绿色可能是由Fe(OH)2表面吸附Fe2+引起.推测所用的硫酸亚铁溶液的浓度应越小越好;氢氧化钠溶液浓度应越大越好.设计了如下实验方案:
试管中10mL | 滴加 | 实验现象 | |
实验2 | 6mol/L | 0.2mol/L FeSO4溶液 | 产生悬浮于液面的白色沉淀(带有少量灰绿色),沉淀下沉后,大部分灰绿色变为白色沉淀 |
实验3 | 6mol/L | 0.1mol/L FeSO4溶液 | 产生悬浮于液面的白色沉淀(带有极少量灰绿色),沉淀下沉后,底部都为白色沉淀 |
该实验得出的结论是 , 能说明灰绿色是由Fe(OH)2表面吸附Fe2+引起的证据是 . 丙同学认为该实验方案不足以证明灰绿色是由Fe(OH)2表面吸附Fe2+引起的,还需补充的实验是 , 证明该假设成立.
(3)丙同学探究温度对氢氧化亚铁制备实验的影响:取少量灰绿色沉淀,在水浴中加热,颜色由灰绿变白,且有絮状白色沉淀下沉,原因为 .
(4)根据以上实验探究,若尽可能制得白色Fe(OH)2沉淀,需要控制的实验条件 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用锌与稀硫酸反应制取氢气,欲使产生的速率加快,下列措施可行的是( )
A. 加水稀释B. 加少量NaOH溶液
C. 改用的浓硫酸D. 加入适量CuSO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】槟榔碱在医疗上常用于治疗青光眼,其一种合成路线如图: 
已知:Ⅰ.不饱和化合物与氨(NH3)或胺(R﹣NH2)反应能生成新的胺类化合物
如:R1﹣CH=CH2+R2﹣NH2 ![]() R1﹣CH2﹣CH2﹣NH﹣R2
R1﹣CH2﹣CH2﹣NH﹣R2
Ⅱ. ![]() +R3
+R3![]()
![]()
 +R2OH
+R2OH
(1)B中含氧官能团的名称为 .
(2)反应①的反应类型为;反应②的反应条件为 .
(3)反应③的化学方程式为 .
(4)C的结构简式为 .
(5)下列说法正确的是(填字母). a.反应④为取代反应
b.槟榔碱与化合物G互为同系物
c.1mol D最多能与2mol NaOH发生反应
(6)已知A在NaOH溶液中水解的产物之一是一种新型功能高分子材料(PAANa)的单体,写出生成PAANa的化学方程式 .
(7)已知:CH2=CHCH3+Cl2 ![]() CH2=CHCH2Cl+HCl,以丙烯和乙醇为起始原料,选用必要的无机试剂合成A,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件) .
CH2=CHCH2Cl+HCl,以丙烯和乙醇为起始原料,选用必要的无机试剂合成A,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件) .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:用Pt﹣Rh合金催化氧化NH3制NO,其反应的微观模型及含氮生成物产率随反应温度的变化曲线分别如图①、图②所示:下列说法中,不正确的是( ) 
A.400℃时,生成的产物有N2、NO、H2O
B.800℃时,反应的化学方程式是:4NH3+5O2 ![]() ?4NO+6H2O
?4NO+6H2O
C.400℃﹣800℃间,Pt﹣Rh合金对N2的吸附力逐渐减弱
D.800℃以上,发生了反应:2NO(g)?O2(g)+N2(g)△H>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验过程如图所示,则图③试管中的现象是( ) 
A.铜片溶解,产生无色气体,该气体遇空气变为红棕色
B.铜片溶解,产生无色气体,该气体遇到空气不变色
C.铜片溶解,放出红棕色有刺激性气味的气体
D.无明显现象,因稀硫酸不与铜反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com