
【题目】恒温恒容条件下,反应2AB(g)![]() A2(g)+B2(g)达到平衡状态的标志是
A2(g)+B2(g)达到平衡状态的标志是
A. 单位时间内生成n mol A2,同时消耗2n mol AB
B. 容器内,3种气体AB、A2、B2共存
C. 容器中各组分的体积分数不随时间变化
D. AB的消耗速率等于A2的消耗速率
【答案】C
【解析】
当化学反应达到平衡状态时,正逆反应速率相等,各物质的浓度不变,由此衍生的一些物理量也不发生变化,注意该反应中反应物化学计量数之和等于生成物的化学计量数之和的特点。
A.化学反应速率之比等于化学计量数之比,无论是否达到平衡状态,都存在单位时间内生成nmolA2,同时消耗2nmolAB,故A不选;
B.容器内,3种气体AB、A2、B2共存时不能说明正逆反应速率相等,则不一定处于平衡状态,故B不选;
C.容器中各组分的体积分数不随时间变化,说明反应达到平衡状态,故C选;
D.AB的消耗速率等于A2的消耗速率说明正逆反应速率不相等,反应没有达到平衡状态,故D不选;
故答案选C。


科目:高中化学 来源: 题型:
【题目】一定条件下,分别对反应C(s)+CO2(g)![]() 2CO(g)(ΔH>0)进行如下操作(只改变该条件):①升高反应体系的温度;②增加反应物C的用量;③缩小反应体系的体积;④减少体系中CO的量。上述措施中一定能使反应速率显著变大的是
2CO(g)(ΔH>0)进行如下操作(只改变该条件):①升高反应体系的温度;②增加反应物C的用量;③缩小反应体系的体积;④减少体系中CO的量。上述措施中一定能使反应速率显著变大的是
A.①②③④B.①③④C.①②D.①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中,反应X(g)+2Y(g)![]() Z(g)分别在三种不同实验条件下进行,它们的起始浓度均为c(X)=0.100mol·L-1,c(Y)=0.200mol·L-1,c(Z)=0mol·L-1。反应物X的浓度随时间的变化如图所示。下列说法正确的是
Z(g)分别在三种不同实验条件下进行,它们的起始浓度均为c(X)=0.100mol·L-1,c(Y)=0.200mol·L-1,c(Z)=0mol·L-1。反应物X的浓度随时间的变化如图所示。下列说法正确的是
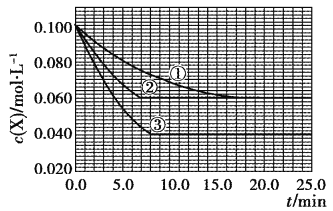
A. 实验②的温度高于实验①的温度
B. 实验②平衡时Y的转化率为60%
C. 实验③与实验①相比,实验③使用了催化剂
D. 反应X(g)+2Y(g)![]() Z(g)的△H>0
Z(g)的△H>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应2Cu+Ag2O=Cu2O+2Ag可设计成如图所示的原电池。普通水泥在固化过程中其自由水分子减少并形成碱性溶液,根据这一物理化学特点,科学家利用该电池发明了电动势法测水泥的初凝时间。下列有关说法正确的是( )
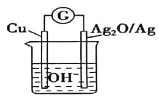
A.电子流动方向从Cu→Ag2O→电解质溶液→Cu,形成闭合回路
B.正极的电极反应式为Ag2O+2H++2e-=2Ag+H2O
C.2molCu与1molAg2O的总能量低于1molCu2O与2molAg的总能量
D.电池工作时,OH-向Cu极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】月球含有H、He、N、Na、Mg、Si等元素,是人类未来的资源宝库。
(1)3He是高效核能原料,其原子核内中子数为_____________。
(2)Na的原子结构示意图为______,Na在氧气中完全燃烧所得产物的电子式为_______。
(3)MgCl2在工业上应用广泛,可由MgO制备。
①MgO的熔点比BaO的熔点________(填“高”或“低”)
②月球上某矿石经处理得到的MgO中含有少量SiO2,除去SiO2的离子方程式为______;SiO2的晶体类型为________。
③MgO与炭粉和氯气在一定条件下反应可制备MgCl2。若尾气可用足量NaOH溶液完全吸收,则生成的盐为______(写化学式)。
(4)月壤中含有丰富的3He,从月壤中提炼1 kg3He同时可得6000kgH2和700kgN2,若以所得H2和N2为原料经一系列反应最多可制得碳酸氢铵___kg。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸溶液中存在电离平衡CH3COOH![]() H++CH3COO-,下列叙述不正确的是
H++CH3COO-,下列叙述不正确的是
A. 升高温度,平衡正向移动,醋酸的电离常数Ka值增大
B. 0.l0mol/L的CH3COOH溶液中加水稀释,溶液中c(OH-)增大
C. CH3COOH溶液中加少量的CH3COONa固体,平衡逆向移动
D. 室温下,欲使0.1mol/L醋酸溶液的pH,电离度a都减小,可加入少量水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关阿伏加德罗常数NA的叙述中不正确的是( )
A.1mol NaHSO4固体所含的阳离子数目为NA
B.常温常压下,92 g的NO2和N2O4混合气体含有的原子数为6NA
C.标准状况下,22.4L HF含有电子数为8NA
D.60g石英晶体中含有的Si-O键数目为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.某实验小组为探究ClO-、I2、SO42-在酸性条件下的氧化性强弱,设计实验如下:
实验①:在淀粉-碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;
实验②:向实验①的溶液中加入4mL 0.5 mol·L-1的亚硫酸钠溶液,蓝色恰好完全褪去。
(1)写出实验①中发生反应的离子方程式:____。
(2)实验②的化学反应中转移电子的物质的量是____。
Ⅱ.(3)Cl2、H2O2、ClO2(还原产物为Cl-)、O3(1mol O3转化为1mol O2和1mol H2O)等物质常被用作消毒剂。等物质的量的上述物质消毒效率最高的是____(填序号)。
A.Cl2 B.H2O2 C.ClO2 D.O3
(4)“84”消毒液(主要成分是NaClO)和洁厕剂(主要成分是浓盐酸)不能混用,原因是____(用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】类推思维是化学解题中常用的一种思维方法,下列有关反应方程式的类推正确的是
已知 | 类推 | |
A | 将Fe加入CuSO4溶液中Fe+Cu2+===Cu+Fe2+ | 将Na加入到CuSO4溶液中2Na+Cu2+===Cu+2Na+ |
B | 稀硫酸与Ba(OH)2溶液反应至中性:2H++SO42-+Ba2++2OH-===BaSO4↓+2H2O | NaHSO4溶液与Ba(OH)2溶液反应至中性2H++SO42-+Ba2++2OH-===BaSO4↓+2H2O |
C | 铁和氯气反应2Fe+3Cl2 | 铁和碘单质反应2Fe+3I2 |
D | 向Ca(ClO)2溶液中通入少量CO2:Ca2++2ClO-+CO2+H2O===CaCO3↓+2HClO | 向Ca(ClO)2溶液中通入少量SO2:Ca2++2ClO-+SO2+H2O===CaSO3↓+2HClO |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com