
| A. | 煤的干馏、石油的裂解都是化学变化 | |
| B. | 用CO2合成聚碳酸酯等可降解塑料,减少白色污染 | |
| C. | 光化学烟雾、硝酸型酸雨的形成都与氮氧化合物有关 | |
| D. | 人造纤维、合成纤维和光导纤维都属于有机高分子化合物 |
分析 A.有新物质生成的变化为化学变化;
B.聚乙烯、聚氯乙烯塑料难以降解,大量使用会造成白色污染;
C.依据光化学烟雾、酸雨的成因解答;
D.光导纤维主要成分二氧化硅;
解答 解:A.煤的干馏、石油的裂解都有新物质生成,都是化学变化,故A正确;
B.用CO2合成聚碳酸酯等可降解塑料,可以减少聚乙烯、聚氯乙烯塑料的使用,减少白色污染,故B正确;
C.光化学烟雾、硝酸型酸雨的形成都与氮氧化合物有关,故C正确;
D.光导纤维主要成分二氧化硅,二氧化硅为无机物,不属于有机高分子化合物,故D错误;
故选:D.
点评 本题为综合题,考查了化学变化的判断、环境污染与保护、材料类型,明确相关知识是解题关键,题目难度不大.


 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源: 题型:选择题
| A. | 用浓盐酸与铁屑反应制取H2:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O | |
| C. | 用醋酸除去水垢:CaCO3+2CH3COOH═Ca2++2CH3COO-+H2O+CO2↑ | |
| D. | 将氯气溶于水制备次氯酸:Cl2+H2O═2H++Cl-+ClO- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3 | B. | 5 | C. | 4 | D. | 7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
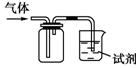 如图装置可用于收集SO2并验证其某些化学性质,下列说法正确的是( )
如图装置可用于收集SO2并验证其某些化学性质,下列说法正确的是( )| 选项 | 试剂 | 现象 | 结论 |
| A | 酸性KMnO4溶液 | 溶液褪色 | SO2有氧化性 |
| B | 品红溶液 | 溶液褪色 | SO2有漂白性 |
| C | NaOH溶液 | 无明显现象 | SO2与NaOH溶液不反应 |
| D | 紫色石蕊试液 | 溶液变红色后不褪色 | SO2有酸性,没有漂白性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离核近的区域运动 | B. | 离核远的区域运动 | ||
| C. | 无法确定运动区域离核远近 | D. | 化学变化中较难失去 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 A、B、C、D、E、F、G为前四周期元素.A、B最外层电子排布可表示为asa、bsbbpb;C元素对应单质是空气中含量最多的物质;D的最外层电子数是内层电子数的3倍;E与D同主族,且位于D的下一周期;F与E同周期,且是本周期中电负性最大的元素:基态G原子核外电子填充在7个能级中,且价层电子均为单电子.
A、B、C、D、E、F、G为前四周期元素.A、B最外层电子排布可表示为asa、bsbbpb;C元素对应单质是空气中含量最多的物质;D的最外层电子数是内层电子数的3倍;E与D同主族,且位于D的下一周期;F与E同周期,且是本周期中电负性最大的元素:基态G原子核外电子填充在7个能级中,且价层电子均为单电子.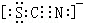 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com