
下列说法合理的是
A.金属锂、镁在氧气中燃烧的产物分别为Li2O、MgO
B.H—F、H—O、H—N三个共价键的极性逐渐增强
C.若X+和Y2-的核外电子层结构相同,则元素电负性X>Y
D.邻羟基苯甲醛沸点高于对羟基苯甲醛是因为形成了分子内氢键
科目:高中化学 来源:2014-2015学年福建省高三上学期第四次月考化学试卷(解析版) 题型:选择题
下列物质的分类全部正确的是
A.NO2——酸性氧化物 、 Na2O2——碱性氧化物 、 Al2O3——两性氧化物
B.汽油——混合物 、 胆矾——纯净物 、 O3——单质
C.纯碱——碱 、 硫化氢——酸 、 小苏打——酸式盐
D.液氯——非电解质 、 硫酸钡——强电解质、 醋酸——弱电解质
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高三上学期10月月考化学试卷(解析版) 题型:选择题
SO2通入足量Fe(NO3)3稀溶液中,溶液由棕色变为浅绿色,但立即又变为棕黄色,这时若滴入BaCl2溶液,会产生白色沉淀。针对上述一系列变化过程中,下列说法中不正确的是
A.上述过程中,最终被还原的是NO3—
B.从上述过程中可以得出结论,氧化性:HNO3>Fe3+>稀H2SO4
C.假设通入的SO2完全反应,则同温同压下,SO2和逸出气体的体积为1∶1
D.上述过程中,会产生一种无色无味的难溶于水的气体
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省德阳市高三一诊考试化学试卷(解析版) 题型:填空题
(10分)甲、乙、丙均为中学化学常见的气体单质,A、B、C为常见的化合物,A和B都极易溶于水,用玻璃棒分别蘸取A和B的浓溶液后,相互靠近会看到白烟。各物质之间存在如下图所示的转化关系:

请回答下列问题:
(1)丙与A反应生成乙和C的化学反应方程式为——————
(2)向0.1 mol/L的C溶液中通入A至显中性,溶液中各离子浓度由大到小的顺序为:__________.
(3)常温下取M的饱和溶液与AgI的饱和溶液等体积混合,再加入足量的AgNO3浓溶液发生反应,则生成沉淀的物质的量较多的是________。(填化学式)
(4)电解尿素[CO(NH2)2]的碱性溶液制取甲的装置示意图如右图(电解池中隔膜仅阻止气体通过,a、b极均为惰性电极)。

电解时,b极的电极反应是_______。若在a极产生112mL气体(标准状况),则消耗尿素的质量为______g。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省德阳市高三一诊考试化学试卷(解析版) 题型:选择题
下列图示与对应的叙述不相符的是
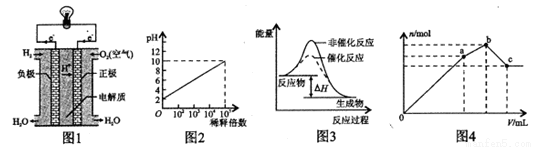
A.图1表示氢氧燃料电池构造示意图
B.图2表示室温下pH=2的HCl溶液加水稀释倍数与pH的变化关系
C.图3表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化
D.图4表示向NH4 Al(SO4)2溶液中逐滴滴入Ba(OH)2溶液,生成沉淀总物质的量(n)随着Ba(OH)2溶液体积(y)的变化
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省日照市高三12月校际联合检测化学试卷(解析版) 题型:实验题
(14分)某化学兴趣小组为研究生铁(含碳)与浓硫酸的反应情况及产物性质,设计如下实验。请回答下列问题:
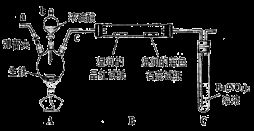
(1)按上图所示装置进行实验(夹持装置及尾气处理装置未画出)。仪器b的名称为_____________:实验过程中,装置B中观察的现象是_______________;装置C中有白色沉淀生成,该沉淀是______________(填化学式)。
(2)装置A中还会产生CO2气体,请写出产生CO2的化学方程式:________________________。
(3)为了验证装置A中产生的气体中含有CO2,应先从下列①~④中选出必要的装置连接A装置中c处管口,从左到右的顺序为_______________(填序号);然后再进行的操作是从a处多次鼓入N2,其目的是________________________________。

(4)某同学通过验证实验后期装置A中产生的气体中还含有H2,理由是_____________(用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省日照市高三12月校际联合检测化学试卷(解析版) 题型:选择题
T℃时,某浓度醋酸钠溶液的pH=10,下列说法一定正确的是
A.溶液中由水电离出的OH一离子浓度c(OH一)=1×10一10mol/L
B.溶液中存在:c(H+)·c(OH一)=l×10-14(mol/L)2
C.溶液中存在:c(Na+)>c(CH3COO一)>c(OH一)>c(H+)>c(CH3COOH)
D.溶液中存在:c(CH3COOH)+c(CH3COO一)=c(Na+)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省高密市高三12月检测理综化学试卷(解析版) 题型:选择题
某离子反应涉及H2O、ClO—、IO3—、OH—、I2、Cl—六种微粒。其中c(ClO—)随反应进行逐渐减小。下列判断错误的是
A.该反应的还原剂是I2
B.氧化剂与还原剂的物质的量之比为5:2
C.消耗l mol氧化剂,转移2 mol电子
D.反应后溶液的碱性明显减弱
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高三上学期12月月考化学试卷(解析版) 题型:填空题
(14分)如下图中A~J分别代表有关反应中的一种中学化学常见单质或化合物,其中B、C、D、I均为无色气体,G为白色沉淀。(部分产物和反应条件已略去)

(1)若A加热后得到等物质的量的B和C,则A的化学式为 。
(2)实验室检验B的方法是 。
(3)写出上述由I生成J的化学方程式: 。
(4)写出C和少量Na[Al(OH)4]溶液反应的离子方程式: 。
(5)若实验室要制备纯净的物质C(可含水蒸气)所需试剂最好选择 (填代号)。
A.石灰石
B.稀硝酸
C.稀硫酸
D.稀盐酸
E.纯碱
所需气体发生装置是 (填代号);所选装置中涉及的玻璃仪器的名称为________________________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com