
【题目】常温下,关于pH相同的氨水和氢氧化钠溶液,下列说法正确的是( )
A.c(NaOH)>c(NH3·H2O)
B.c(![]() )=c(Na+)=c(OH-)
)=c(Na+)=c(OH-)
C.两种溶液中水的电离程度相同
D.等体积的氨水和氢氧化钠溶液分别与相同浓度的盐酸完全中和时,消耗的盐酸体积相同
【答案】C
【解析】
A.NH3·H2O是弱电解质,pH相同的氨水和氢氧化钠溶液,c(NH3·H2O)>c(NaOH),故A错误;
B.氨水中存在一水合氨和水的电离平衡,故溶液中的离子有氢离子、氢氧根和铵根离子,根据电荷守恒可有:c(OH-)=c(![]() )+c(H+),同理,在NaOH溶液中:c(OH-)=c(Na+)+c(H+),又因为两溶液pH相同,故c(
)+c(H+),同理,在NaOH溶液中:c(OH-)=c(Na+)+c(H+),又因为两溶液pH相同,故c(![]() )=c(Na+)<c(OH-),故B错误;
)=c(Na+)<c(OH-),故B错误;
C.pH相同的氨水和氢氧化钠溶液,水电离的H+浓度相同,两种溶液中水的电离程度相同,故C正确;
D.NH3·H2O是弱电解质,电离程度小,浓度大,等体积的氨水和氢氧化钠溶液分别与相同浓度的盐酸完全中和时,氨水所消耗的盐酸体积多,故D错误;
答案选C。


科目:高中化学 来源: 题型:
【题目】NA 为阿伏加德罗常数的值。下列说法正确的是
A.2.24L(标准状况下)甲苯在O2中完全燃烧,得到0.7NA个CO2分子
B.1mo1乙酸(忽略挥发损失)与足量的C2H518OH浓硫酸作用下加热,充分反应可生成NA个CH3CO18OC2H5分子
C.14g乙烯和丙烯混合气体中的氢原子数为2NA
D.常温常压下,78g苯含有σ键数为6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对有机物性质进行探究,下列描述不正确的是
A.对甲基苯甲醛(![]() )能使酸性高锰酸钾溶液褪色,说明它含有醛基
)能使酸性高锰酸钾溶液褪色,说明它含有醛基
B.将铜丝在酒精灯的外焰上加热变黑后再移至内焰,铜丝又恢复到原来的红色
C.向2mL10%的NaOH溶液中滴几滴CuSO4溶液,再加入乙醛溶液加热有红色沉淀产生
D.向苯酚溶液中滴加几滴稀溴水出现白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是一些晶体的结构示意图。请回答下列问题:
(1)下图为金刚石晶胞,则1个金刚石晶胞含有_________个碳原子。若碳原子半径为r,金刚石晶胞的边长为a,根据硬球接触模型,则r=_________a。
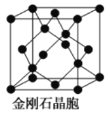
(2)下图为钛酸钡晶体的晶胞结构,该晶体经X—射线分析得出,重复单位为立方体,顶点位置被Ti4+所占据,体心位置被Ba2+所占据,棱心位置被O2-所占据。
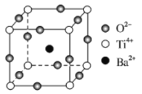
①在该物质的晶体中,每个Ti4+周围与它距离最近且相等的Ti4+有_____个,它们的空间构型为_____。O2-的钡配位数是______。
②若将Ti4+置于晶胞的体心,Ba2+置于晶胞顶点,则O2-处于立方体的______位置。
(3)PbS是一种重要的半导体材料,具有NaCl型结构(如下图),其中阴离子采用面心立方最密堆积方式,X—射线衍射实验测得PbS的晶胞参数为a=0.594nm。
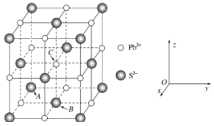
①已知坐标参数:A(0,0,0),B(![]() ,
,![]() ,0),则C 的坐标参数为 ________ 。
,0),则C 的坐标参数为 ________ 。
②PbS晶体的密度为______ gcm-3。(列出计算式即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物I(C11H12O3)是制备液晶材料的中间体之一,其分子中含有醛基和酯基。I可以用 E和 H 在一定条件下合成:
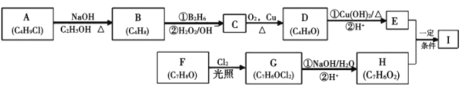
已知以下信息:①A 的核磁共振氢谱表明其只有一种化学环境的氢;
②R—CH=CH2![]() R— CH2CH2OH;
R— CH2CH2OH;
③ 化合物F苯环上的一氯代物只有两种;
④ 通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基。
请回答下列问题:
(1)A 所含官能团的名称是 ____________ 。C→D 的反应类型为 __________
(2)C 的名称为 ___________ ,I的结构筒式为 ___________ 。
(3)写出 D→E 第①步反应的化学方程式;________________ ;
(4)I的同系物J比I相对分子质量小14,J的同分异构体中能同时满足如下条件:①苯环上只有两个取代基,②既能发生银镜反应,又能与饱和NaHCO3溶液反应放出CO2,共有_________种(不考虑立体异构)。J的一种同分异构体发生银镜反应并酸化后核磁共振氢谱为三组峰,且峰面积比为2:2:1,写出J的这种同分异构体的结构简式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏伽德罗常数的值。关于常温下pH=2的H2SO4溶液,溶液中不存在H2SO4分子,但存在HSO4一离子,下列说法错误的是
A.每升溶液中的H+数目为0.01NA
B.Na2SO4溶液中:c(Na+)=2c(SO42-)>c(H+)=2c(OH-)
C.向稀硫酸中逐滴滴加浓硫酸,溶液中![]() 减小
减小
D.NaHSO4不是弱电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化合物的同分异构体数目与分子式为C3H6Cl2的同分异构体数目相同的是
A.![]() B.C8H8O2(含苯环且属于酸)
B.C8H8O2(含苯环且属于酸)
C.C3H8O2D.C7H8O(含苯环)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解质溶液的电导率越大,导电能力越强。用![]() 的NaOH溶液滴定
的NaOH溶液滴定![]() 浓度均为
浓度均为![]() 的
的![]() 和
和![]() 溶液。利用传感器测得滴定过程中溶液的电导率如图所示。下列说法正确的是
溶液。利用传感器测得滴定过程中溶液的电导率如图所示。下列说法正确的是![]()
![]()
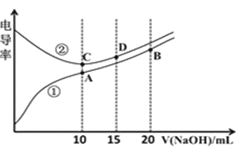
A.C点溶液呈酸性,A点溶液呈碱性
B.A点溶液中:![]()
C.在相同温度下,A、B、C三点溶液中水的电离程度:![]()
D.D点溶液中:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化镁(MgO2)产品中常混有少量MgO,甲、乙两小组分别设计了两种实验方案测定样品中过氧化镁的质量分数。
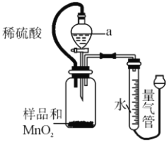
方案Ⅰ:取一定量过氧化镁样品,加入少量的MnO2,搅拌使其充分混合,再向其中滴加足量的稀硫酸(如图)。
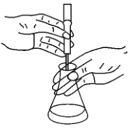
方案Ⅱ:称取0.1000g样品置于碘量瓶中,加入足量KI溶液和稀硫酸,滴加几滴指示剂X,摇匀后在暗处静置5 min,然后用0.1000 mol·L-1 Na2S2O3的标准溶液滴定至终点(如图),消耗Na2S2O3溶液30.00 mL。(已知:I2+2Na2S2O3=Na2S4O6+2NaI)
回答下列问题:
(1)方案Ⅰ实验前检验气密性的方法是________。仪器a的名称是________,使用该仪器的优点是________。
(2)广口瓶内发生的化学反应方程式为:MgO2+H2SO4=MgSO4+H2O2,________。
(3)方案Ⅱ滴定过程中若操作过慢,导致结果________(填“偏高”“偏低”或“无影响”)。指示剂X为________,判断到滴定终点的现象为________。
(4)根据方案Ⅱ实验数据,样品中过氧化镁的质量分数为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com