
分析 (1)依据①N2H4(l)+O2(g)=N2(g)+2H2O(g)△H1=-534kJ/mol
$②{H}_{2}O(g)+\frac{1}{2}{O}_{2}(g)={H}_{2}{O}_{2}(l)$△H2=+98kJ/mol
N2H4和液态H2O2反应的方程式为:N2H4(l)+2H2O2(l)=N2(g)+4H2O(g),可由①-②×2得到,根据盖斯定律,焓变为△H=△H1-2△H2
(2)N2H4设计的碱性燃料电池,负极电极N2H4失去电子与OH-反应生成N2和H2O;
(3)50mL 0.018mol/L 的AgNO3与50mL 0.020mol/L 的盐酸混合,生成AgCl沉淀,发生反应Ag++Cl-?AgCl.
解答 解:(1)依据①N2H4(l)+O2(g)=N2(g)+2H2O(g)△H1=-534kJ/mol
$②{H}_{2}O(g)+\frac{1}{2}{O}_{2}(g)={H}_{2}{O}_{2}(l)$△H2=+98kJ/mol
N2H4和液态H2O2反应的方程式为:N2H4(l)+2H2O2(l)=N2(g)+4H2O(g),可由①-②×2得到,根据盖斯定律,焓变为△H=△H1-2△H2=-730kJ/mol.
故答案为N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-730 kJ/mol;
(2)N2H4设计的碱性燃料电池,负极电极N2H4失去电子与OH-反应生成N2和H2O,反应方程式为:N2H4-4e-+4OH-═N2+4H2O.
故答案为:N2H4-4e-+4OH-═N2+4H2O;
(3)50mL 0.018mol/L 的AgNO3与50mL 0.020mol/L 的盐酸混合,生成AgCl沉淀,忽略溶液体积变化,起始浓度$c(A{g}^{+})=\frac{0.018mol/L}{2}=0.009mol/L$,$c(C{l}^{-})=\frac{0.020mol/L}{2}=0.010mol/L$,Ag++Cl-?AgCl,最终HCl剩余,整个反应没有H+参与反应,则$c({H}^{+})=\frac{0.02mol/L}{2}=0.01mol/L$,pH=-lgc(H+)=2;
最终剩余c(Cl-)=0.010-0.009=0.001mol/L,则溶液中$c(A{g}^{+})=\frac{{K}_{sp}(AgCl)}{c(C{l}^{-})}=\frac{1.0×1{0}^{-10}}{0.001}=1.0×1{0}^{-7}mol/L$.
故答案为:2,1.0×10-7mol/L.
点评 本题考察热化学方程式,盖斯定律,沉淀溶解平衡,溶液pH的计算,电解反应等知识,较为综合,题目难度不大,是基础题.


 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.2mol/L的硫酸10mL | B. | 0.25mol/L的盐酸20mL | ||
| C. | 18.4mol/L的硫酸30mL | D. | 0.3mol/L的硝酸20mL |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH、H2SO4、(NH4)2SO4 | B. | HCl、Al2O3、MgCl2 | ||
| C. | Na2CO3、HNO3、MgO | D. | Ba(OH)2、Na2SO4、Na3PO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  如图验证溴乙烷发生消去反应生成烯烃 | |
| B. | 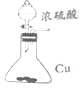 如图进行浓硫酸与铜的反应 | |
| C. |  如图实验验证酸性:CH3COOH>H2CO3>C6H5OH | |
| D. |  如图吸收氨气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com