
| ���� | X | Y | Z | W |
| ��ʼŨ��/mol?L-1 | 1.0 | 2.0 | 0 | 0 |
| ƽ��Ũ��/mol?L-1 | 0..4 | 0.2 | 1.2 | 0.6 |
| A����Ӧ�ﵽƽ��ʱ��Y��ת����Ϊ90% |
| B����Ӧ�ɱ�ʾΪX��g��+3Y��g���T2Z��g��+W��g������ƽ�ⳣ��Ϊ270 L?mol-1 |
| C������ѹǿƽ��������Ӧ�����ƶ���ƽ�ⳣ������ |
| D���ı��¶Ȼ���ƽ����ϵ�м���X����ʹƽ���ƶ���ƽ�ⳣ��Ҳ����֮�ı� |
| ת����Ũ�� |
| ��ʼŨ�� |
| ת����Ũ�� |
| ��ʼŨ�� |
| 2.0-0.2 |
| 2.0 |
| 1.2 2��0.6 |
| 0.4��0.2 3 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��CH4 C2H4 |
| B��CH4 C3H6 |
| C��C2H4 C3H4 |
| D��CH4 C3H4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����25g CuSO4?5H2O����100 mL����ˮ�У�����100mol l.0 mol/LCuSO4��Һ |
| B������NH4+ʱ���������м���NaOH��Һ���ȣ���ʪ��ĺ�ɫʯ����ֽ�����ݳ������� |
| C���ü��ȷֽ�ķ�������̼���ƺ�̼���������ֹ��� |
| D����������Һ���������Ǻ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| A�����л���ķ���ʽ��C15H27O4N4 |
| B���÷����к��а������Ȼ����ǻ���ȩ���ȹ����� |
| C���÷��Ӳ����������ԣ����ܷ���ˮ�ⷴӦ��������Ӧ |
| D���÷����к���5������̼ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
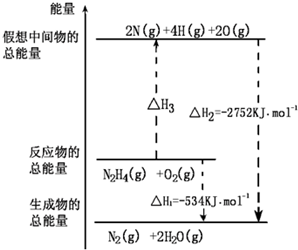 �£�H2NNH2����һ�ָ���ȼ�ϣ��йػ�ѧ��Ӧ�������仯��ͼ����֪����1mol��ѧ�������������kJ����N��NΪ942��N-HΪ391��O=OΪ500�������1molN-N�������������kJ���ǣ�������
�£�H2NNH2����һ�ָ���ȼ�ϣ��йػ�ѧ��Ӧ�������仯��ͼ����֪����1mol��ѧ�������������kJ����N��NΪ942��N-HΪ391��O=OΪ500�������1molN-N�������������kJ���ǣ�������| A��1327 | B��391 |
| C��516 | D��154 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
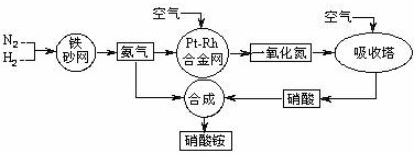
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ������ҺA |
| ��ַ�Ӧ |
| ������ҺB |
| ��ַ�Ӧ |
| A����ҺA����ҺB�������������NaOH��Һ |
| B������һ���ܲ�������������������ʣ��ͭ |
| C������ҺBѡ��Ũ���ᣬ���ͭ����������ƫ�� |
| D��ʵ�����з����������ʵʩ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��0.1 mol/L Na2S2O3��H2SO4��5 mL����ˮ5 mL����Ӧ�¶�10�� |
| B��0.1 mol/L Na2S2O3��H2SO4��5 mL����ˮ10 mL����Ӧ�¶�10�� |
| C��0.1 mol/L Na2S2O3��H2SO4��5 mL����ˮ5 mL����Ӧ�¶�30�� |
| D��0.2 mol/L Na2S2O3��H2SO4��5 mL����ˮ10 mL����Ӧ�¶�30�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����֪a g��ϩ������ȼ��ʱ����1 mol CO2��Һ̬ˮ���ų�b kJ�����������ʾ��ϩȼ���ȵ��Ȼ�ѧ����ʽΪ2C2H4��g��+6O2��g���T4CO2��g��+4H2O��l����H=-4b kJ?mol-1 | ||||
| B����֪��H2��g��+F2��g���T2HF��g����H=-270 kJ?mol-1����1 mol������1 mol������Ӧ����2 molҺ̬������ų�������С��270 kJ | ||||
C��500�桢30 MPa�£���0.5 mol N2��1.5 mol H2�����ܱյ������г�ַ�Ӧ����NH3��g��������19.3 kJ�����Ȼ�ѧ����ʽΪN2��g��+3H2��g��
| ||||
| D����֪����C��s��ʯī��+O2��g���TCO2��g����H=-393.5 kJ?mol-1����C��s�����ʯ��+O2��g���TCO2��g����H=-395.0 kJ?mol-1����C��s�����ʯ���TC��s��ʯī����H=-1.5 kJ?mol-1 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com