
| A、6.4 gS6与S8的混合物中所含S原子数一定为0.2 NA |
| B、1 L 0.1 mol.L-1的醋酸溶液中氢离子数为0.1 NA |
| C、以惰性电极电解NaCl溶液时,每放出11.2LCl2时,则消耗NaCl个数为NA |
| D、在密闭容器盛有0.1molN2和0.3molH2,在一定条件下充分反应,转移的电子数为0.6NA |
| 6.4g |
| 32g/mol |
| 6.4g |
| 32g/mol |


科目:高中化学 来源: 题型:
| 催化剂 |
| 实验 编号 | T(℃) | NO初始浓度 (mol/L) | CO初始浓度 (mol/L) | 催化剂的比表面积(m2/g) |
| Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| Ⅱ | 280 | 1.20×10-3 | 5.80×10-3 | 124 |
| Ⅲ | 350 | 1.20×10-3 | 5.80×10-3 | 124 |
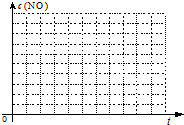
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、质子数:a>c>b>d |
| B、离子的还原性:Y2->Z- |
| C、离子半径:Y2->Z->X+>W3+ |
| D、元素电负性大小顺序:Y>Z |
查看答案和解析>>
科目:高中化学 来源: 题型:
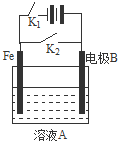 根据图示装置,下列说法不正确的是( )
根据图示装置,下列说法不正确的是( )| 选项 | 开关状态 | 溶液A | 电极B | 说明 |
| A | 打开K1,闭合K2 | NaCl | 石墨 | 正极反应:O2+2H2O+4e-=4OH- |
| B | 打开K1,闭合K2 | NaCl | Zn | 铁制品保护:牺牲阳极的阴极保护法 |
| C | 打开K2,闭合K1 | CuSO4 | Cu | 铁表面镀铜 |
| D | 打开K2,闭合K1 | CuSO4 | 粗铜 | 电解法精炼铜 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、27g铝的原子最外层电子总数为NA |
| B、2.8 g N2和2.8 g CO所含电子数均为1.4NA |
| C、1L0.1mol?L-1乙酸溶液中H+数为0.1NA |
| D、标准状况下,22.4L乙醇的分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下4.6g NO2和N2O4混合气体所含原子总数为0.3NA |
| B、标准状况下,22.4L SO3的分子数为NA |
| C、1molFe在22.4L的Cl2(标准状况下)燃烧,转移的电子总数为3NA |
| D、电解58.5 g熔融的NaCl,能产生22.4 L氯气(标准状况)、23.0 g金属钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该化合物仅含碳、氢两种元素 |
| B、该化合物中碳、氢原子个数比为1:2 |
| C、无法确定该化合物是否含有氧元素 |
| D、该化合物中一定含有氧元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
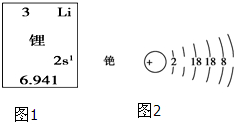 碱金属元素在科学研究与生产生活中有着非常广泛的用途.
碱金属元素在科学研究与生产生活中有着非常广泛的用途.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com