
目前国内外使用的融雪剂一般有两大类:一类是以醋酸钾为主要成分的有机融雪剂;另一类是以“氯盐”为主要成分的无机融雪剂,如氯化钠、氯化钙、氯化镁等,通称“化冰盐”。某研究性学习小组拟对融雪氯盐(主要含有氯化钠及不溶性杂质、Mg2+、Ca2+等)进行回收提纯研究。
| 化学式 | CaCO3 | CaSO3 | CaC2O4 | Mg(OH)2 |
| Ksp | 2.8×10-9 | 6.8×10-8 | 4.0×10-9 | 1.8×10-11 |
该小组设计流程如图:
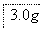

(1)加入混合液A的主要成分是________________(填化学式)。
(2)为检验溶液B中的Mg2+、Ca2+,通常分别取少量溶液B于两支试管中,进行如下实验:
步骤一:检验Mg2+,向其中一支试管中加入________溶液(填化学式),看是否有沉淀生成。
步骤二:检验Ca2+,向另一支试管中加入某溶液,看是否有沉淀生成。下列三种溶液,其沉淀效果最好的是________。
A.0.1mol·L-1 Na2CO3溶液
B.0.1mol·L-1 Na2SO3溶液
C.0.1mol·L-1 Na2C2O4溶液
(3)在除杂过程中,向粗盐悬浊液中加混合液A时需控制溶液pH=12以确保Mg2+除尽,根据提供的数据计算,溶液B中Mg2+物质的量浓度将被控制在________________以下。
(4)对溶液B加热并不断滴加6mol·L-1的盐酸,同时用pH试纸检测溶液,直至pH=2时停止加盐酸,得到溶液C。该操作的目的是__________________________________________________。
(5)溶液C倒入蒸发皿中,加热蒸发并用玻璃棒不断搅拌,直到有大量固体析出时停止加热。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
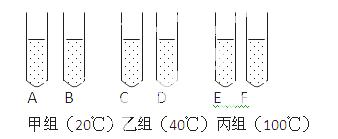
将某种玉米子粒浸种发芽后研磨匀浆、过滤,得到提取液。取6支试管分别加入等量的淀粉溶液后,分为3组并分别调整到不同温度,如图所示,然后在每支试管中加入等量的玉米子粒提取液,保持各组温度30分钟后,继续进行实验(提取液中还原性物质忽略不计):若向 A、C、E三支试管中分别加入适量的新制氢氧化铜,沸水浴一段时间,观察该三支试管。
A、C、E三支试管中分别加入适量的新制氢氧化铜,沸水浴一段时间,观察该三支试管。
(1)液体颜色呈砖红色的试管是
A.A和C B.A和E C.C和E D.A、C和E
(2)有一支砖红色较深的试管是
A. A B.C C.E D.不能确定
A B.C C.E D.不能确定
(3)液体颜色不呈砖红色的原因是
A.淀粉酶在40℃时活性相对较高
B.淀粉酶催化淀粉水解产生的无还原糖
C.淀粉酶与新制氢氧化铜反应
D.淀粉酶在100℃时失活
(4) 若向B、D、F三支试管中分别加入等量的碘液,观察三支试管,发现液体的颜色是蓝色,产生该颜色的原因是
若向B、D、F三支试管中分别加入等量的碘液,观察三支试管,发现液体的颜色是蓝色,产生该颜色的原因是
A.淀粉完全水解 B.淀粉部分水解
C.淀粉未能水解 D.淀粉酶与碘反应
查看答案和解析>>
科目:高中化学 来源: 题型:
PVDC是聚偏二氯乙烯的英文缩写,可作为保鲜食品的包装材料,它的结构简式为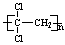 。下列说法中错误的是
。下列说法中错误的是
A.PVDC由单体CCl2=CH2发生加聚反应合成
B.PVDC由单体CCl3CH3发生缩聚反应合成
C.PVDC有很大缺点,如在空气中熔融可分解出HCl等,会污染空气
D.PVDC的单体可发生加成、取代、氧化、消去等反应
查看答案和解析>>
科目:高中化学 来源: 题型:
等物质的量下列各状态的电解质,自由离子数由大到小的排列顺序是( )
①熔融的NaHSO4 ②NaHSO4溶液 ③NaHCO3溶液 ④H2CO3溶液
A.①②③④ B.④②③①
C.②③①④ D.②①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
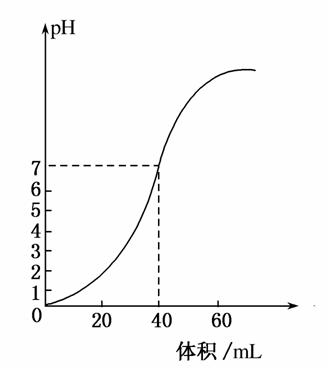
用1.0mol·L-1NaOH溶液中和某浓度硫酸溶液时,其pH和所加NaOH溶液的体积关系如图所示,原硫酸溶液的物质的量浓度和完全反应后溶液的总体积是( )
A.1mol·L-1,60mL
B.0.5mol·L-1,80mL
C.0.5mol·L-1,40mL
D.1mol·L-1,80mL
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:2CH2===CH2+O2 2CH3CHO。在下列反应中,其中有机反应物发生的反应类型与乙烯相同的是( )
2CH3CHO。在下列反应中,其中有机反应物发生的反应类型与乙烯相同的是( )
①乙醛转化为乙醇 ②苯酚置于空气中变红 ③乙醛的银镜反应 ④CH3CH2Br在NaOH醇溶液中加热 ⑤丙酮(CH3COCH3)与氢气生成2丙醇 ⑥甲苯使酸性高锰酸钾溶液褪色 ⑦乙酸乙酯碱性条件下水解
A.①⑤ B.①②⑥
C.②③⑥ D.除④⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值。下列叙述正确的是( )
A.标准状况下,22.4 L甲醇中含有的氧原子数为1.0 NA
B.室温下,28.0 g乙烯和丁烯的混合气体中含有的碳原子数目为2NA
C.标准状况下,2.24 L CO2与足量的Na2O2充分反应,转移电子总数为0.2 NA
D.25 ℃时,pH=1的1.0 LH2SO4溶液中含有H+的数目为0.2 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
弱电解质的电离平衡、盐类的水解平衡和难溶物的溶解平衡均属于化学平衡。
Ⅰ.已知H2A在水中存在以下平衡:H2A===H++HA-,HA-H++A2-。
(1)常温下NaHA溶液的pH________(填选项字母),原因是________。
A.大于7 B.小于7
C.等于7 D.无法确定
(2)某温度下,若向0.1 mol·L-1的NaHA溶液中逐滴滴加0.1 mol·L-1 KOH溶液至溶液呈中性(忽略混合后溶液的体积变化)。此时该混合溶液中的下列关系一定正确的是________。
A.c(H+)·c(OH-)= 1.0×10-14
1.0×10-14
B.c(Na+)+c(K+)=c(HA-)+2c(A2-)
C.c(Na+)>c(K+)
D.c(Na+)+c(K+)=0.05 mol·L-1
(3)已知常温下H2A的钙盐(CaA)的饱和溶液中存在以下平衡:CaA(s)Ca2+(aq)+A2-(aq) ΔH>0。若要使该溶液中Ca2+浓度变小,可采取的措施有________(填选项字母)。
A.升高温度 B.降低温度
C.加入NH4Cl晶体 D.加入Na2A固体
Ⅱ.含有Cr2O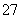 的废水毒性较大,某工厂废水中含5.0×10-3 mol·L-1的Cr2O
的废水毒性较大,某工厂废水中含5.0×10-3 mol·L-1的Cr2O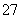 。为了使废
。为了使废 水的排放达标,进行如下处理:
水的排放达标,进行如下处理:
Cr2O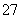
 Cr3+、Fe3+
Cr3+、Fe3+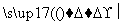 Cr(OH)3、Fe(OH)3
Cr(OH)3、Fe(OH)3
(1)该废水中加入绿矾和H+,发生反应的离子方程式为___________。
(2)若处理后的废水中残留的c(Fe3+)=2.0×10-13 mol·L-1,则残留的Cr3+的浓度为______________。(已知:Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cr(OH) 3]=6.0×10-31)
3]=6.0×10-31)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com