
【题目】 下列表述不正确的是( )
A.人造刚玉熔点很高,可用作高级耐火材料,主要成分是Al2O3
B.硅是制造太阳能电池的常用材料
C.四氧化三铁俗称铁红,可用于作油漆、红色涂料
D.分散系中分散质粒子的直径:Fe(OH)3 悬浊液>Fe(OH)3 胶体>FeCl3 溶液
科目:高中化学 来源: 题型:
【题目】已知羟基和Cl原子不能连在同一碳原子上,且羟基也不能连在双键碳原子上,则与钠反应能生成氢气的有机物C4H7ClO,其所有可能的同分异构体数目有( )
A. 9种 B. 12种 C. 15种 D. 20种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作中正确的是( )
A.蒸馏操作时,应向蒸馏液体中加入几块沸石,以防止暴沸
B.蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热
C.分液操作时,先将分液漏斗中下层液体从下口放出,再将上层液体从下口放出
D.萃取操作时,可以选用CCl4或酒精作为萃取剂从溴水中萃取溴
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由氢气和氧气反应生成1mol水蒸气放热241.8KJ,写出该反应的热化学方程式_______________________。若1g水蒸气转化成液态水时放热2.444KJ,则反应H2(g) + 1/2O2(g) == H2O(l)的△H=______________ kJ·![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向下列物质的水溶液中滴加稀硫酸或MgCl2溶液时,均有白色沉淀生成的是( )
A. BaCl2 B. Ba(OH)2 C. Na2CO3 D. KOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过渡金属钛、铬、铁、镍、铜等金属及其化合物在工业上有用途。
(1)钛铁合金具有放氢温度低、价格适中等优点,是钛系储氢合金的代表。
①Ti的基态原子价电子排布式为_________。
②Fe元素在周期表中的位置是_________。
(2)制备 CrO2Cl2的反应为 K2Cr2O7+3CCl4=2KCl+2 CrO2Cl2+3COCl2↑。
①上述化学方程式中非金属元素电负性由小到大的顺序________。(用元素符号表示)
②COCl2分子中所有原子均满足8电子构型,COCl2分子中π键和σ键的个数比为____,中心原子的杂化方式为_______。
(3)NiO、FeO的晶体结构均与NaCl的晶体结构相似,其中Ni2+和Fe2+的离子半径分別为6.9×10-2nm和7.8×10-2nm。则熔点:FeO_____(填“>”“<”或“=” )NiO。
(4)Ni和La的合金是目前使用广泛的储氢材料,具有大容量、高寿命、耐低温等特点,在中国已实现了产业化.该合金的晶胞结构如图所示。

①该晶体的化学式为__________。
②已知该晶胞的摩尔质量为Mg/mol,密度为dg/cm3。设NA为阿伏加徳罗常数的值,则该晶胞的体积是_______(用含M、d、NA的代数式表示)。
③该晶体的内部具有空隙,且每个晶胞的空隙中储存6个氢原子比较温定。
已知:a=511pm,c=397pm;标准状况下氢气的密度为8. 98×10-5g/cm3;
![]() 。若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为________。
。若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,CH4与H2O(g)发生反应:CH4(g)+H2O(g)![]() CO(g)+3H2(g),设起始
CO(g)+3H2(g),设起始![]() =Z,在恒压下,平衡时
=Z,在恒压下,平衡时![]() (CH4)的体积分数与Z和T(温度)的关系如图所示。下列说法正确的是( )
(CH4)的体积分数与Z和T(温度)的关系如图所示。下列说法正确的是( )
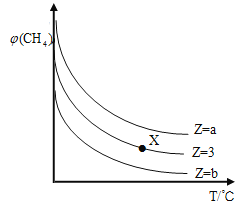
A.该反应的焓变△H﹤0
B.图中Z的大小为b >3> a
C.图中X点对应的平衡混合物中![]() =3
=3
D.温度不变时,图中X点对应的平衡在加压后![]() (CH4)减小
(CH4)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题: 
(1)从氯化钾溶液中得到氯化钾固体,选择装置(填代表装置图的字母,下同);除去自来水中的Cl﹣等杂质,选择装置 .
(2)从碘水中分离出I2 , 选择装置 , 该分离方法的名称为 .
(3)装置A中①的名称是 , 进水的方向是 .
(4)海水中蕴藏着丰富的资源,在实验室中取少量海水,进行如图流程的实验: 
问题1:粗盐中含Ca2+、Mg2+、Fe3+、SO42﹣等杂质,需要提纯后才能综合利用.
粗盐提纯的步骤有:
①加入过量的Na2CO3溶液; ②加入过量的BaCl2溶液; ③加入过量的NaOH溶液;
④调节溶液的pH等于7; ⑤溶解; ⑥过滤; ⑦蒸发.
正确的操作顺序是(填写序号字母).
a.⑤②③①⑥④⑦b.⑤①②③⑥④⑦c.⑤②①③④⑥⑦d.⑤③①②⑥④⑦
问题2:按所选顺序操作时,步骤④的离子方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:根据离子反应,碳酸根离子与钡离子产生碳酸钡沉淀,硫酸根离子与钡离子产生硫酸钡沉淀,而碳酸钡能与盐酸反应,硫酸钡不溶.
现取50.0mLNa2CO3和Na2SO4的混合溶液,加入过量BaCl2溶液后得到14.51g白色沉淀,用过量稀盐酸处理后沉淀量减少到4.66g,并有气体放出.试计算:
(1)所得白色沉淀中BaCO3的物质的量;
(2)原混合液中Na2CO3的物质的量浓度;
(3)产生的气体在标准状况下的体积.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com