
【题目】某工业残渣主要成分为Fe2O3(含有少量FeO、Cu、Mg等杂质)。某课外兴趣小组利用该残渣制取Fe2O3粉末的流程如下:(说明:流程中“向黄色溶液加入MgO”的目的是调节溶液的酸碱性,使Fe3+生成沉淀而Mg2+不沉淀。)
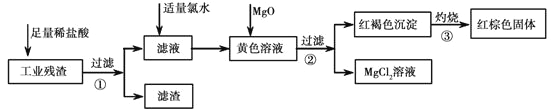
请回答下列问题:
(1)加入足量稀盐酸后,发生化学反应的类型有_____________(填写代号)。
A. 氧化还原反应 B.化合反应 C.分解反应 D.复分解反应
(2)加入适量氯水的作用是____________________________.
(3)写出灼烧红褐色沉淀时发生反应的化学方程式_____________________。实验室灼烧红褐色沉淀可选用的装置是__________(填序号)。

(4)若向黄色溶液中加入过滤①后的滤渣,发生反应的离子方程式为___________。
(5)检验黄色溶液中Fe3+是否完全沉淀的方法是:取过滤②后的少量滤液于试管中,____________。
【答案】 AD 将Fe2+氧化成Fe3+ 2Fe(OH)3 ![]() Fe2O3+3H2O d 2Fe3++Cu=2Fe2++Cu2+ 滴加KSCN溶液,若溶液变为血红色,说明Fe3+沉淀不完全;若溶液不变色,说明Fe3+沉淀完全
Fe2O3+3H2O d 2Fe3++Cu=2Fe2++Cu2+ 滴加KSCN溶液,若溶液变为血红色,说明Fe3+沉淀不完全;若溶液不变色,说明Fe3+沉淀完全
【解析】本题考查化学工艺流程,(1)工业残渣中加入盐酸,发生Fe2O3+6H+=2Fe3++3H2O、FeO+2H+=Fe2++H2O、Mg+2H+=Mg2++H2↑,Cu不与盐酸反应,发生的反应类型为置换反应(氧化还原反应)、复分解反应,故选项AD正确;(2)黄色溶液中加入MgO的目的是调节pH,使Fe3+生成沉淀,而Mg2+不沉淀,根据(1)发生反应,因此适量氯水的作用是将Fe2+氧化成Fe3+;(3)红褐色沉淀是Fe(OH)3,Fe(OH)3不稳定受热易分解,因此发生反应是:2Fe(OH)3 ![]() Fe2O3+3H2O;灼烧氢氧化铁沉淀,需要用到坩埚,即选项d正确;(4)黄色溶液含有主要离子是Fe3+、Mg2+、Cl-,操作①中滤渣为Cu,Cu能与Fe3+发生Cu+2Fe3+=2Fe2++Cu2+;(5)需要检验溶液中是否含有Fe3+,具体操作是取过滤②后的少量滤液于试管中,滴加KSCN溶液,若溶液变为血红色,说明Fe3+沉淀不完全;若溶液不变色,说明Fe3+沉淀完全。
Fe2O3+3H2O;灼烧氢氧化铁沉淀,需要用到坩埚,即选项d正确;(4)黄色溶液含有主要离子是Fe3+、Mg2+、Cl-,操作①中滤渣为Cu,Cu能与Fe3+发生Cu+2Fe3+=2Fe2++Cu2+;(5)需要检验溶液中是否含有Fe3+,具体操作是取过滤②后的少量滤液于试管中,滴加KSCN溶液,若溶液变为血红色,说明Fe3+沉淀不完全;若溶液不变色,说明Fe3+沉淀完全。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】常温下,pH=1的某溶液A中含有NH4+、K+、Na+、Fe3+、Al3+、Fe2+、CO32-、NO3-、Cl-、I-、SO42-中的4种,且溶液中各离子的物质的量浓度均为0.1mol/L,现取该溶液进行有关实验,实验结果如下图所示: 下列有关说法正确的是

A.该溶液中一定有上述离子中的NO3-、Al3+、SO42-、Cl-四种离子
B.实验消耗Cu 14.4g,则生成气体丁的体积为3.36L
C.沉淀乙一定有BaCO3,可能有BaSO4
D.一定没有Fe3+,但是无法确定是否含有I-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】①溴水 ②氯水 ③碘酒 ④氯化钾 ⑤酸性高锰酸钾溶液。能使湿润的淀粉KI试纸变蓝的是( )
A. ①②③ B. ①⑤ C. ①②③⑤ D. ③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生活处处有化学。下列说法正确的是( )
①食盐可作调味剂 ②鸡肉富含蛋白质 ③米饭的主要成分是葡萄糖 ④竹子属于天然高分子材料 ⑤橄榄油的主要成分是氨基酸
A.①②③B.①②④C.②③④D.②③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中,溶质的物质的量浓度为1moI/L的是
A. 将6.2gNa2O溶解于水,并配成200mL溶液
B. 1L含1mol K+的K2SO4溶液
C. 将22.4LHC1溶于1L水
D. 将40.0 g NaOH溶于1L水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 元素周期表中元素排序的依据是原子的核电荷数
B. 元素周期表有十六个纵列,也就是十六个族
C. 原子的最外层电子数相同的元素,一定属于同一族
D. 电子层数相同的粒子,对应元素一定属于同一周期
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出下列反应的离子方程式。
①钠和水反应____________________________________。
②硫酸铜溶液中滴加氢氧化钡溶液___________________________________。
(2)3.01×1023个OH-的物质的量为______mol,质量为_______g。
(3)将28g纯净的铁粉投入到200ml足量的稀盐酸中,该反应能够放出标准状况下的气体____L,实验后所得溶液中Fe2+的物质的量浓度为_________mol/L 。
(4)将200 mL 0.5 mol/LNaOH稀释成1000 mL后其物质的量浓度是_________mol/L 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com