
����Ŀ��
�����������ž�����ҵ�Ŀ��ٷ�չ�����������������Ȼ���IJ�����Ҳ��֮Ѹ����������ˣ����Ȼ���ת��Ϊ�����ļ�����Ϊ��ѧ�о����ȵ㡣�ش��������⣺
��1��Deacon������ֱ��������Ϊ��4HCl(g)+O2(g)=2Cl2(g)+2H2O(g)����ͼΪ���������У�����Ũ�ȱ�c(HCl) ��c(O2)�ֱ����1��1��4��1��7��1ʱHClƽ��ת�������¶ȱ仯�Ĺ�ϵ��
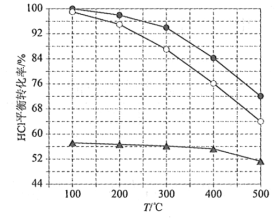
��֪��Ӧƽ�ⳣ��K��300�棩____________K��400�棩����������������С����������HCl��ʼŨ��Ϊc0�����ݽ���Ũ�ȱ�c(HCl)��c(O2)=1��1�����ݼ���K��400�棩=____________���г�����ʽ��������ѧ�����Ƚ��Ͽ��Ա��ַ�Ӧ���ת���ʣ�ͬʱ���Ͳ��������ܺġ�����Ũ�ȱ�c(HCl)��c(O2)���͡����ߵIJ���Ӱ��ֱ���____________��
��2��Deaconֱ���������ɰ����д����̽��У�
CuCl2(s)=CuCl(s)+![]() Cl2(g) ��H1=83 kJ��mol-1
Cl2(g) ��H1=83 kJ��mol-1
CuCl(s)+![]() O2(g)=CuO(s)+
O2(g)=CuO(s)+![]() Cl2(g) ��H2=-20 kJ��mol-1
Cl2(g) ��H2=-20 kJ��mol-1
CuO(s)+2HCl(g)=CuCl2(s)+H2O(g) ��H3=-121 kJ��mol-1
��4HCl(g)+O2(g)=2Cl2(g)+2H2O(g)����H=_________ kJ��mol-1��
��3����һ���¶ȵ������£���һ�����HCI��ת���ʵķ�����______________����д��2�֣�
��4���ڴ�ͳ�ĵ���Ȼ���������������Ļ����ϣ���ѧ���������̼���缫���������һ���µĹ��շ�������Ҫ�����绯ѧ���̺ͻ�ѧ���̣�����ͼ��ʾ��
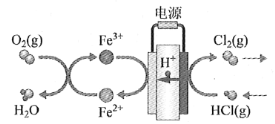
�����������ķ�Ӧ��____________________��д��Ӧ����ʽ������·��ת��1 mol���ӣ�����������__________L����״����
���𰸡����� ![]() O2��Cl2�����ܺĽϸߡ�HClת���ʽϵ� ��116 ���ӷ�Ӧ��ϵѹǿ����ʱ��ȥ���� Fe3++e=Fe2+��4Fe2++O2+4H+=4Fe3++2H2O 5.6
O2��Cl2�����ܺĽϸߡ�HClת���ʽϵ� ��116 ���ӷ�Ӧ��ϵѹǿ����ʱ��ȥ���� Fe3++e=Fe2+��4Fe2++O2+4H+=4Fe3++2H2O 5.6
��������
��1�����ݷ�Ӧ����ʽ֪��HClƽ��ת����Խ��ƽ�ⳣ��KԽ���ͼ��֪�����¶�ƽ��ת���ʽ��ͣ�˵�������¶�ƽ�����淴Ӧ������У���K(300��)>K(400��)��
��ͼ��֪��400��ʱ��HClƽ��ת����Ϊ84%��������ʽ�������ݽ��д����ã�
![]()
��ʼ��Ũ�ȣ� c0 c0 0 0
�仯��Ũ�ȣ� 0.84c0 0.21c0 0.42c0 0.42c0
ƽ�⣨Ũ�ȣ�(1-0.84)c0 (1-0.21)c0 0.42c0 0.42c0
��K=![]() �����������Ϣ֪������Ũ�ȱȹ��ͣ���������ʣ�࣬���·�������������������ܺĽϸߣ�����Ũ�ȱȹ��ߣ�HCl���ܳ�ַ�Ӧ������HClת���ʽϵͣ�
�����������Ϣ֪������Ũ�ȱȹ��ͣ���������ʣ�࣬���·�������������������ܺĽϸߣ�����Ũ�ȱȹ��ߣ�HCl���ܳ�ַ�Ӧ������HClת���ʽϵͣ�
��2�����ݸ�˹����֪������ӦI+��ӦII+��ӦIII����2��![]() H=��H1+H2+H3����2=-116kJ��mol-1��
H=��H1+H2+H3����2=-116kJ��mol-1��
��3���������HCl��ת���ʣ�Ӧ�ô�ʹƽ�������ƶ����÷�ӦΪ���������С�ķ�Ӧ��������������ԭ������������ѹǿ��ʹƽ�������ƶ���Ҳ���Լ�ʱ��ȥ�����С����Ũ�ȣ�ʹƽ�������ƶ���
��4���������У��������������Ϸ������ǵõ��ӷ�Ӧ��Ԫ�ػ��ϼ۽��ͣ����ڻ�ԭ��Ӧ����ͼ�����Ϊ������Ӧ������ͼʾ��Ϣ֪�缫��ӦΪ��Fe3++e����Fe2+��4Fe2++O2+4H+��4Fe3++2H2O����·��ת��1 mol���ӣ����ݵ��ӵ�ʧ�غ��֪���������������ʵ�����1mol��4��0.25mol���ڱ�״���µ����Ϊ0.25mol��22.4L/mol��5.6L��


 ��1����Ԫ�¿�������ĩϵ�д�
��1����Ԫ�¿�������ĩϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����״����VL�����ܽ���1Lˮ�У�ˮ���ܶȽ���Ϊlg/ml����������Һ���ܶ�Ϊ��g/ml����������ΪW������Ũ��Ϊcmol/L,�����й�ϵ�в���ȷ����
A. W= 17V/(17V+22400) B. W= 17c/(l000��)
C. ��= (17V+ 22400)/(22.4 + 22.4V) D. c=1000V��/(17V+22400)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȡ100mL��Na2CO3��Na2SO4�����Һ����������Ba(OH)2��Һ100 mL��ǡ����ȫ��Ӧ�����ˡ������õ�14.51g��ɫ��������Һ�����ù���ϡ���ᴦ�������������ٵ�4.66g����������ų������㣺
��1����ԭ���Һ��Na2SO4�����ʵ�����__________________
��2�������������ڱ�״���µ����Ϊ���٣�_________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������X��Y��Z����Է���������ϵΪMr(X)<Mr(Y)��0��5Mr(Z)������˵����ȷ����
A. ԭ����Ŀ��ȵ��������壬����������Z
B. ͬ��ͬѹ�£�ͬ�������������壬�����ܶ���С����X
C. ��һ�������£��������������Ϊ2��24 L�������ǵ����ʵ���һ����Ϊ0.1 mol
D. ͬ���£������ͬ���������ֱ��2 g Y�����1 g Z���壬����ѹǿ��Ϊ2�U1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڱ�״���£�ag����A��bg����B�ķ�������ͬ��������йص�����˵���в���ȷ����
A.����A������B��Ħ������֮��Ϊ![]()
B.��ͬ״���£�ͬ���������A������B������֮��Ϊ![]()
C.������ͬ������A������B�ķ�����֮��Ϊ![]()
D.ͬ��ͬѹ�£�����A������B���ܶ�֮��Ϊ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ij��84����Һ��ƿ�岿�ֱ�ǩ��ͼ��ʾ������84����Һ��ͨ��ϡ��100��(���֮��)��ʹ�á���ش��������⣺

��1������84����Һ�������ʵ���Ũ��Լ___mol��L��1(С�������һλ)��
��2��ijͬѧȡ100mL����84����Һ����ϡ�ͺ�����������ϡ�ͺ����Һ��c(Na+)=___mol��L��1��
��3����ͬѧ���ĸ���84����Һ�����䷽������NaClO��������480mL��NaClO��������Ϊ25%������Һ����Ҫ����NaClO���������Ϊ__g������Ϊ�����˵IJ���ʾ��ͼ������ȷ����Ϊ____��

��4�����ƹ��������и������������Һ���ʵ���Ũ���к�Ӱ�죨����ƫС������ƫ����������Ӱ������
A����������ƽ����NaClO����ʱ����������___��
B������ƿ������ˮϴ�Ӻ�δ���������������ˮ____��
C������ʱ����������ƿ�̶��߽��ж���____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) ��H= ��1025kJ/mol������Ӧ����ʼ���ʵ�����ͬ�����й��ڸ÷�Ӧ��ʾ��ͼ����ȷ����( )
4NO(g)+6H2O(g) ��H= ��1025kJ/mol������Ӧ����ʼ���ʵ�����ͬ�����й��ڸ÷�Ӧ��ʾ��ͼ����ȷ����( )
A.  B.
B. 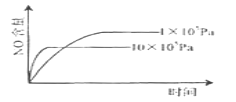
C.  D.
D. 
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��Fe2+�����軯�أ�K3[Fe(CN)6]���������������ɫ������AgI��������ˮ�Ļ�ɫ���塣��0.2mol��L-1��KI��Һ��0.05mol��L-1Fe2(SO4)3��Һ�������Ϻ�ȡ���Һ�ֱ��������ʵ�飬��˵����Һ�д��ڻ�ѧƽ�⡰2Fe3++2I-![]() 2Fe2++I2�����ǣ� ��
2Fe2++I2�����ǣ� ��
��� | ʵ����� | ʵ������ |
�� | ����KSCN��Һ | ��Һ���ɫ |
�� | ����AgNO3��Һ | ���ɻ�ɫ���� |
�� | ����K3[Fe��CN��6]��Һ | ������ɫ���� |
�� | ���������Һ | ��Һ����ɫ |
A.��B.�ں͢�C.�ۺ͢�D.��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±�����ͼ��ʾ��һЩ���ʻ�����Ĵ�����ϵ������ȷ����
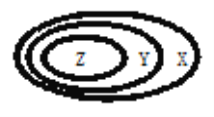
Z | Y | X | |
A | ������ | ������ | ������ |
B | �ǵ���� | ����� | ������ |
C | ���� | ��ɢϵ | ����� |
D | ���������� | ���������� | ������ |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com