
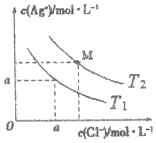
 已知AgCl在水中的溶解是吸热过程.不同温度下,AgCl在水中的沉淀溶解平衡曲线如图所示.己知T1温度下Ksp(AgCl)=1.6×10-9,下列说法正确的是( )
已知AgCl在水中的溶解是吸热过程.不同温度下,AgCl在水中的沉淀溶解平衡曲线如图所示.己知T1温度下Ksp(AgCl)=1.6×10-9,下列说法正确的是( )| A. | T1>T2 | |
| B. | a=4.0×10-5 | |
| C. | M点溶液温度变为T1时,溶液中Cl-的浓度不变 | |
| D. | T2时饱和AgCl溶液中,c(Ag+)、c(Cl-)可能分别为2.0×10-5mol/L、4.0×10-5mol/L |
分析 AgCl在水中的溶解是吸热过程,则升高温度,溶解平衡正向移动,则Ksp增大,T2时c(Ag+)、c(Cl-)大于T1温度下,说明T2时Ksp较大,则T1<T2,以此解答该题.
解答 解:A.AgCl在水中的溶解是吸热过程,升高温度Ksp增大,由图象可知T1<T2,故A错误;
B.T1温度下Ksp(AgCl)=1.6×10-9,可知a2=1.6×10-9,则a=4.0×10-5,故B正确;
C.M点溶液温度变为T1时,温度降低,Ksp减小,则溶液中Cl-的浓度减小,故C错误;
D.T2时Ksp(AgCl)>1.6×10-9,如c(Ag+)、c(Cl-)分别为2.0×10-5mol/L、4.0×10-5mol/L,则Qc=8×10-10,小于Ksp,故D错误.
故选B.
点评 本题考查难溶电解质的溶解平衡,为高频考点,把握Ksp的计算、溶解平衡移动、平衡状态为解答的关键,侧重分析与应用能力的考查,注意K的计算,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 64gCaC2中含有的共用电子对数为3NA | |
| B. | 常温常压下,1.8g甲基(-CD3)中含有的中子数为NA | |
| C. | 1.5mol的MnO2粉末与足量浓盐酸共热转移电子数目小于3NA | |
| D. | 1L0.01 mol•L-1CKA1(SO4)2溶液中含有的阳离子数为0.02NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纤维素是多糖,但不能作人类的营养物质 | |
| B. | 生理盐水就是物质的量浓度为0.9 mol/L的氯化钠水溶液 | |
| C. | 葡萄酒中可添加适量的二氧化硫起抗氧化、防腐和杀菌等作用 | |
| D. | “卤水点豆腐”就是胶体的聚沉,豆腐、豆腐脑就是凝聚的豆类蛋白质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金刚石>晶体硅>二氧化硅>碳化硅 | B. | HCHO<CH3OH | ||
| C. | MgO>CO2>H2O | D. | 金刚石>CsCl>NaCl>钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化还原反应的本质是电子的转移 | B. | 还原剂是在反应中得电子的物质 | ||
| C. | 还原剂在反应中发生还原反应 | D. | 置换反应不一定都是氧化还原反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com