
【题目】实验室常利用反应:NaNO2+NH4Cl![]() NaCl+N2↑+2H2O制取少量氮气,下列关于该反应的说法不正确的是
NaCl+N2↑+2H2O制取少量氮气,下列关于该反应的说法不正确的是
A.N2既是氧化产物,又是还原产物
B.NH4Cl中氮元素被还原
C.被氧化的氮原子与被还原的氮原子的物质的量之比为1:1
D.每生成1 mol N2时,转移电子为3 mol
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:
【题目】30 mL1 mol·L-1NaCl溶液和40 mL0.5 mol·L-1CaCl2溶液混合后,混合液中Cl-浓度为(假设溶液体积混合前后不变)( )
A.0.5 mol·L-1B.0.6 mol·L-1C.1.0 mol·L-1D.2 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空。
Ⅰ.现有下列10种物质:①熔融的氢氧化钠②蔗糖③盐酸④金属钠⑤硫酸⑥二氧化硫⑦硫粉⑧石膏![]() ⑨酒精溶液⑩液氨
⑨酒精溶液⑩液氨
(1)属于电解质的是_______________(填序号,下同)。
(2)属于非电解质的是_____________。
(3)上述状态下能导电的是__________。
Ⅱ.已知某“84消毒液”瓶体部分标签如图所示。请回答下列问题:
84消毒液
[有效成分]![]()
[规格]![]()
[质量分数]25%
[密度]![]()
(1)![]() 的物质的量浓度约为________
的物质的量浓度约为________![]() (保留两位有效数字)。
(保留两位有效数字)。
(2)某同学参阅该“84消毒液”的配方,欲用![]() 固体配制
固体配制![]() 含
含![]() 质量分数为25%的消毒液。下列说法正确的是___________(填字母)。
质量分数为25%的消毒液。下列说法正确的是___________(填字母)。
A.如图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器
![]()
![]()
![]()

![]()
B.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制
C.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低
D.需要称量![]() 固体的质量为
固体的质量为![]()
E.配制过程中,定容时俯视刻度线会使得溶液浓度偏大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将6.5 g Zn放入5 L 0.1mol/L 的盐酸中,待Zn完全反应后,试计算:
(1)6.5 g Zn的物质的量________。
(2)生成氢气的体积________。
(3)反应后剩余HCl的物质的量________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为一定量饱和Ca(OH)2溶液中通入CO2气体后,产生CaCO3白色沉淀的质量与通入的CO2体积之间的关系曲线。请回答:
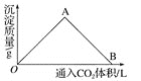
①OA段曲线所表示的化学反应方程式:_________,A点处已参加反应的CO2与Ca(OH)2的物质的量之比为________。
②B处溶液中存在的浓度较大的两种离子是________和________(填离子符号),将B处生成的溶液煮沸,可见到的现象是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A.1 mol/L的BaCl2溶液中含Cl-的数目为2NA
B.常温常压下,28 g N2中所含电子数目为10NA
C.标准状况下,4.48 L CH4中所含原子数目为NA
D.2 mol Al与足量盐酸完全反应,转移电子数目为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应2SO2(g)+O2(g) ![]() 2SO3(g) ΔH =a kJmol-1能量变化如图所示。下列说法中正确的是
2SO3(g) ΔH =a kJmol-1能量变化如图所示。下列说法中正确的是

A.a=E3-E1
B.逆反应的活化能大于a kJmol-1
C.过程②使用催化剂降低活化能,从而改变反应的焓变
D.将2molSO2(g)和1mol O2(g)置于一密闭容器中充分反应后放出的热量等于a kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所给信息和标志,判断下列说法错误的是( )
A | B | C | D |
碳酸氢钠药片
| 铜片制成的“纳米铜”在空气中易燃烧 |
| “绿蚁新醅酒,红泥小火炉”,“新醅酒”即新酿的酒 |
过量服用阿司匹林引起酸中毒后,可服用碳酸氢钠药片解毒 | 说明“钠米铜”的金属性比铜片强 | 看到有该标识的丢弃物,应远离并报警 | 在酿酒过程中,发生的反应有水解反应、氧化还原反应等 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示为钠硫高能电池的结构示意图,M由Na2O和Al2O3制得,该电池的工作温度为320℃左右,电池反应为2Na+xS=Na2Sx。下列说法不正确的是
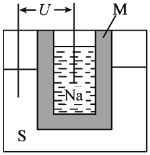
A. 负极反应式为Na - e- = Na+
B. 放电时,消耗32 g正极活性物质,转移的电子为2 mol
C. M的作用是导电和隔离钠与硫
D. 消耗相同质量的负极活性物质,钠硫电池的理论放电量是铅蓄电池的4.5倍
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com