
����Ŀ�������飨C8H10�����������ϵ��屽��ϩ��C8H8�����䷴Ӧԭ����C8H10��g��![]() C8H8��g����H2��g�� ��H����125kJ��mol��1��ij�¶��£���0.40mol�����飬����2L����ܱ������з�����Ӧ���ⶨ��ͬʱ������������ʵ������õ��������±���
C8H8��g����H2��g�� ��H����125kJ��mol��1��ij�¶��£���0.40mol�����飬����2L����ܱ������з�����Ӧ���ⶨ��ͬʱ������������ʵ������õ��������±���
ʱ�䣯min | 0 | 10 | 20 | 30 | 40 |
n��C8H10����mol | 0.40 | 0.30 | 0.26 | n2 | n3 |
n��C8H8����mol | 0.00 | 0.10 | n1 | 0.16 | 0.16 |
��1������Ӧ���е�20minʱ���ö�ʱ����H2��ƽ����Ӧ������________��
��2�����¶��£��÷�Ӧ�Ļ�ѧƽ�ⳣ����________��������λ��Ч���֣���
��3�������������������䣬��0.40mol H2��g����0.40mol C8H8��g���ϳ�C8H10��g��������30kJ�����ų�ʱ���÷�Ӧ��H2��ת������________��
���𰸡�0.0035mol��L��1��min��10.05360��
��������
��1����0.40mol�����飬����2L����ܱ������з�����Ӧ��20min��ʣ��0.26mol��������0.14mol����
C8H10��g��![]() C8H8��g����H2��g��
C8H8��g����H2��g��
��ʼ����mol�� 0.40 0 0
�仯����mol�� 0.14 0.14 0.14
20min�������mol�� 0.26 0.14 0.14
����Ũ����0.14mol��2L��0.07mol/L����v��H2����0.07mol/L��20min=0.0035mol/��Lmin����
��2�� C8H10��g��![]() C8H8��g����H2��g��
C8H8��g����H2��g��
��ʼ����mol�� 0.40 0 0
�仯����mol�� 0.16 0.16 0.16
ƽ������mol�� 0.24 0.16 0.16
��Ũ�ȷֱ���0.12mol/L��0.08mol/L��0.08mol/L����ѧƽ�ⳣ��K��c(C8H8)��c(H2)/c(C8H10)��0.08��0.08/0.12��0.053��
��3������C8H10��g��![]() C8H8��g����H2��g����H����125kJ��mol��1��֪C8H8��g��+H2��g��
C8H8��g����H2��g����H����125kJ��mol��1��֪C8H8��g��+H2��g��![]() C8H10��g����H=��125kJ��mol��1����30kJ�����ų�ʱ�����ĵ�H2��Ϊ
C8H10��g����H=��125kJ��mol��1����30kJ�����ų�ʱ�����ĵ�H2��Ϊ![]() ��0.24mol����������ת����Ϊ0.24mol/0.4mol��100%��60%��
��0.24mol����������ת����Ϊ0.24mol/0.4mol��100%��60%��


 ��ѧȫ��������ѵ��ϵ�д�
��ѧȫ��������ѵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����X��Y��Z��R���ֶ�����Ԫ�أ�Y��Z��Rͬ���ڡ������Ϣ���£�
�����Ϣ | |
X | ����Ϊ˫ԭ�ӷ��ӡ�����������Һ̬����������е�ϵͿ��Ȼ��X�ĵ��� |
Y | ��YԪ�ص�������ɫ��ӦΪ��ɫ |
Z | ͬ����Ԫ����ԭ�Ӱ뾶��С |
R | RԪ��ԭ�ӵ�������������K���������3�� |
(1)ZԪ�������ڱ���λ����_____��Y��Z��R�����ӵİ뾶�Ӵ�С��˳����__________(�����ӷ��ű�ʾ)��
(2)��X��Z����Ԫ����ɵĻ�����ף�������Ϊ�ӷ��ĵ���ɫҺ�壬���ӹ���Ϊ�����Σ��ҷ�����X��Z����ԭ���������ﵽ8�����ӵ��ȶ��ṹ������ˮ�������γ�һ�ֳ�����Ư�������ʡ���ĽṹʽΪ ___________��
(3)��������(Y2R)��Һ�ڿ����г��ڷ��ã���������Ӧ��������������ƵĽṹ�ͻ�ѧ�������Ƶ�����Y2R2������Һ�Ի�ɫ����Y2R2�ĵ���ʽΪ_______��д������Һ�ڿ����б��ʹ��̵Ļ�ѧ����ʽ___________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС��̽��NO��Na2O2�ķ�Ӧ�����������ͼ��ʾʵ��װ�ã�����EΪʵ��ǰѹ������ҡ�
���ϣ���dz��ɫ��AgNO2������ˮ�⣬�����������ξ�������ˮ��
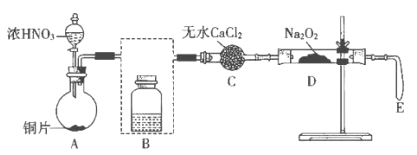
��1��д��A�з�Ӧ�Ļ�ѧ����ʽ��____________________________��
��2����װ��B�����������������Լ�_____________��
��3������ˮCaCl2��ȥˮ������Ŀ����_____________________________��
��4����Ӧһ��ʱ���D�������ֵĸо������й����ɵ���ɫ��Ϊ��ɫ��ֱ����ɫ���ٱ仯ʱ������Eʼ��û�����Թ���
��ѧ�����ݷ�Ӧ�����������ԭ��Ӧ�����ƶϹ������ΪNaNO2��д���÷�Ӧ�Ļ�ѧ����ʽ��_________________________________��
�����ʵ��֤����NaNO2���ɣ�ʵ�鷽����___________________________����д������������ͽ��ۣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ѭ�����̿�����ͼ��ʾ������˵����ȷ����(��֪����Ӧ�ܵ����ӷ���ʽΪ4NH4+ + 5O2![]() 2NO2- + 6H+ + N2O + 5H2O)
2NO2- + 6H+ + N2O + 5H2O)

A. �٢ھ����ڹ̵���Ӧ
B. �����еķ���������һ����Ҫ�����μ�
C. ��Ӧ����ÿ����1 mol H2Oת��2 mol e-
D. �����ŷź�NO3-�ķ�ˮ����Ӱ�캣���е���ѭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NaOH+HCl = NaCl+H2O����10gNaOH��ȫ��Ӧ�����ɵ�ˮ������Ϊ
A. 4g B. 4.5g C. 5g D. 5.5g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����4 mol A�����2 mol B������2 L���ܱ������л�ϣ�����һ�������·������·�Ӧ��A(g)+B(g)![]() 2C(g)����Ӧ2 s����C�����ʵ���Ϊ1.2 mol������˵����ȷ����
2C(g)����Ӧ2 s����C�����ʵ���Ϊ1.2 mol������˵����ȷ����
A. ������A��ʾ2 s�ڵ�ƽ����Ӧ����Ϊ0.3 mol��L-1��s-1
B. ������B��ʾ2 s�ڵ�ƽ����Ӧ����Ϊ0.6 mol��L-1��s-1
C. ��λʱ������a molA���ɣ�ͬʱ����2a molC����
D. ��A��B��C��ʾ�ķ�Ӧ����֮��Ϊ1��1��2ʱ�ﵽƽ��״̬
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Խ��Խ�����ӣ�ij��������Ϊ���ٻ�����Ⱦ�������Դ�������ʡ����ѳ����ȼ���״���������������������Ҫ�����������£���FeTiO3��TiΪ+4�ۣ�

����������ȷ����
A. ��������ֻ��������������Ȼ����漰������ԭ��Ӧ
B. ���Ȼ���ʱÿ����36g��̿����ת��7mol����
C. ���ϳɡ���Ӧ���������뻹ԭ�������ʵ���֮��Ϊ1��1
D. ������������Mg��Ar��������Mg��CO2������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������(�Ҷ���)��������Ȼ���ֲ���У���������κͼ���������ˮ���������������ˮ�����ᾧ��(H2C2O4��2H2O)��ɫ���۵�Ϊ101�棬������ˮ����������ˮ��������175��ʱ�ֽ⡣
��.�������������Ʊ����ᾧ�岢�ⶨ�䴿�ȣ��Ʊ�װ����ͼ��ʾ(���ȡ��̶���װ����ȥ)��
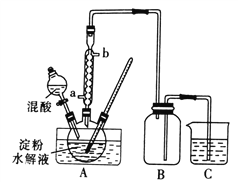
ʵ�鲽������
���ǻ����Ƚ�����ˮ��Ϊ�����ǣ�
���������ڵ���ˮ��Һ�м������(����֮��Ϊ3��2��65%HNO3��98%HSO4�Ļ����)����55~60����ˮԡ���ȷ�����Ӧ��
�۽ᾧ�������������Ӧ����Һ����ȴ����ѹ���ˣ����ò��ᾧ��ֲ�Ʒ��
��1��װ�������������Ϊ________���������,ˮԡ���ȵ��ŵ�Ϊ__________��
��2������������ʱ��������Ҫ��Ӧ���£�������л�ѧ����ʽ��
___C6H12O6+___HNO3 ![]() ___H2C2O4+9NO2��+3NO��+ ______
___H2C2O4+9NO2��+3NO��+ ______
��3����ȡmg���ᾧ��ֲ�Ʒ�����100mL��Һ��ȡ20.00mL����ƿ�У���amoL��L-1KMnO4��Һ�궨��ֻ����
5H2C2O4+2MnO4-+6H+=2Mn2++10CO2��+8H2O��Ӧ������KMnO4��Һ���ΪVmL�������ò��ᾧ��(H2C2O4��2H2O)�Ĵ���Ϊ___________��
��.֤�����ᾧ��ֽ�õ��IJ���
��4����ͬѧѡ������װ����֤����CO2��װ��B����Ҫ������__________��
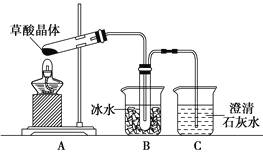
��5����ͬѧ��Ϊ���ᾧ��ֽ�IJ����г���CO2��H2OӦ�û���CO��Ϊ������֤��ѡ�ü�ͬѧʵ���е�װ��A��B����ͼ��ʾ�IJ���װ�ã������ظ�ѡ�ã�����ʵ�顣
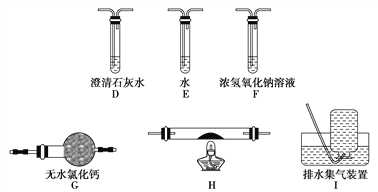
����ͬѧ��ʵ��װ���У��������ӵĺ���˳��ΪA��B��_____________������װ��H��Ӧ����ʢ�е�������________________________��
����֤�����ᾧ��ֽ��������CO��������_____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���״���һ������ȼ�ϣ��ڹ�ҵ�ϳ���CO��H2�ϳɼ״�����Ӧ����ʽΪCO(g)+2H2(g) ![]() CH3OH(g)��
CH3OH(g)��
��֪��
��CO(g)��1/2O2(g)��CO2(g) ��H1����283.0kJ/mol
��H2(g)��1/2O2(g)��H2O(g) ��H2����241.8kJ/mol
��CH3OH(g)��3/2O2(g)��CO2(g)��2H2O(g) ��H3����192.2kJ/mol
�ش��������⣺
��1������CO(g)+2H2(g) ![]() CH3OH(g)�ķ�Ӧ�ȡ�H4=________________��
CH3OH(g)�ķ�Ӧ�ȡ�H4=________________��
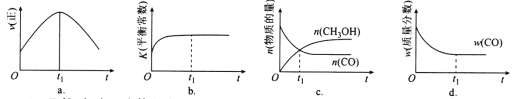
��2�����ھ��ȡ����ݵ��ܱ������г���1 mol CO��2 mol H2������CO(g)+2H2(g) ![]() CH3OH(g)��Ӧ������ʾ��ͼ��ȷ����˵����Ӧ�ڽ��е�t1ʱ��Ϊƽ��״̬����________(��ѡ����ĸ)��
CH3OH(g)��Ӧ������ʾ��ͼ��ȷ����˵����Ӧ�ڽ��е�t1ʱ��Ϊƽ��״̬����________(��ѡ����ĸ)��
��3��T1��ʱ����һ�����Ϊ5 L�ĺ��������г���1 mol CO��2 mol H2������5 min�ﵽƽ�⣬CO��ת����Ϊ0.8����5 min����H2��ʾ�ķ�Ӧ����Ϊv(H2)=_______________________��T1��ʱ������һ���������ܱ�������Ҳ����1 mol CO��2 mol H2���ﵽƽ��ʱCO��ת����Ϊ0.7��������������______5 L(�>����<����=��)��T1��ʱ��CO(g)+2H2(g) ![]() CH3OH(g)��ƽ�ⳣ��K=____________________________��
CH3OH(g)��ƽ�ⳣ��K=____________________________��
��4��Ϊ�����ȼ�ϵ������ʿ��Խ��״����Ϊȼ�ϵ�أ�д��KOH���������Һʱ���״�ȼ�ϵ�صĸ�����Ӧʽ��_________________________���õ�ظ�����ˮ�����բ����ʱ�����Ա�����բ������ʴ�����ֵ绯ѧ������������___________��
��5�����м״��ķ�ˮ�����ŷŻ����ˮ��Ⱦ������ClO2��������ΪCO2��Ȼ���ټӼ��кͼ��ɡ�д�������״����Է�ˮ�����У�ClO2��״���Ӧ�����ӷ���ʽ��_________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com