
【题目】二氧化氯(ClO2)是一种优良的消毒剂,熔点为-59℃,沸点为 11℃,浓度过高时易发生分解,甚至爆炸。某课外兴趣小组通过氯气与 NaClO2溶液反应来制取少量ClO2,装置如下图所示:
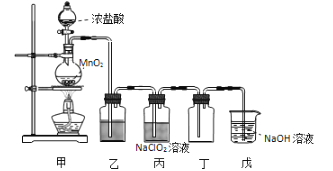
(1)甲装置中圆底烧瓶内发生反应的化学方程式是____________________。
(2)丙装置中发生的反应可能经两步完成,请将其补充完整:
①____________________________________________(用化学方程式表示),
②HClO + HCl + 2NaClO2 2ClO2↑+ 2NaCl + H2O。
(3)Clˉ存在时会催化 ClO2的生成,若无乙装置,则丙装置内产生 ClO2的速率明显加快。乙装置中试剂瓶内的液体是__________。实验过程中常需通入适量的 N2稀释 ClO2,其目的是_______________________。
(4)戊装置烧杯中 NaOH 溶液吸收 ClO2后,生成了 ClO2-、ClO3-,该反应的离子方程式是__________。
【答案】MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O Cl2+H2O
MnCl2+Cl2↑+2H2O Cl2+H2O![]() HCl+HClO 饱和食盐水 防止ClO2 发生分解,甚至爆炸 2ClO2+2OH-= ClO2- +ClO3- +H2O
HCl+HClO 饱和食盐水 防止ClO2 发生分解,甚至爆炸 2ClO2+2OH-= ClO2- +ClO3- +H2O
【解析】
(1)甲装置中是MnO2和HCl(浓)反应制氯气的。
(2)丙装置中氯气先和水反应,反应的化学方程式为Cl2+H2O![]() HCl+HClO。
HCl+HClO。
(3)从甲装置中出来的氯气中混有氯化氢,氯气在饱和食盐水中不溶,氯化氢溶解在水中。
(4)根据元素守恒和电荷守恒配平离子方程式。
(1)甲装置中是MnO2和HCl(浓)反应制氯气的,圆底烧瓶内发生反应的化学方程式是:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,故答案为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,故答案为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。
(2)丙装置中氯气先和水反应,反应的化学方程式为Cl2+H2O![]() HCl+HClO,故答案为:Cl2+H2O
HCl+HClO,故答案为:Cl2+H2O![]() HCl+HClO。
HCl+HClO。
(3)从甲装置中出来的氯气中混有氯化氢,氯气在饱和食盐水中不溶,氯化氢溶解在水中,故乙装置中试剂瓶内的液体是饱和食盐水,通入适量的 N2稀释 ClO2,其目的是防止ClO2 发生分解,甚至爆炸,故答案为:饱和食盐水;防止ClO2 发生分解,甚至爆炸。
(4)戊装置烧杯中NaOH溶液吸收 ClO2后,生成了 ClO2-、ClO3-,根据元素守恒可知产物还有水生成,再根据电荷守恒可得出该反应的离子方程式是:2ClO2+2OH-= ClO2- +ClO3- +H2O,故答案为:2ClO2+2OH-= ClO2- +ClO3- +H2O。


 名师点拨卷系列答案
名师点拨卷系列答案科目:高中化学 来源: 题型:
【题目】等质量的甲、乙、丙三种金属,分别与足量的溶质质量分数相同的稀硫酸完全反应后,都生成+2价的硫酸盐,其产生氢气的体积与反应时间的关系如图所示,则下列说法正确的是
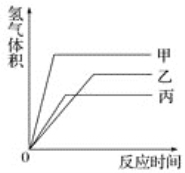
A. 三种金属的活动性顺序为甲>乙>丙
B. 反应结束消耗硫酸的质量一定相同
C. 三种金属的相对原子质量是甲>乙>丙
D. 甲先反应完,乙最后反应完
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)如图为CO2分子晶体结构的一部分,观察图形。试说明每个 CO2分子周围有________个与之紧邻且等距的 CO2分子;该结构单元平均占有________个CO2分子。

(2)在40 GPa高压下,用激光器加热到1800 K时,人们成功制得原子晶体干冰,其结构和性质与SiO2原子晶体相似,下列说法正确的是________。
A.原子晶体干冰易升华,可用作制冷剂
B.原子晶体干冰有很高的熔点和沸点
C.原子晶体干冰的硬度小,不能用作耐磨材料
D.原子晶体干冰在一定条件下可与氢氧化钠反应
E.每摩尔原子晶体干冰中含有4 mol C—O键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求进行填空:
(1)6.20 g Na2O 晶体中含 Na+的物质的量是 _________________。
(2)等质量的 NH3 和 H2S 中,氢原子的个数比是______________________。
(3) 铁与水蒸气反应的化学方程式_______________________________________。
(4) 向少量氯化铝溶液中加入足量氢氧化钠的离子方程式________________________。
(5)人通过呼吸作用吸入氧气,氧化体内的葡萄糖(C6H12O6)提供能量以维持生命活动,反应式为:C6H12O6+6O26CO2+6H2O+能量,该反应中的还原剂是______,若在该反应中消耗氧化剂的体积在标准状况下为4.48L,则反应中转移电子的物质的量为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常通过高温分解FeSO4的方法制备Fe2O3,其化学方程式为:2FeSO4![]() Fe2O3+SO2↑+SO3↑为检验FeSO4高温分解的产物,进行如下实验
Fe2O3+SO2↑+SO3↑为检验FeSO4高温分解的产物,进行如下实验
(1)检验产物Fe2O3取少量FeSO4高温分解得到的固体,加入一定量__________溶解,再向该溶液中加入适量的__________溶液,如有____________现象产生,则证明产物中存在Fe2O3
(2)检验气体产物:将FeSO4高温分解产生的气体通入下图三个装置中,以检验产生的气体中是否含有SO2、SO3。
①三个装量的连接序为_______________(填装置序号)
②实验中如观察到装置A中品红溶液______,装置B BaCl2溶液中__________,则可证明FeSO4高温分解产生的气体中含有SO2、SO3。
③装置C中NaOH溶液的作用是_______________(用离子方程式表示〕。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应:2NO2![]() 2NO+O2在体积固定的密闭容器中进行,达到平衡状态的标志是
2NO+O2在体积固定的密闭容器中进行,达到平衡状态的标志是
①单位时间内生成nmolO2的同时消耗2nmolNO2
②单位时间内生成nmolO2的同时消耗2nmolNO
③用NO2、NO、O2表示的反应速率之比为2∶2∶1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的压强不再改变的状态
⑦混合气体的平均相对分子质量不再改变的状态
A. ②④⑥⑦ B. ②③⑤⑦ C. ①③④⑤ D. 全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于分散系的说法中正确的是( )
A.不能发生丁达尔效应的分散系有氯化钠溶液、水等
B.可吸入颗粒(例如硅酸盐粉尘)形成气溶胶,对人类健康的危害更大
C.胶体的分散质粒子的直径为1~10 nm
D.氯化铁溶液与氢氧化铁胶体的本质区别是有无丁达尔效应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.摩尔是国际单位制中七个基本物理量之一
B.常温常压下,11.2LCO2所含分子数为0.5NA
C.H2SO4 的摩尔质量为98 g
D.6.02×1022个H2SO4分子的质量为9.8 g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com