
某有机物的结构简式如下图所示,则下列有关说法正确的是

A.该有机物可以发生氧化、加成、加聚、取代等反应
B.该有机物能与NaOH溶液反应,则1mol该有机物能消耗2molNaOH
C.该有机物的分子式为C12H14O5,且与C11H12O5 一定互为同系物
D.该有机物分子中所有碳原子不可能都在同一平面上
 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:
M和N两溶液分别含有下列十二种离子中的五种和七种离子:K+、Na+、H+、
NH4+、Fe3+、 A13+、Cl-、OH-、NO3-、S2-、CO32-、SO42-。己知两溶液所含离子各不相同,M溶液里的阳离子只有两种,则N溶液里的阴离子应该是( )
A.OH-、CO32-、SO42- B.S2-、Cl-、SO42-
C.CO32-、NO3-、S2- D.Cl-、SO42-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
有a、b、c、d四种金属。将a与b连接起来,浸入电解质溶液中,b不易腐蚀。将a、d分别投入等浓度的盐酸中,d比a反应强烈。将铜浸入b的盐溶液里,无明显变化。如果把铜浸入c的盐溶液里,有金属c析出。据此判断它们的活动性顺序由强到弱的为( )
A.a > c > d > b B.d > a > b > c
C.d > b > a > c D.b > a > d > c
查看答案和解析>>
科目:高中化学 来源: 题型:
化合物A、B是中学常见的物质,其阴阳离子可从下表中选择
| 阳离子 | Na+ Fe2+ Ba2+ NH4+ |
| 阴离子 | OHˉ NO3ˉ Iˉ HSO4ˉ |
(1)若A、B的水溶液均为无色,B的水溶液呈碱性,且混合后只产生不溶于稀硝酸的白色沉淀及能使红色石蕊试纸变蓝的气体。
①B的化学式为 ;
②A、B溶液混合后加热呈中性反应的离子方程式为
(2)若A的水溶液呈浅绿色,B的水溶液无色且其焰色反应为黄色。向A的水溶液中加入稀盐酸无明显现象,再加入B后溶液变黄,但A、B的水溶液混合亦无明显变化。则①A为 ;
②经分析上述过程中溶液变黄的原因可能是有两种:
Ⅰ Ⅱ ;
③请用一简易方法证明上述溶液变黄的原因 ;
④利用溶液变黄原理,将其设计成原电池,若电子由a流向b,则b极的电极反应式
为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
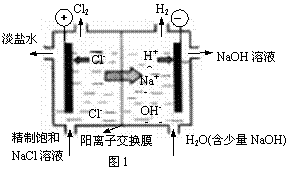
Ⅰ.氯碱工业中常用离子交换膜法电解制碱(如图1所示)。
(1)写出图1中阴极的电极反应式 。
 (2)已知阳离子交换膜只允许阳离子通过,阴离子交换膜只允许阴离子通过。工业上若用图2装置电解饱和Na2SO4溶液来生产纯净的NaOH和H2SO4,则该装置最主要的缺陷是 。
(2)已知阳离子交换膜只允许阳离子通过,阴离子交换膜只允许阴离子通过。工业上若用图2装置电解饱和Na2SO4溶液来生产纯净的NaOH和H2SO4,则该装置最主要的缺陷是 。

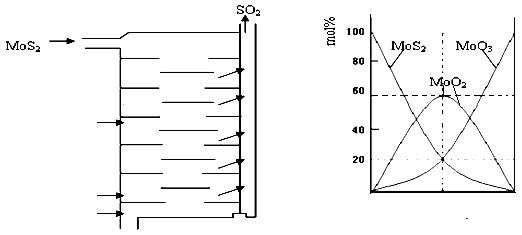
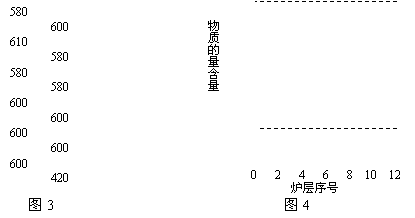
Ⅱ.辉钼矿(MoS2)是一种重要的矿物。图3是辉钼矿多层焙烧炉的示意图,其中1,2,3,…是炉层编号。580,600,610,…是各炉层的温度(℃)。图4给出了各炉层固体物料的物质的量百分含量。
|
 | |||
 | |||
(1)验证辉钼矿焙烧生成的气体是SO2而不是SO3的方法是 。
(2)辉钼矿焙烧生成的气体能使硫酸酸化的KMnO4溶液褪色,用化学方程式表示褪色的原因 。
(3)第6炉层存在的固体物质分别是MoS2、MoO3、MoO2,则它们的物质的量之比为 。
(4)图4表明,中间炉层(4~6)可能存在一种“固体+固体→固体+…”的反应,请写出该反应的热化学反应方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
PH=2的A、B两种酸溶液各1ml,分别加水稀释到1000ml,其溶液的PH与溶液体积﹝V﹞的关系如右图所示,则下列说法正确的是
A.A、B两种酸溶液的物质的量浓度一定相等
B.稀释后A酸溶液的酸性比B酸溶液的强
C.a=5 时,A是弱酸,B是强酸
D.若A、B都是弱酸,则5>a >2
 |
查看答案和解析>>
科目:高中化学 来源: 题型:
电子层数相同的三种元素X、Y、Z,它们最高价氧化物对应水化物的酸性由强到弱顺序
为:HXO4>H2YO4>H3ZO4,下列判断错误的是
A.原子半径 X>Y>Z B.气态氢化物稳定性X>Y>Z
C.元素原子得电子能力X>Y>Z D.单质与氢气反应难易X>Y>Z
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com