
【题目】由几种离子化合物组成的混合物,含有以下离子中的若干种:K+、Cl﹣、NH4+、Mg2+、CO32﹣、Ba2+、SO42﹣ . 将该混合物溶于水后得澄清溶液,现取3份100mL该溶液分别进行如下实验:
实验序号 | 实验内容 | 实验结果 |
1 | 加AgNO3溶液 | 有白色沉淀生成 |
2 | 加足量NaOH溶液并加热 | 收集到气体1.12L(已折算成标准状况下的体积) |
3 | 加足量BaCl2溶液,反应后进行( )、( )、干燥、称量;再向沉淀中加足量稀盐酸,然后干燥、称量 | 第一次称量读数为6.27g,第二次称量读数为2.33g |
试回答下列问题:
(1)根据实验1~3判断混合物中一定不存在的离子是;
(2)写出实验3中的空格处的实验操作;
(3)根据实验对Cl﹣是否存在的判断是(填“一定存在”、“一定不存在”或“不能确定”);
(4)溶液中K+是否存在?(填“一定存在”、“一定不存在”或“不能确定”);若“一定存在”,则K+物质的量浓度的范围(若“一定不存在”或“不能确定”不填此空).
【答案】
(1)Mg2+、Ba2+
(2)过滤、洗涤
(3)不能确定
(4)一定存在;>0.1 mol?L﹣1
【解析】解:(1)碳酸银、硫酸银、氯化银都是白色沉淀,因此实验1得到沉淀无法确定是氯化银,故实验1对Cl﹣是否存在的判断是:不能确定;利用实验2可知含有铵离子,利用实验3可知沉淀一定是碳酸钡和硫酸钡,即溶液中一定含有CO32﹣、SO42﹣ , 碳酸钡、碳酸镁、硫酸钡等都是不溶于水的沉淀,故可判知溶液一定不存在的离子是:Ba2+、Mg2+ , 所以答案是:Ba2+、Mg2+;(2)加足量BaCl2 溶液,对所得沉淀进行过滤、洗涤、干燥、称量,得到的4.66是碳酸钡和硫酸钡,再向沉淀中加足量稀盐酸,然后干燥、称量,得到的是硫酸钡,所以答案是:过滤、洗涤;(3)结合(1)(2)中分析可知溶液中一定含有的阴离子为CO32﹣、SO42﹣ , 由碳酸钡可溶于盐酸,硫酸钡不溶于盐酸可推知加入盐酸后剩余2.33g固体为BaSO4 , 利用硫守恒可知溶液中n(SO42﹣)= ![]() =0.01mol,c(SO42﹣)=
=0.01mol,c(SO42﹣)= ![]() =0.1mol/L;6.27g固体中碳酸钡的质量为6.27g﹣2.33g=3.94g,利用碳守恒可知溶液中n(CO32﹣)=
=0.1mol/L;6.27g固体中碳酸钡的质量为6.27g﹣2.33g=3.94g,利用碳守恒可知溶液中n(CO32﹣)= ![]() =0.02mol,c(CO32﹣)=
=0.02mol,c(CO32﹣)= ![]() =0.2mol/L,溶液中肯定存在的离子是NH4+、CO32﹣和SO42﹣ , 经计算,NH4+的物质的量为
=0.2mol/L,溶液中肯定存在的离子是NH4+、CO32﹣和SO42﹣ , 经计算,NH4+的物质的量为 ![]() =0.05 mol,利用(2)中分析、计算可知CO32﹣、SO42﹣的物质的量分别为0.02 mol和0.01 mol,根据电荷守恒,n(正电荷)=n(NH4+)=0.05mol,n(负电荷)=2n(CO32﹣)+2n(SO42﹣)=0.06mol,钾离子一定存在,氯离子无法判断是否存在,所以答案是:不能确定;(4)溶液中肯定存在的离子是NH4+、CO32﹣和SO42﹣ , 经计算,NH4+的物质的量为
=0.05 mol,利用(2)中分析、计算可知CO32﹣、SO42﹣的物质的量分别为0.02 mol和0.01 mol,根据电荷守恒,n(正电荷)=n(NH4+)=0.05mol,n(负电荷)=2n(CO32﹣)+2n(SO42﹣)=0.06mol,钾离子一定存在,氯离子无法判断是否存在,所以答案是:不能确定;(4)溶液中肯定存在的离子是NH4+、CO32﹣和SO42﹣ , 经计算,NH4+的物质的量为 ![]() =0.05 mol,利用(2)中分析、计算可知CO32﹣、SO42﹣的物质的量分别为0.02 mol和0.01 mol,根据电荷守恒,n(正电荷)=n(NH4+)=0.05mol,n(负电荷)=2n(CO32﹣)+2n(SO42﹣)=0.06mol,钾离子一定存在,最小浓度是0.1 molL﹣1 , 所以答案是:一定存在;>0.1 molL﹣1 .
=0.05 mol,利用(2)中分析、计算可知CO32﹣、SO42﹣的物质的量分别为0.02 mol和0.01 mol,根据电荷守恒,n(正电荷)=n(NH4+)=0.05mol,n(负电荷)=2n(CO32﹣)+2n(SO42﹣)=0.06mol,钾离子一定存在,最小浓度是0.1 molL﹣1 , 所以答案是:一定存在;>0.1 molL﹣1 .


科目:高中化学 来源: 题型:
【题目】已知氯化亚铁的熔点674℃、沸点1023℃;三氯化铁在300℃以上易升华,易溶于水并且有强烈的吸水性.在500℃条件下氯化亚铁与氧气可能发生多种反应,反应之一为:12FeCl2+3O2 ![]() 2Fe2O3+8FeCl3 . 某研究小组选用以下装置(夹持装置省略,装置可重复选用)进行反应的探究.回答下列问题:
2Fe2O3+8FeCl3 . 某研究小组选用以下装置(夹持装置省略,装置可重复选用)进行反应的探究.回答下列问题: 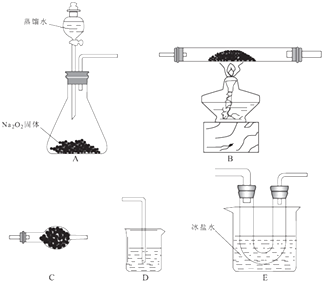
(1)装置的合理连接顺序为A、、D,其中E装置U形管左边设计为粗导管的目的是 .
(2)A装置中发生反应的化学方程式为 .
(3)反应过程发现,装置B中除生成红棕色固体外,还观察到黄绿色气体,生成该气体的化学方程式为 .
(4)待B中充分反应后,停止加热后,还需持续通氧气至 .
(5)设计实验: ①利用E装置U形管里的固体验证Fe(OH)3是弱碱: .
②测定装置B的残留固体中铁元素的质量分数: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】掌握仪器的名称、组装及使用方法是中学化学实验的基础,下图为两套实验装置。
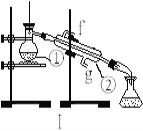
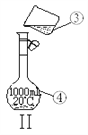
(1)写出下列仪器的名称:①__________;②_________ 。
(2)若利用装置I制取蒸馏水,将仪器补充完整后进行实验,冷却水从____________口进。(填g或f)
(3)现需配制250 mL 0.2 mol·L—1 NaCl溶液,其中装置II是某同学配制此溶液时转移操作的示意图,图中有两处错误,一处是未用玻璃棒引流,另一处是_________________ 。
(4)在配制过程中,其他操作都是正确的,下列情况对所配制的NaCl溶液的浓度偏低有______。
A.没有洗涤烧杯和玻璃棒 B.容量瓶不干燥,含有少量蒸馏水 C.定容时俯视刻度线 D.定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)下列物质中:①能导电的是________(填代号,以下同);
②属于电解质的是____________;
③属于非电解质的是____________。
A.NaOH溶液 B.Cu C.液态HCl D.蔗糖溶液
E.液氯 F.氨水 G.胆矾晶体 H.无水乙醇
(2)若将0.2mol钠、镁、铝分别投入到100mL1mol·L-1的盐酸中,在标准状况下,产生氢气体积之比是_____________。
(3)取等质量的铁硅合金样品两份,分别投入到足量的稀盐酸和足量的稀氢氧化钠溶液中,充分反应后,收集到等量的氢气,则原合金样品中铁和硅的物质的量之比为______________________。
(4)向盛有10mL1mol·L-1NH4Al(SO4)2溶液的烧杯中滴加1mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积变化示意图如下:
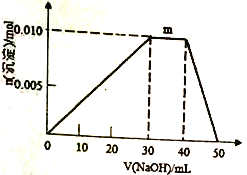
①写出m点反应的离子方程式____________________________________。
②若NH4Al(SO4)2溶液改加20mL1.2mol/LBa(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】教材中制取氯气的方法如下:
(1)电解法制氯气:观察如图1,回答: 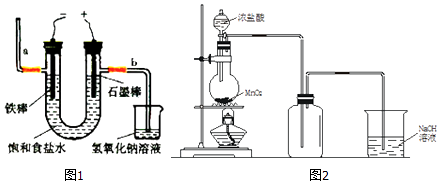
①此反应化学方程式为 .
②若饱和食盐水中含有酚酞,通电后(填“铁棒”或“石墨棒”)附近变红.图中b端产生的气体如用湿润的淀粉﹣KI试纸检验,其现象为 .
(2)实验室也可以用加热MnO2和浓盐酸制取Cl2 , 如图2
①盛装浓盐酸的仪器名称为;
②若要收集纯净且干燥的Cl2 , 此装置还应依次加入的试剂为;
③NaOH溶液的作用是 , 发生反应的化学方程式是;
④实验室用下列两种方法制氯气:I、用含HCl 146g的浓盐酸与足量的MnO2反应;
II、用87gMnO2与足量浓盐酸反应.所得的氯气
A. I比 II多 B. II比 I多 C.一样多 D.无法比较
⑤将Cl2溶于水得到新制的氯水,用玻璃棒蘸取新制的氯水,滴在pH试纸上,现象为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】到目前为止,由化学能转变的热能或电能仍然是人类使用最主要的能源.
(1)化学反应中放出的热能(焓变,△H)与反应物和生成物的键能(E)有关.已知:H2(g)+Cl2(g)=2HCl(g)△H=﹣a kJmol﹣1;E(H﹣H)=b kJmol﹣1 , E(Cl﹣Cl)=c kJmol﹣1 , 则:E(H﹣Cl)=;
(2)氯原子对O3的分解有催化作用:O3(g)+Cl(g)=ClO(g)+O2(g)△H1 , ClO(g)+O(g)=Cl(g)+O2(g)△H2 , 大气臭氧层的分解反应是O3+O=2O2△H.该反应的能量变化示意图如图1所示.则反应O3(g)+O(g)=2O2(g)的正反应的活化能为kJmol﹣1 . 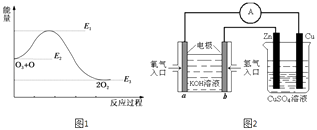
(3)实验中不能直接测出由石墨和氢气反应生成甲烷反应的反应热,但可测出CH4、石墨和H2燃烧反应的反应热,求由石墨生成甲烷的反应热.已知:
①CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=﹣a kJmol﹣1
②C(石墨)+O2(g)═CO2(g)△H=﹣b kJmol﹣1
③H2(g)+ ![]() O2(g)═H2O(l)△H=﹣c kJmol﹣1
O2(g)═H2O(l)△H=﹣c kJmol﹣1
则反应C(石墨)+2H2(g)→CH4(g)的反应热:
△H=kJmol﹣1 .
又已知:该反应为放热反应,△H﹣T△S可作为反应方向的判据,当△H﹣T△S<0时可自发进行;则该反应在什么条件下可自发进行 . (填“低温”、“高温”)
(4)有图2所示的装置,该装置中Cu极为极;当铜片的质量变化为12.8g时,a极上消耗的O2在标准状况下的体积为L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)按要求写出下列反应的化学方程式:
①由饱和FeCl3溶液制备Fe(OH)3胶体_______________________________。
②氢氟酸腐蚀玻璃____________________________________。
(2)按要求写出下列反应的离子方程式:
①制漂白粉(有效成分为次氯酸钙)____________________________________。
②用硫氰化钾溶液检验溶液中含有Fe3+____________________________________。
③向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性____________________________________。向以上中性溶液中继续滴加Ba(OH)2溶液,写出此步的离子方程式_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N4的分子结构类似白磷分子,它的结构如图所示,已知断裂1mol N﹣N键需要吸收167kJ热量,生成1mol N≡N键需放出942kJ热量.根据以上信息和数据,下列说法中正确的是( ) 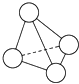
A.1 mol N4气体转变为N2将放出775 kJ热量
B.1 mol N4气体转变为N2将放出882 kJ热量
C.1 mol N4气体转变为N2将吸收775 kJ热量
D.1 mol N4气体转变为N2将吸收882 kJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能证明某烃分子里只含有一个碳碳双键的事实是( )
A. 该烃分子里碳氢原子个数比为1:2
B. 该烃能使酸性KMnO4溶液褪色
C. 该烃完全燃烧生成的CO2和H2O的物质的量相等
D. 该烃容易与溴水发生加成反应,且1mol该烃完全加成消耗1mol溴单质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com