
下列反应的离子方程式书写正确的是()
A. 氯化铝溶液中加入过量氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+
B. Cu溶于稀硝酸HNO3:Cu+2H++NO3﹣═Cu2++NO2↑+H2O
C. Fe2(SO4)3溶液和Ba(OH)2溶液反应:Fe3++SO42﹣+Ba2++3OH﹣═Fe(OH)3↓+BaSO4↓
D. 向Fe(OH)3中加入氢碘酸:Fe(OH)3+3H+═Fe3++3H2O
考点: 离子方程式的书写.
专题: 离子反应专题.
分析: A、氯化铝溶液和一水合氨反应生成氢氧化铝沉淀,氢氧化铝是两性氢氧化物,溶于强酸强碱,不溶于弱酸弱碱,据此分析;
B、铜和稀硝酸发生氧化还原反应,硝酸被还原为一氧化氮;
C、硫酸铁和氢氧化钡溶液反应生成硫酸钡沉淀和氢氧化铁沉淀,离子方程式中需要符合化学式的组成比;
D、铁离子具有氧化性能氧化碘离子为碘单质.
解答: 解:A、氯化铝溶液和一水合氨反应生成氢氧化铝沉淀,氢氧化铝是两性氢氧化物,溶于强酸强碱,不溶于弱酸弱碱,氯化铝溶液中加入过量氨水反应的离子方程式为:Al3++3NH3•H2O═Al(OH)3↓+3NH4+,故A正确;
B、铜和稀硝酸发生氧化还原反应,硝酸被还原为一氧化氮,反应的离子方程式为:3Cu+8H++2NO3﹣═3Cu2++2NO↑+4H2O,故B错误;
C、反应的离子方程式中需要符合化学式的组成比,Fe2(SO4)3溶液和Ba(OH)2溶液反应的离子方程式为:2Fe3++3SO42﹣+3Ba2++6OH﹣═2Fe(OH)3↓+3BaSO4↓,故C错误;
D、铁离子具有氧化性能氧化碘离子为碘单质,向Fe(OH)3中加入氢碘酸反应的离子方程式为:2Fe(OH)3+2I﹣+6H+═2Fe2++6H2O+I2,故D错误;
故选A.
点评: 本题考查了离子方程式的正误判断和书写方法,主要是量不同产物不同,氧化还原反应的产物判断,电荷守恒的分析应用,掌握基础是关键,题目较简单.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
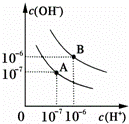
已知水在25℃和95℃时,其电离平衡曲线如图所示:
(1)则25℃时水的电离平衡曲线应为 (填“A”或“B”),请说明理由 .
(2)25℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为 .
(3)曲线B对应温度下,pH=2的HCl溶液和pH=10的某BOH溶液等体积混合后,混合溶液的pH=8.请分析其原因: .
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA代表阿伏加德罗常数说法不正确的是()
A. 醋酸的摩尔质量(单位:g/mol)与NA个醋酸分子的质量在数值上相等
B. NA个氧分子和NA个氢分子的质量比等于16:1
C. 28克氮气所含的原子数目为NA
D. 在标准状况下,0.5NA个氯气分子所占体积约为11.2L
查看答案和解析>>
科目:高中化学 来源: 题型:
在核磁共振氢谱图(1H核磁共振谱图)中,只有一个吸收峰的物质是()
A. CH3CH2OH B. CH3CH2CH3 C. CH2=CH﹣CH3 D. CH3CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
化学于生产、生活,并应用于生产、生活,下列有关说法不正确的是()
A. 明矾能水解生成氢氧化铝胶体,可用作净水剂
B. 石英、玛瑙、水晶通常作为装饰品使用,但都可溶于氢氟酸
C. Na2CO3俗称纯碱,可与盐酸反应,故可用于治疗人体内胃酸过多
D. 农村施肥时,草木灰不能与铵态氮肥混用,以免氮肥肥效下降
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值,下列叙述中正确的是()
A. 常温下,含1 mol Fe的铁片与过量浓HNO3反应,转移电子的数目为3 NA个
B. 19.2 g铜与足量的稀硝酸反应产生NO的体积为4.48 L
C. 标准状况下,33.6 L SO3含有9.03×1023个SO3分子
D. 在46 gNO2和N2O4的混合物气体中所含原子总数为3NA个
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是()
A. 欲配制质量分数为10%的ZnSO4溶液,将10g ZnSO4•7H2O溶解在90g水中
B. 常温常压下,22.4L的NO2气体含有1.81×1024个原子
C. 为鉴别KCl、AlCl3和MgCl2溶液,各取少量分别向三种溶液中滴加NaOH溶液至过量
D. 某溶液中加入盐酸能产生使石灰水变浑浊的气体,则该溶液中一定含有CO32﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)实验操作中,不慎将手指划破,这时可从急救箱中取FeCl3溶液止血,其原理是 .
(2)今有两瓶标签模糊不清,只知道分别盛有淀粉溶液和氯化钠溶液,试用2种方法对其鉴别.
① ;② .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com