
��6 g CaCO3��100 mLϡ���ᷴӦ��ȡ������CO2����Ӧ���������ɵ�CO2�������������Ϊ��״�����淴Ӧʱ��仯���������ͼ��ʾ������˵����ȷ���ǣ� ��
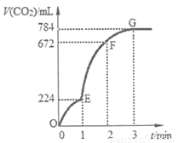
A��OE�α�ʾ��ƽ����Ӧ������죬���ܵ�ԭ���Ǹ÷�Ӧ�Ƿ��ȷ�Ӧ
B��EF����HC1Ũ�ȵļ�С��ʾ�ĸ÷�Ӧ��ƽ����Ӧ����Ϊ0.2 mol/��L��min��
C����F���ռ�����CO2��������
D����G���Ժ��ռ���CO2�����������࣬ԭ����ϡ�����ѷ�Ӧ��ȫ
 һ��һ����ʱ���ϵ�д�
һ��һ����ʱ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ��ʡ�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ʲ������л�����ǣ� ��
A�����軯� B��������
C������ D�����Ȼ�̼
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꽭��ʡ�����и�һ��ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ������
A��B��C��D��E��������Ԫ�ط������������ڣ���ԭ��������������B��D��ԭ������֮��Ϊ8��Bԭ���������������������������3����Cԭ����ͬ��������Ԫ����ԭ�Ӱ뾶���
�ش��������⣺
��1��B�����ڱ��е�λ��Ϊ ��A��E�γɵĻ������д��ڵĻ�ѧ���������� ��
��2��B��C��Dԭ�ӵİ뾶�Ӵ�С��˳���� ����Ԫ�ط��ű�ʾ����C������A�������ﷴӦ�Ļ�ѧ����ʽ�� ��
��3�����ʵ��֤��E�ķǽ����Ա�D�ķǽ�����ǿ ��д���������輰����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꽭��ʡ�����и�һ��ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
����ֻ�������Ӽ��Ļ�������
A��HI B��NaOH C��Br2 D��NaCl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ��ʡ��һ6���¿���ѧ�Ծ��������棩 ���ͣ������
��ԭ�������ĵ��������ֶ�����Ԫ�أ�����ĸX��ʾ��ԭ�Ӱ뾶����Դ�С��������ۻ�����۵ı仯����ͼ��ʾ��
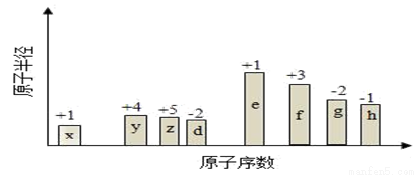
�����жϳ���Ԫ�ػش����⣺
��1��f��Ԫ�����ڱ���λ����__________��
��2���Ƚ�d��e�������ӵİ뾶��С���û�ѧʽ��ʾ����ͬ��_______��__________���Ƚ�g��h������������Ӧ��ˮ���������ǿ���ǣ�_______��__________��
��3��д��x��z�γ���ԭ�ӹ��ۻ�����ĵ���ʽ__________��
��4������A��һ�ֱ�ˮ�����״Һ�壬����x��y����Ԫ����ɣ�yԪ����xԪ�ص�������Ϊ12��1��A����Է�������Ϊ78��A��Ũ������Ũ������50-60�淴Ӧ�Ļ�ѧ��Ӧ����ʽ______����Ӧ����______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ��ʡ��һ6���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ���ǣ� ��
A�������һ�������ɸ�CH2ԭ���ţ��ҷ���ͬһͨʽ���л��ﻥ��Ϊͬϵ��
B�������ʺ���֬�����ڸ߷��ӻ����һ�������¶���ˮ��
C��������λ��Ԫȡ����ֻ��һ��˵�������в����ڵ�˫������
D��CH3-CH3 +Cl2��CH2ClCH2Cl�ķ�Ӧ����Ϊ�ӳɷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ��ʡ��һ6���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���б�ʾ���ʽṹ�Ļ�ѧ�����ģ����ȷ���ǣ� ��
A���ǻ��ĵ���ʽ��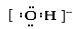
B��CH4 ���ӵ����ģ�ͣ�
C����ϩ�����ʽ��CH2
D�������ӵĽṹʾ��ͼ��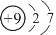
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ��ʡ�߶���ѧ�������¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����Һ�м�������Na2O2�����ܴ���������������ǣ� ��
A��NH4+��Ba2+��Cl-��NO3-
B��K+��AlO2-��Cl-��SO42-
C��Ca2+��Mg2+��NO3-��HCO3-
D��Na+��Cl-��CO32-��SO32-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���Ĵ�ʡ�ɶ��и߶���4���¿���ѧ�Ծ��������棩 ���ͣ������
ԭ������С��20��X��Y��Z��W����Ԫ�أ�����X���γɻ�������������Ԫ��֮һ��Yԭ�ӻ�̬ʱ���������������ڲ����������2����Zԭ�ӻ�̬ʱ2pԭ�ӹ������3��δ�ɶԵĵ��ӣ�W�γɵij������ʼ�����ǿ�ᷴӦ��������ǿ�Ӧ���ش��������⣺
��1��Y2X4������Yԭ�ӹ�����ӻ�����Ϊ ��1mol Y2X4���ЦҼ�����ĿΪ ��
��2��Ԫ��Y��һ����������Ԫ��Z��һ�������ﻥΪ�ȵ����壬Ԫ��Z������������ķ���ʽ�� ��
��3��������ZX3��ˮ�е��ܽ�ȱȻ�����YX4��ö࣬����Ҫԭ���� ��
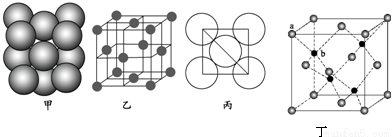
��4����д��W���ʺ�ǿ����Һ��Ӧ�����ӷ���ʽ ��W���ʵľ�����ԭ�ӵĶѻ���ʽ��ͼ����ʾ���侧��������ͼ����ʾ��ԭ��֮���λ�ù�ϵ��ƽ��ͼ��ͼ����ʾ����������ԭ�ӵ���λ��Ϊ ������֪W��ԭ�Ӱ뾶Ϊd��NA���������ӵ�������W�����ԭ������ΪM���þ�����ܶ�Ϊ ������ĸ��ʾ����
��5������ZnS�����ṹ��ͼ����ʾ����������Ķ��������λ��ΪZn2+����Zn2+����λ��Ϊ �����侧���߳�Ϊa pm��aλ��Zn2+��bλ��S2��֮��ľ���Ϊ pm����ʽ��ʾ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com