
| A.溶解的铁粉为2.8g | B.原溶液中C(SO42-)=0.5mol/L |
| C.原混合溶液中C(H+)=1.2mol/L | D.原溶液中n(NO3-)=0.08mol |
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源:不详 题型:单选题
| A.2.4g | B.3.36g | C.5.60g | D.6.4g |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
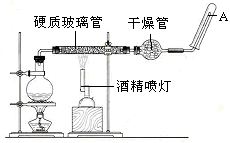
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
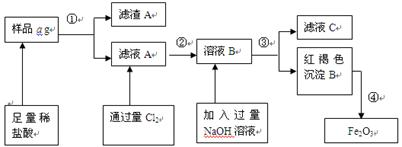
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
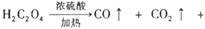
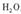 。下列装置中,可用作上述反应制取气体的是(填编号)。
。下列装置中,可用作上述反应制取气体的是(填编号)。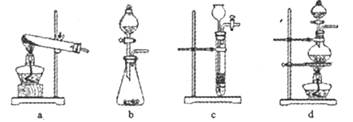
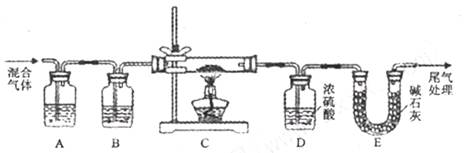
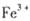 外还可能含有
外还可能含有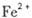 。若要确认其中的
。若要确认其中的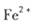 .应选用 ________________(填编号)。
.应选用 ________________(填编号)。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
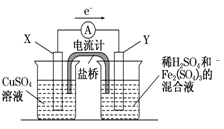
| | 正、负极判断 | 电极材料 | 电极反应式 |
| X极 | | | |
| Y极 | | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.5.6 g | B.2.8 g | C.8.4g | D.14 g |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
 量浓度以及产生氢气的体积。(注:氢气的体积测定环境为标准状况)
量浓度以及产生氢气的体积。(注:氢气的体积测定环境为标准状况)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com