
| A£® | 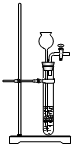 | B£® | 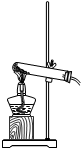 | C£® | 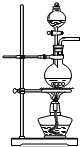 | D£® | 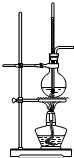 |
·ÖĪö ŹµŃéŹŅ²ÉÓĆ¼ÓČČŅŅ“¼ŗĶÅØĮņĖį»ģŗĻĪļµÄ·½·ØÖĘČ”ŅŅĻ©£¬ĪĀ¶ČæŲÖĘŌŚ170”ę£¬ŅŌ“ĖĄ“½ā“š£®
½ā“š ½ā£ŗA£®×°ÖĆƻӊ¼ÓČČ£¬²»ÄÜÖʱøŅŅĻ©£¬¹ŹA²»Ń”£»
B£®ĪŖ¹ĢĢå¼ÓČČ×°ÖĆ£¬²»ÄÜÖʱøŅŅĻ©£¬¹ŹB²»Ń”£»
C£®Ķ¼ÖŠ×°ÖĆ²»ÄÜæŲÖĘĪĀ¶Č£¬¹ŹC²»Ń”£»
D£®Ķ¼ÖŠ×°ÖĆĪŖŅŗĢå¼ÓČČ×°ÖĆ£¬ĒŅĪĀ¶Č¼Ęæɲā¶ØĪĀ¶Č£¬æÉĄūÓĆŅŅ“¼·¢ÉśĻūČ„·“Ó¦ÖʱøŅŅĻ©£¬¹ŹDŃ”£»
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²éŹµŃé×°ÖƵÄÓ¦ÓĆ£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕŅŅĻ©µÄÖʱøŌĄķ”¢ŹµŃé×°ÖƵÄ×÷ÓĆ”¢ŹµŃé¼¼ÄÜĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėŹµŃéÄÜĮ¦µÄ漲飬עŅāŅŅ“¼µÄĻūČ„·“Ó¦Ģõ¼ž£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | Ķ¼1±ķŹ¾ĻąĶ¬ĪĀ¶ČĻĀpH=1µÄŃĪĖįŗĶ“×ĖįČÜŅŗ·Ö±š¼ÓĖ®Ļ”ŹĶŹ±pHµÄ±ä»ÆĒśĻߣ¬ĘäÖŠĒśĻߢņĪŖŃĪĖį£¬ĒŅbµćČÜŅŗµÄµ¼µēŠŌ±ČaµćĒæ | |
| B£® | Ķ¼2ÖŠ“æĖ®½öÉżøßĪĀ¶Č£¬¾ĶæÉŅŌ“Óaµć±äµ½cµć | |
| C£® | Ķ¼1ÖŠ£¬bµćĖįµÄ×ÜÅØ¶Č“óÓŚaµćĖįµÄ×ÜÅØ¶Č | |
| D£® | Ķ¼2ÖŠŌŚbµć¶ŌÓ¦ĪĀ¶ČĻĀ£¬½«pH=2µÄH2SO4ÓėpH=10µÄNaOHČÜŅŗµČĢå»ż»ģŗĻŗó£¬ČÜŅŗĻŌÖŠŠŌ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŌŚ³£ĪĀĻĀ£¬³£Ń¹ĻĀ£¬11.2L N2ŗ¬ÓŠµÄ·Ö×ÓŹżĪŖ0.5 NA | |
| B£® | ±ź×¼×“æöĻĀ£¬11.2L±½Ėłŗ¬·Ö×ÓŹżĪŖ0.5NA | |
| C£® | ŌŚ³£ĪĀĻĀ£¬°Ń100 g CaCO3¼Óµ½1LĖ®ÖŠ£¬ĖłµĆČÜŅŗÖŠµÄCa2+ŹżµČÓŚNA | |
| D£® | ŌŚ±ź×¼×“æöĻĀ£¬22.4L CH4Óė18 g H2OĖłŗ¬ÓŠµÄµē×ÓŹż¾łĪŖ10NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÉśŹÆ»ŅÓėĖ®µÄ·“Ó¦ | B£® | ĀČ»Æļ§ÓėĒāŃõ»Æ±µµÄ·“Ó¦ | ||
| C£® | ŠæʬÓėĻ”ĮņĖįµÄ·“Ó¦ | D£® | ½šŹōÄĘÓėĄäĖ®µÄ·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
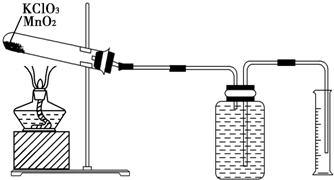
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
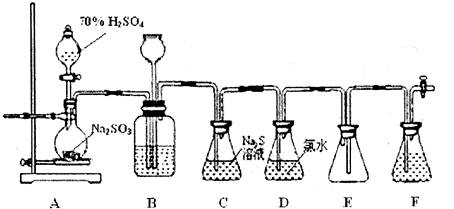
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĀĮ”¢Ģś”¢ĶĻą±Č½Ļ£¬ĶŌŖĖŲŌŚ×ŌČ»½ēÖŠµÄŗ¬Įæ×īµĶ”¢ĢśŌŖĖŲŗ¬Įæ×īøß | |
| B£® | Al2O3”¢MgOæÉÓĆ×÷øßĪĀ²ÄĮĻ£¬¶žŃõ»Æ¹čŹĒÉś²ś¹āĻĖÖĘĘ·µÄ»ł±¾ŌĮĻ | |
| C£® | ¹¤ŅµÉĻ²ÉÓƵē½āČŪČŚĢ¬Al2O3”¢MgOµÄ·½·ØŅ±Į¶Al”¢Mg | |
| D£® | ÓĆ“æ¼īÖĘ²£Į§”¢ÓĆĢśæóŹÆĮ¶Ģś”¢ÓĆ°±ÖĘĢ¼Ėįļ§¶¼»į²śÉśĪĀŹŅĘųĢå |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com