
【题目】为研究哈伯法合成氨反应,T℃时,在容积为2 L恒容容器中通入4 mol N2和12mol H2,反应如下: N2(g)+3H2(g) ![]() 2NH3(g) △H=-92.0kJmol-1,相关键能数据如下:
2NH3(g) △H=-92.0kJmol-1,相关键能数据如下:
N≡N | H-H | N-H | |
键能数据( kJ/mol) | 946 | 436 | X |
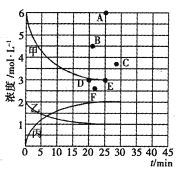
若25min时反应达到平衡,各物质浓度随时间变化曲线如下图中甲、乙、丙。回答下列问题:
(1)0-25min内,反应的平均速率v(H2)为_________;表中X=_________________。
(2)T℃时,该反应的平衡常数K=_____________ (用最简分数表达)。
(3)T℃时,若起始充入8mol N2和24 mol H2,则反应刚达到平衡时,表示c( H2)在右图中相应的点为_____(填字母)。
(4)以煤为主要原料的合成氨工业中,原料气氢气常用下述方法获得:
①C(s) +H2O(g)![]() CO(g) +H2(g) △H1
CO(g) +H2(g) △H1
②CO(g) +H2O(g)![]() CO2(g) +H2(g) △H2
CO2(g) +H2(g) △H2
若已知CO和H2的燃烧热分别为283 kJ·mol-l和285.8kJ·mol-l;H2O( g) =H2O(1) △H =-44kJ·mol-l 则△H2=_______________。
(5)氨气是生产硝酸的重要原料,其过程如下:
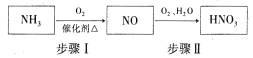
写出步骤I的化学方程式:_________________。
(6)下图是科学家提出的利用电解法常温常压下由氮气、氢气合成氨的示意图:
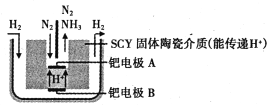
由图可知,钯电极B是电解池的________(填“阴极”或“阳极”);钯电极A上的电极反应式为________。
【答案】 0.12 moI/(L·min) 391 ![]() B -41.2 kJ·mol-1 4NH3 +5O2
B -41.2 kJ·mol-1 4NH3 +5O2![]() 4NO +6H2O 阳极 N2+6e-+6H+=2NH3
4NO +6H2O 阳极 N2+6e-+6H+=2NH3
【解析】(1) 在容积为2 L恒容容器中通入4 mol N2和12mol H2,根据图像,0-25min内,氢气的浓度变成3mol/L,反应的平均速率v(H2)= ![]() =
=![]() = 0.12 moI/(L·min); △H=-92.0KJmol-1=946+436×2-6X,解得X=391 KJmol-1,故答案为:0.12 moI/(L·min);391;
= 0.12 moI/(L·min); △H=-92.0KJmol-1=946+436×2-6X,解得X=391 KJmol-1,故答案为:0.12 moI/(L·min);391;
(2)T℃时,平衡时c(N2)=1mol/L,c(H2)=3mol/L,c(NH3)=2mol/L,该反应的平衡常数K= =
=![]() =
=![]() ,故答案为:
,故答案为: ![]() ;
;
(3)T℃时,若起始充入8mol N2和24 mol H2,相当于增大压强,若平衡不移动,氢气的浓度为原来的2倍为6mol.L,而增大压强,平衡正向移动,c( H2)减小,反应速率加快,建立平衡需要的时间缩短,故选B;
(4)已知:①CO(g)+![]() O2(g)═CO2(g)△H=-283.0kJ/mol;②H2(g)+
O2(g)═CO2(g)△H=-283.0kJ/mol;②H2(g)+![]() O2(g)═H2O(l)△H=-285.8kJ/mol;③H2O( g) =H2O(1) △H =kJ·mol-l,由盖斯定律可知,①-②+③可得CO(g)+H2O(g)=CO2(g)+H2(g)△H=-283.0kJ/mol-(-285.8)+(-44 kJ/mol)=-41.2kJ/mol,故答案为: -41.2kJ/mol;
O2(g)═H2O(l)△H=-285.8kJ/mol;③H2O( g) =H2O(1) △H =kJ·mol-l,由盖斯定律可知,①-②+③可得CO(g)+H2O(g)=CO2(g)+H2(g)△H=-283.0kJ/mol-(-285.8)+(-44 kJ/mol)=-41.2kJ/mol,故答案为: -41.2kJ/mol;
(5)步骤I中氨气被氧化为NO ,反应的化学方程式为4NH3 +5O2![]() 4NO +6H2O,故答案为:4NH3 +5O2
4NO +6H2O,故答案为:4NH3 +5O2![]() 4NO +6H2O;
4NO +6H2O;
(6)由图可知,钯电极A上氮气反应生成了氨气,发生了还原反应,是阴极,则是钯电极B是电解池的阳极;钯电极A上的电极反应式为N2+6e-+6H+=2NH3,故答案为:阳极;N2+6e-+6H+=2NH3。


科目:高中化学 来源: 题型:
【题目】下图为阿托酸甲酯的一种合成路线:

已知:反应③为取代反应,另一反应产物为乙醇
请回答下列问题:
(1)已知A为芳香烃,其核磁共振氢谱中出现5个蜂,其面积比为1:1:2:2:2,则A的名称为___________,
(2)写出有关的化学方程式
反应②__________________________;
反应③__________________________。
(3)阿托酸甲酯所含官能团的名称为____________________;阿托酸甲酯有多种同分异构体,其中苯环上只有一个支链,既能与NaHCO3溶液反应,又能使溴的四氯化碳溶液褪色的同分异构体有__________种(不考虑立体异构)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一氯甲烷(CH3Cl)是一种重要的化工原料,常温下它是无色有毒气体,微溶于水,易溶于乙醇、CCl4等。
(1)甲组同学在实验室用下图所示装置模拟催化法制备和收集一氯甲烷。
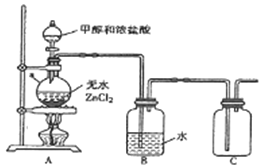
①仪器a的名称为___________。
②无水ZnCl2为催化剂,a瓶中发生反应的化学方程式为_____________。
③装置B的主要作用是_____________。
(2)乙组同学选用甲组A、B装置和下图所示的部分装置检验CH3Cl中的氯元素。
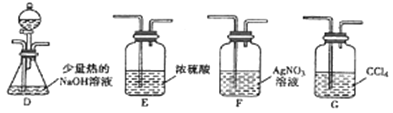
①乙组同学的实验装置中,依次连接的合理顺序为A→B→_____→_____→_____。
②通入一段时间的CH3Cl气体,打开装置D中分液漏斗的活塞先后加入两种试剂,观察实验现象。分液漏斗中先后加入的试剂是_______________。
③能证明CH3Cl中含有氯元素的实验现象是____________。
(3)查阅资料可知:AgNO3的乙醇溶液可以检验CH3Cl中的卤素原子。相关数据如下表:
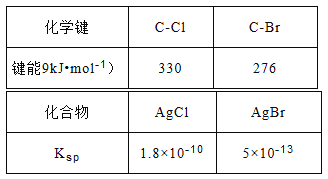
将CH3Cl和CH3Br的混合气体通入AgNO3的乙醇溶液中,先出现淡黄色沉淀。请依据表中数据解释原因__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、W为五种短周期元素,X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15,X与Z可形成XZ2分子;丫与M形成的气态化合物在标准状况下的密度为0.76g·L-1; W的质子数是X、Y、Z、M四种元素质子数之和的![]() ,下列说法正确的是
,下列说法正确的是
A. 原子半径:W>Z>Y>X>M
B. YZ2溶于水形成的溶液具有较强的氧化性
C. 由X、Y、Z、M四种元素形成的化合物一定既有离子键,又有共价键
D. 1 molWM溶于足量水中完全反应共转移2mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素A、B、C、D,它们的原子序数依次增大。其中A、C与B、D分别是同主族元素。又知B、D两元素的原子核中质子数之和是A、C两元素原子核中质子数和的2倍。这四种元素的单质中有2种气体,2种固体。
(1)写出元素符号:A______;B______;
(2)写出元素D在元素周期表中的位置______;
(3)写出C元素的单质与B元素的单质在常温下反应的化学方程式______;
(4)写出两种均含有A、B、C、D四种元素的化合物相互作用逸出气体的离子方程式______;
(5)A、C组成的化合物,常作为野外考察的取氢(H2)剂。该化合物中加入适量的水,即可形成氢气。写出制氢化学方程式______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁电池能长时间保持稳定的放电电压,有广泛的应用前景。总反应为:3Zn+2K2FeO4+8H2O ![]() 3Zn(OH)2+2Fe(OH)3+4KOH。下列叙述错误的是
3Zn(OH)2+2Fe(OH)3+4KOH。下列叙述错误的是
A. 充电时,Zn板应与外接电源的负极相连
B. 放电时,溶液中的OH-从正极向负极移动
C. 正极反应式为:FeO42-+3e-+4H2O= Fe(OH)3+5OH-
D. 充电时,当转移0.2mol电子时,阴极质量增加3.4g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学镀镍是指不使用外加电流,利用氧化还原作用在金属制件的表面上沉积一层镍的方法。次磷酸钠(NaH2PO2)是化学镀镍的重要原料,工业上制备NaH2PO2·H2O的流程如下:

回答下列问题:
⑴次磷酸钠(NaH2PO2)是次磷酸(H3PO2)与足量NaOH溶液反应的产物,NaH2PO2属于_______(填“正盐”“酸式盐”“碱式盐”), NaH2PO2中磷元素的化合价为___________。
(2)在反应器中加入乳化剂并高速搅拌的目的是________________
(3)在反应器中发生多个反应,其中白磷(P4)与Ca(OH)2反应生成次磷酸钠及磷化氢的化学方程式为_________________________
(4)流程中通入CO2的目的是______________,滤渣X的化学式为_____________
(5)流程中母液中的溶质除NaH2PO2外,还有的一种主要成分为_____________
(6)含PH3的废气可用NaClO和NaOH的混合溶液处理将其转化为磷酸盐,该反应的离子方程式为____________
(7)某次生产投入的原料白磷为1240 kg,在高速乳化反应器中有80%的白磷转化为次磷酸钠及磷化氢,忽略其它步骤的损失,理论上最终得到产品NaH2PO2·H2O的质量应为__________kg(NaH2PO2·H2O的相对分子质量为106)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com