
| A. | CH3OH的标准燃烧热为△H=-192.9 kJ•mol-1 | |
| B. | 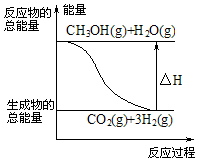 反应①中的能量变化如图所示 | |
| C. | CH3OH转变成H2的过程一定要吸收能量 | |
| D. | 根据②推知反应:CH3OH(l)+$\frac{1}{2}$O2(g)=CO2(g)+2H2(g)的△H>-192.9kJ•mol-1 |
分析 A.利用盖斯定律,②×3-①×2可得甲醇燃烧的热化学方程式,进而可知甲醇的燃烧热;
B.反应①为吸热反应,反应物总能量小于生成物总能量;
C.根据已知的甲醇转化为氢气的两种反应原理来判断;
D.根据物质的能量大小与物质的状态关系来判断.
解答 解:A.甲醇燃烧应生成二氧化碳和水,故A错误;
B.反应①为吸热反应,反应物总能量小于生成物总能量,故B错误;
C.由已知可知,反应①为吸热反应,而反应②为放热反应,故C错误;
D.同物质的量的同种物质,气态能量最高,其次液态能量,固态能量最低,由②推知反应:CH3OH(l)+$\frac{1}{2}$O2(g)=CO2(g)+2H2(g)的△H>-192.9kJ•mol-1,故D正确.
故选D.
点评 本题考查化学反应的反应热的计算,为高频考点,侧重于学生的分析能力的考查,注意在比较反应热大小时要带符号比较,并注意盖斯定律的应用来解答.


科目:高中化学 来源: 题型:选择题
| A. | 原子易形成-2价阴离子 | |
| B. | 单质均为双原子分子,具有氧化性 | |
| C. | 原子半径随原子序数递增逐渐减小 | |
| D. | 氢化物的稳定性随原子序数递增依次增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应速率用于衡量化学反应进行的快慢 | |
| B. | 决定反应速率的主要因素是反应物的性质 | |
| C. | 反应速率越大,反应现象就一定越明显 | |
| D. | 增大反应物的浓度、提高反应温度都能增大反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用试管夹夹试管应从试管底往上套,拇指按在试管夹的短柄上 | |
| B. | 装碘的试剂瓶中残留的碘可以用酒精洗涤 | |
| C. | 配制溶液时,如果试样是液体,用量筒量取试样后直接倒入容量瓶中,缓慢加入蒸馏水到接近刻度线1~2 cm处,用滴管滴加蒸馏水到刻度线 | |
| D. | 定容时,俯视刻度线,会使所配溶液的浓度偏低 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 醇的官能团是羟基(-OH) | B. | 酚的官能团是羟基(-OH) | ||
| C. | 醛的官能团是醛基(-CHO) | D. | 羧酸的官能团是羟基(-OH) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
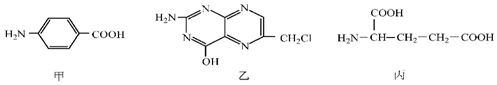
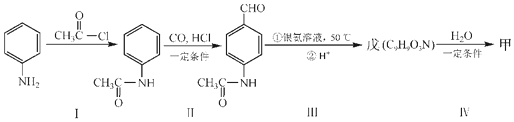
 .
. .
.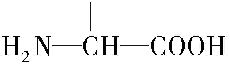 b.在稀硫酸中水解有乙酸生成.
b.在稀硫酸中水解有乙酸生成.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com