
”¾ĢāÄæ”æ·śĢ¼īęæó(Ö÷ŅŖ³É·ÖĪŖCeFCO3)ŹĒĢįČ”Ļ”ĶĮ»ÆŗĻĪļ”¢Ņ±Į¶īęµÄÖŲŅŖæóĪļŌĮĻ£¬ŅŌ·śĢ¼īęæóĪŖŌĮĻĢįČ”īęµÄ¹¤ŅÕĮ÷³ĢČēĶ¼ĖłŹ¾”£

»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©CeFCO3ÖŠCeµÄ»ÆŗĻ¼ŪĪŖ___________”£
£Ø2£©Ńõ»ÆÅąÉÕŹ±²»ÄÜŹ¹ÓĆĢÕ“ÉČŻĘ÷£¬ŌŅņŹĒ_________________”£Ńõ»Æ±ŗÉÕŗóµÄ²śĪļÖ®Ņ»ĪŖCeO2£¬ŌņĖį½žŹ±·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ____________________”£²Ł×÷¢ńµÄĆū³ĘĪŖ_________”£
£Ø3£©ĪŖĮĖĢįøßĖį½žĀŹ£¬æÉŅŌŹŹµ±Ģįøß·“Ó¦ĪĀ¶Č£¬µ«ĪĀ¶ČĘ«øß½ž³öĀŹ·“¶ų»į¼õŠ”£¬ĘäŌŅņŹĒ_______________”£
£Ø4£©ŅŃÖŖÓŠ»śĪļHTÄܽ«Ce3+“ÓĖ®ČÜŅŗÖŠŻĶČ”³öĄ“£¬øĆ¹ż³ĢæɱķŹ¾ĪŖCe3+(Ė®²ć)+3HT(ÓŠ»ś²ć) ![]() CeT3(ÓŠ»ś²ć)+3H+(Ė®²ć)”£ĻņCeT3(ÓŠ»ś²ć)ÖŠ¼ÓČėĻ”ĮņĖįÄÜ»ńµĆ½Ļ“æµÄŗ¬Ce3+Ė®ČÜŅŗ£¬“ÓĘ½ŗā½Ē¶Č½āŹĶĘäŌŅņ£ŗ____________________”£
CeT3(ÓŠ»ś²ć)+3H+(Ė®²ć)”£ĻņCeT3(ÓŠ»ś²ć)ÖŠ¼ÓČėĻ”ĮņĖįÄÜ»ńµĆ½Ļ“æµÄŗ¬Ce3+Ė®ČÜŅŗ£¬“ÓĘ½ŗā½Ē¶Č½āŹĶĘäŌŅņ£ŗ____________________”£
£Ø5£©298KŹ±£¬Ļņc(Ce3+)=0.02mol”¤L-1µÄČÜŅŗÖŠ¼ÓČėĒāŃõ»ÆÄĘĄ“µ÷½ŚČÜŅŗµÄpH£¬Čō·“Ó¦ŗóČÜŅŗpH=10£¬“ĖŹ±Ce3+ŹĒ·ń³ĮµķĶźČ«£æ__________________{ĮŠŹ½¼ĘĖć£¬ŅŃÖŖ£ŗKsp[Ce(OH)3]5”Įl0-20£¬c(Ce3+)-5mol”¤L-1 ŹÓĪŖ³ĮµķĶźČ«}”£
£Ø6£©Š“³öĻņCe(OH)3Šü×ĒŅŗÖŠĶØČėŃõĘųµĆµ½²śĘ·Ce(OH)4µÄ»Æѧ·½³ĢŹ½£ŗ_______________________”£
”¾“š°ø”æ +3 ĢÕ“É»įÓėÉś³ÉµÄHF·“Ó¦ 2CeO2+H2O2+6H+=2Ce3++O2”ü+4H2O ·ÖŅŗ ĪĀ¶ČÉżøߣ¬Ė«ŃõĖ®·¢Éś·Ö½ā£¬Ōģ³É½ž³öĀŹĘ«Š” Ļņ»ģŗĻŅŗÖŠ¼ÓČėĻ”ĮņĖį£¬Ź¹c(H+)Ōö“ó£¬Ę½ŗāĻņŠĪ³ÉCe3+Ė®ČÜŅŗ·½ĻņŅĘ¶Æ c(Ce3+)”Į(10-4)3=1.5”Į10-20, c(Ce3+)=1.5”Į10-8mol”¤L-1<1”Į10-5mol”¤L-1£¬Ce3+³ĮµķĶźČ« 4Ce(OH)3+O2+2H2O=4Ce(OH)4
”¾½āĪö”æ£Ø1£©CeFCO3ÖŠFĪŖ-1¼Ū”¢CĪŖ+4¼Ū”¢ŃõĪŖ-2¼Ū£¬Ķعż¼ĘĖćæÉÖŖCeµÄ»ÆŗĻ¼ŪĪŖ+3¼Ū£»£Ø2£©Ńõ»ÆÅąÉÕŹ±²»ÄÜŹ¹ÓĆĢÕ“ÉČŻĘ÷£¬ŌŅņŹĒĢÕ“ÉÖŠµÄ¶žŃõ»Æ¹č»įÓėÉś³ÉµÄHF·“Ó¦£»Ńõ»Æ±ŗÉÕŗóµÄ²śĪļÖ®Ņ»ĪŖCeO2£¬ŌņĖį½žŹ±CeO2ŌŚĖįŠŌĢõ¼žĻĀ±»Ė«ŃõĖ®Ńõ»Æ£¬·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ2CeO2+H2O2+6H+=2Ce3++O2”ü+4H2O£»²Ł×÷¢ńŹĒŌŚ¼ÓČėŻĶČ”¼Įŗó·ÖĄė³öÓŠ»ś²ćŗĶĮņĖįīęĻ”ČÜŅŗ£¬ŌņĘäĆū³ĘĪŖ·ÖŅŗ£»£Ø3£©ĪŖĮĖĢįøßĖį½žĀŹ£¬æÉŅŌŹŹµ±Ģįøß·“Ó¦ĪĀ¶Č£¬µ«ĪĀ¶ČĘ«øß½ž³öĀŹ·“¶ų»į¼õŠ”£¬ĘäŌŅņŹĒĪĀ¶ČÉżøߣ¬Ė«ŃõĖ®·¢Éś·Ö½ā£¬Ōģ³É½ž³öĀŹĘ«Š”£»£Ø4£©Ę½ŗāCe3+(Ė®²ć)+3HT(ÓŠ»ś²ć) ![]() CeT3(ÓŠ»ś²ć)+3H+(Ė®²ć)£¬Ļņ»ģŗĻŅŗÖŠ¼ÓČėĻ”ĮņĖį£¬Ź¹c(H+)Ōö“ó£¬Ę½ŗāĻņŠĪ³ÉCe3+Ė®ČÜŅŗ·½ĻņŅĘ¶Æ£¬ÄÜ»ńµĆ½Ļ“æµÄŗ¬Ce3+Ė®ČÜŅŗ£»£Ø5£©pH=10Ź±£¬c(OH-)=10-4mol/L£¬c(Ce3+)”Į(10-4)3=1.5”Į10-20£¬c(Ce3+)=1.5”Į10-8mol”¤L-1<1”Į10-5mol”¤L-1£¬Ce3+³ĮµķĶźČ«£»£Ø6£©ĻņCe(OH)3Šü×ĒŅŗÖŠĶØČėŃõĘųµĆµ½²śĘ·Ce(OH)4µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ4Ce(OH)3+O2+2H2O=4Ce(OH)4”£
CeT3(ÓŠ»ś²ć)+3H+(Ė®²ć)£¬Ļņ»ģŗĻŅŗÖŠ¼ÓČėĻ”ĮņĖį£¬Ź¹c(H+)Ōö“ó£¬Ę½ŗāĻņŠĪ³ÉCe3+Ė®ČÜŅŗ·½ĻņŅĘ¶Æ£¬ÄÜ»ńµĆ½Ļ“æµÄŗ¬Ce3+Ė®ČÜŅŗ£»£Ø5£©pH=10Ź±£¬c(OH-)=10-4mol/L£¬c(Ce3+)”Į(10-4)3=1.5”Į10-20£¬c(Ce3+)=1.5”Į10-8mol”¤L-1<1”Į10-5mol”¤L-1£¬Ce3+³ĮµķĶźČ«£»£Ø6£©ĻņCe(OH)3Šü×ĒŅŗÖŠĶØČėŃõĘųµĆµ½²śĘ·Ce(OH)4µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ4Ce(OH)3+O2+2H2O=4Ce(OH)4”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ£Ø¶ąŃ”£©Ęū³µ¾ēĮŅÅöײŹ±£¬°²Č«ĘųÄŅÖŠ·¢Éś·“Ó¦10NaN3+2KNO3ØTK2O+5Na2O+16N2”ü£®ČōŃõ»Æ²śĪļ±Č»¹Ō²śĪļ¶ą1.75mol£¬ŌņĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ£Ø £©
A.Éś³É42.0 L N2£Ø±ź×¼×“æö£©
B.×ŖŅʵē×ÓµÄĪļÖŹµÄĮæĪŖ1.25 mol
C.ÓŠ0.250 mol KNO3±»Ńõ»Æ
D.±»Ńõ»ÆµÄNŌ×ÓµÄĪļÖŹµÄĮæĪŖ3.75 mol
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀŹö¹ŲÓŚĢžµÄĖµ·ØÖŠ£¬ÕżČ·µÄŹĒ£Ø £©
A. ĢžŹĒÖø½öŗ¬ÓŠĢ¼ŗĶĒāĮ½ÖÖŌŖĖŲµÄÓŠ»śĪļ
B. ĢžŹĒÖø·Ö×ÓĄļŗ¬Ģ¼ŌŖĖŲµÄ»ÆŗĻĪļ
C. ĢžŹĒÖøČ¼ÉÕ·“Ó¦ŗóÉś³É¶žŃõ»ÆĢ¼ŗĶĖ®µÄÓŠ»śĪļ
D. ĢžŹĒÖøŗ¬ÓŠĢ¼ŗĶĒāŌŖĖŲµÄ»ÆŗĻĪļ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĪŖĮĖŹµĻÖ”°½«Č«ĒņĪĀ¶ČÉĻÉż·ł¶ČæŲÖĘŌŚ2”ęŅŌÄŚ”±µÄÄæ±ź£¬æĘѧ¼ŅÕżŌŚŃŠ¾æĪĀŹŅĘųĢåCO2µÄ×Ŗ»ÆŗĶĄūÓĆ”£
£Ø1£©ŗ£ŃóŹĒµŲĒņÉĻĢ¼ŌŖĖŲµÄ×ī“ó”°ĪüŹÕ³Ų”±
¢ŁČÜÓŚŗ£Ė®ÖŠµÄCO2Ö÷ŅŖŅŌĖÄÖÖĪŽ»śĢ¼ŠĪŹ½“ęŌŚ£¬·Ö±šĪŖCO2”¢H2CO3”¢CO32-ŗĶ_________(ĢīĄė×Ó·ūŗÅ)”£
¢ŚŌŚŗ£ŃóÖŠ£¬æÉĶعżČēĶ¼ĖłŹ¾µÄĶ¾¾¶Ą“¹ĢĢ¼”£Ōņ·¢Éś¹āŗĻ×÷ÓĆŹ±£¬CO2ÓėH2O·“Ӧɜ³É(CH2O)xŗĶO2µÄ»Æѧ·½³ĢŹ½ĪŖ__________________”£

£Ø2£©ÓŠæĘѧ¼ŅĢį³öæÉĄūÓĆFeOĄ“ĪüŹÕCO2£¬ŅŃÖŖ£ŗ
C(s)+2H2O(g)![]() CO2(g)+2H2(g) ”÷H=+113.4 kJ”¤mol-1
CO2(g)+2H2(g) ”÷H=+113.4 kJ”¤mol-1
3FeO(s)+H2O(g)![]() Fe3O4(s)+H2(g) ”÷H=+18.7 kJ”¤mol-1
Fe3O4(s)+H2(g) ”÷H=+18.7 kJ”¤mol-1
Ōņ6FeO(s)+CO2(g)![]() 2Fe3O4(s)+C(s) ”÷H=_____kJ”¤mol-1”£
2Fe3O4(s)+C(s) ”÷H=_____kJ”¤mol-1”£
£Ø3£©ŅŌCO2ĪŖŌĮĻæÉÖʱø¼×“¼£ŗCO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)£¬ĻņŅ»ŗćČŻĆܱÕČŻĘ÷ÖŠ³äČė1moCO2(g)ŗĶ3molH2(g)£¬²āµĆCO2(g)ŗĶCH3OH(g)µÄÅضČĖꏱ¼äµÄ±ä»ÆČēĶ¼ĖłŹ¾”£
CH3OH(g)+H2O(g)£¬ĻņŅ»ŗćČŻĆܱÕČŻĘ÷ÖŠ³äČė1moCO2(g)ŗĶ3molH2(g)£¬²āµĆCO2(g)ŗĶCH3OH(g)µÄÅضČĖꏱ¼äµÄ±ä»ÆČēĶ¼ĖłŹ¾”£
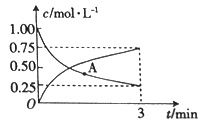
¢ŁČōAµćµÄÕż·“Ó¦ĖŁĀŹÓĆvÕż(CO2)Ą“±ķŹ¾£¬AµćµÄÄę·“Ó¦ĖŁĀŹÓĆvÄę(CO2)Ą“±ķŹ¾£¬ŌņvÕż(CO2)_______(Ģī”°>”±”° <”±»ņ”°=”±)vÄę(CO2)”£
¢Ś0”«3minÄŚ£¬ĒāĘųµÄĘ½¾ł·“Ó¦ĖŁĀŹv(H2)_______________”£
£Ø4£©ŌŚŅ»¶ØĢõ¼žĻĀ£¬¶žŃõ»ÆĢ¼×Ŗ»ÆĪŖ¼×Ķé£ŗCO2(g)+4H2(g)![]() CH4(g)+2 H2O(g)£¬”÷H”£ĻņŅ»ĆܱÕČŻ»żÕż³äČėŅ»¶ØĮæµÄCO2ŗĶH2£¬ŌŚ300”ꏱ·¢ÉśÉĻŹö·“Ó¦£¬“ļµ½Ę½ŗāŹ±²āµĆc(CO2)= 0.2 mol”¤L-1£¬c(H2) =0.8 mol”¤L-1£¬c(H2O)=1.6mol”¤L-1”£ŌņøĆĪĀ¶ČĻĀÉĻŹö·“Ó¦µÄĘ½ŗā³£ŹżK= ________”£Čō200”ꏱøĆ·“Ó¦µÄĘ½ŗā³£ŹżK=64.8£¬ŌņøĆ·“Ó¦µÄ”÷H_____(Ģī”°£¾”Ɣƻņ”°<”±)O”£
CH4(g)+2 H2O(g)£¬”÷H”£ĻņŅ»ĆܱÕČŻ»żÕż³äČėŅ»¶ØĮæµÄCO2ŗĶH2£¬ŌŚ300”ꏱ·¢ÉśÉĻŹö·“Ó¦£¬“ļµ½Ę½ŗāŹ±²āµĆc(CO2)= 0.2 mol”¤L-1£¬c(H2) =0.8 mol”¤L-1£¬c(H2O)=1.6mol”¤L-1”£ŌņøĆĪĀ¶ČĻĀÉĻŹö·“Ó¦µÄĘ½ŗā³£ŹżK= ________”£Čō200”ꏱøĆ·“Ó¦µÄĘ½ŗā³£ŹżK=64.8£¬ŌņøĆ·“Ó¦µÄ”÷H_____(Ģī”°£¾”Ɣƻņ”°<”±)O”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÉś»īÖŠ³£ÓĆŅ©Ę·ŗܶą£¬Čē£ŗaµā¾Ę bĀé»Ę¼ī cĒąĆ¹ĖŲ d°¢Ė¾Ę„ĮÖ eĘĻĢŃĢĒ×¢ÉäŅŗ fĪøŹęĘ½£Øŗ¬Ńõ»ÆĀĮ£¬µķ·Ū£©
£Ø1£©ÉĻŹöĪļÖŹÖŠŹōÓŚæ¹ÉśĖŲµÄŹĒ_______£ØĢīŠņŗÅ£¬ĻĀĶ¬£©
£Ø2£©ÓĆ×÷Ņ½ÓĆʤ·ōĻū¶¾µÄŹĒ________£¬
£Ø3£©ĪøŹęĘ½æÉ·ĄÖĪĪøĖį·ÖĆŚ¹ż¶ą£¬Ęä·¢»Ó¹¦Š§µÄĄė×Ó·½³ĢŹ½ŹĒ_________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¾Żæ¼Ö¤£¬ÉĢ“śĮ¶Ķ£¬Ö÷ŅŖæóĪļŌĮĻŹĒæ×ČøŹÆ£¬Ö÷ŅŖČ¼ĮĻŹĒľĢ棬Ņ±Į¶ĪĀ¶Č¹Ą¼ĘŌŚ1000”ę×óÓŅ£¬æÉÄÜÉę¼°µÄ·“Ó¦ÓŠ£ŗ¢ŁCu2£ØOH£©2CO3 ![]() 2CuO+CO2”ü+H2O
2CuO+CO2ӟ+H2O
¢Ś2CuO+C ![]() 2Cu+CO2”ü
2Cu+CO2ӟ
¢ŪCuO+CO ![]() Cu+CO2
Cu+CO2
¢ÜCO2+C ![]() 2CO
2CO
£Ø1£©“ÓĖÄÖÖ»ł±¾·“Ó¦ĄąŠĶæ“£¬¢Ł¢Ś¢Ü·Ö±šŹōÓŚ”¢”¢ £®
£Ø2£©ŌŚÉĻŹö·“Ó¦ÖŠ£¬ŹōÓŚŃõ»Æ»¹Ō·“Ó¦µÄŹĒ£ØĢīŠņŗÅ£©£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ°®»¤»·¾³ŹĒĪŅĆĒĆæŅ»øöČĖ²»æÉĶĘŠ¶µÄŌšČĪ”£ĻĀĮŠĻÖĻóÓėĪŪČ¾Ō“¶ŌÓ¦²»ÕżČ·µÄŹĒ£Ø £©
A.ĖįÓź”Ŗ”ŖĮņµÄŃõ»ÆĪļ”¢µŖµÄŃõ»ÆĪļB.¹ā»ÆѧŃĢĪķ”Ŗ”ŖµŖµÄŃõ»ÆĪļ
C.³ōŃõæÕ¶“”Ŗ”Ŗ·śĀČĢž£Ø¼“·śĄū°ŗ£©D.ĪĀŹŅŠ§Ó¦”Ŗ”ŖSO2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ£Ø¶ąŃ”£©ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A.ĶßĖ¹ÖŠ¼×ĶéŗĶŃõĘųµÄÖŹĮæ±ČĪŖ1£ŗ4Ź±¼«Ņ×±¬ÕØ£¬“ĖŹ±¼×ĶéÓėŃõĘųµÄĢå»ż±ČĪŖ1£ŗ2
B.ÓūÅäÖĘ1.00 L1.00 molL©1µÄNaClČÜŅŗ£¬æɽ«58.5 g NaClČÜÓŚ1.00 LĖ®ÖŠ
C.22.4LN2ŗĶH2µÄ»ģŗĻĘųĢåÖŠŗ¬NAøöŌ×Ó
D.3molµ„ÖŹFeĶźČ«×Ŗ±äĪŖFe3O4 £¬ µĆµ½8NAøöµē×Ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ±ź×¼×“æöĻĀ£¬560mLijĘųĢåAµÄÖŹĮæĪŖ0.75g£¬ŌņĘäĦ¶ūÖŹĮæĪŖ£»ŅŃÖŖøĆĘųĢåŌŚĖ®ÖŠµÄČܽā¶ČĪŖ448£ØĘųĢåČܽā¶ČÖøøĆĘųĢåŌŚŃ¹ĒæĪŖ101kPa£¬0”ꏱ£¬ČܽāŌŚ1Ģå»żĖ®Ąļ“ļµ½±„ŗĶדĢ¬Ź±µÄĘųĢåµÄĢå»ż£©£¬ŌņµĆµ½µÄ±„ŗĶČÜŅŗÖŠČÜÖŹAµÄÖŹĮæ·ÖŹżĪŖ£ØA²»ÓėĖ®·“Ó¦£©£¬Čō²āµĆøĆČÜŅŗĆܶČĪŖ1.24g/cm3 £¬ ŌņøĆČÜŅŗµÄĪļÖŹµÄĮæÅضČĪŖ £®
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com