
【题目】下列关于电解质溶液的叙述正确的是( )
A.常温下,在pH=7的醋酸钠和醋酸混合溶液中:c(CH3COO﹣)>c(Na+)
B.稀释醋酸溶液,溶液中所有离子的浓度均降低
C.在pH=5的氯化钠和稀硝酸的混合溶液中,c(Na+)=c(Cl﹣)
D.0.1molL﹣1的硫化钠溶液中,c(OH﹣)=c(H+)+c(HS﹣)+c(H2S)
【答案】C
【解析】解:A.常温下,在pH=7的醋酸钠和醋酸混合溶液中c(H+)=c(OH﹣),电荷守恒式为c(H+)+c(Na+)=c(OH﹣)+c(CH3COO﹣),则c(CH3COO﹣)=c(Na+),故A错误;B.稀释醋酸溶液,c(H+)减小,Kw不变,则醋酸稀释时c(OH﹣)增大,故B错误;
C.pH=5的溶液中c(H+)>c(OH﹣),由电荷守恒可知,c(Na+)+c(H+)=c(OH﹣)+c(Cl﹣)+c(NO3﹣),则c(Na+)<c(Cl﹣)+c(NO3﹣),但钠离子、氯离子均来源氯化钠的电离,则c(Na+)=c(Cl﹣),故C正确;
D.硫化钠溶液中,由电荷守恒可知c(Na+)+c(H+)=2c(S2﹣)+c(HS﹣)+c(OH﹣),由物料守恒可知 ![]() c(Na+)=c(S2﹣)+c(HS﹣)+c(H2S),则c(OH﹣)=c(H+)+c(HS﹣)+2c(H2S),故D错误;
c(Na+)=c(S2﹣)+c(HS﹣)+c(H2S),则c(OH﹣)=c(H+)+c(HS﹣)+2c(H2S),故D错误;
故选C.


科目:高中化学 来源: 题型:
【题目】不粘锅的内壁有一薄层为聚四氟乙烯的涂层,用不粘锅烹烧饭菜时不易粘锅,下列关于聚四氟乙烯的说法正确的是( )
A.聚四氟乙烯分子中含有双键
B.聚四氟乙烯的单体不是饱和烃
C.聚四氟乙烯中氟的质量分数是76%
D.聚四氟乙烯的化学活泼性很大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钒和镍及其化合物是重要的合金材料和催化剂,其储氢合金可作为一种新型锌离子电池的负极材料,该电池以Zn(CF3SO3)2为电解质,以有缺陷的阳离子型ZnMn2O4为电极,成功获得了稳定的大功率电流。
(1)基态钒原子的价电子排布式为_______,其排布时能量最高的电子所占据能级的原子轨道有_______个伸展方向。
(2)VO2+与 可形成配合物。
可形成配合物。 中,三种非金属元素的电负性由大到小的顺序为_______ (用元素符号表示)。
中,三种非金属元素的电负性由大到小的顺序为_______ (用元素符号表示)。
(3)镍形成的配离子[Ni(NH3)6]2+、[Ni(CN)4]2-中,NH3分子的空间构型为_______。与CN-互为等电子体的一种分子的化学式为________ 。
(4)三氟甲磺酸(CF3SO3H)是一种有机强酸,结构式如图1所示,通常以CS2、IF5、H2O2等为主要原料来制取。
①H2O2分子中O原子的杂化方式为_______。
②三氟甲磺酸能与碘苯反应生成三氟甲磺酸苯酯和碘化氢。1个三氟甲磺酸苯酯分子中含有σ键的数目为_______。
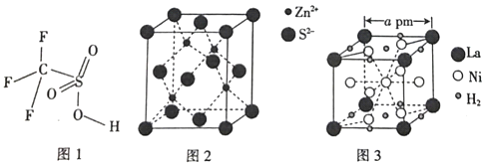
(5)硫化锌晶体的构型有多种,其中一种硫化锌的晶胞如图2所示,该晶胞中S2-的配位数为_________。
(6)镧镍合金是重要的储氢材料,其储氢后的晶胞如图3所示。
①储氢前该镧镍合金的化学式为_________。
②该镧镍合金储氢后氢的密度为_________(用NA表示阿伏加德罗常数的数值)g/cm3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关乙烯的叙述中,不正确的是( )
A.乙烯的化学性质比乙烷活泼
B.乙烯燃烧时火焰明亮,并产生黑烟
C.乙烯可用作香蕉等果实的催熟剂
D.乙烯双键中的一个键可以断裂,容易发生加成反应和取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表述方式错误的是( )
A.Fe的基态原子外围电子排布图: ![]()
B.氯化钠的分子式:NaCl
C.N的基态原子核外电子排布式:1S22S22p3
D.HC1O的结构式:H﹣O﹣Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】应对雾霾污染、改善空气质量需要从多方面入手,如开发利用清洁能源。甲醇是一种可再生的清洁能源,具有广阔的开发和应用前景。
(1)已知: ①CH3OH(g)+H2O(l)=CO2(g)+3H2(g) Δ H=+93.0 kJ·mol-1
②CH3OH(g)+1/2 O2(g)=CO2(g)+2H2(g) Δ H=-192.9 kJ·mol-1
③CH3OH(g)=CH3OH(l) Δ H=-38.19 kJ·mol-1
则表示 CH3OH 的燃烧热的热化学方程式为___________ 。
(2)在一定条件下用CO和H2合成 CH3OH:CO(g)+2H2(g)![]() CH3OH(g),在2 L恒容密闭容器中充入1mol CO和2mol H2,在催化剂作用下充分反应。下图表示平衡混合物中CH3OH的体积分数在不同压强下随温度的变化的平衡曲线。
CH3OH(g),在2 L恒容密闭容器中充入1mol CO和2mol H2,在催化剂作用下充分反应。下图表示平衡混合物中CH3OH的体积分数在不同压强下随温度的变化的平衡曲线。
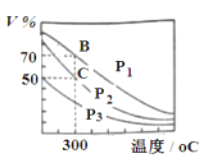
回答下列问题:
①该反应的反应热 Δ H________ 0(填“>” 或“<” ),压强的相对大小与p1_______ p2(填“>” 或“<” )。
②压强为 p2,温度为 300℃时,该反应的化学平衡常数的计算式为K=_______(只列算式不计算结果)。
③下列各项中,不能说明该反应已经达到平衡的是_______。
A.容器内气体压强不再变化
B.υ (CO):υ (H2)=1:2
C.容器内的密度不再变化
D.容器内混合气体的平均相对分子质量不再变化
E.容器内各组分的质量分数不再变化
④某温度下,在保证 H2 浓度不变的情况下,增大容器的体积, 平衡_______。
A.向正反应方向移动 B.向逆反应方向移动 C.不移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com