
| A、所得溶液中由水离出的C(OH-)=1.0×10-13mol?L-1 |
| B、所加烧碱溶液的pH=13 |
| C、所得溶液中C(Mg2+)=5.6×10-10mol?L-1 |
| D、在整个反应过程中,H2O的电离度在逐渐减小 |
| Ksp |
| c2(OH) |


科目:高中化学 来源: 题型:
| A、氢氧化钡溶液与盐酸的反应 2OH-+2H+=2H2O |
| B、钠和冷水反应 Na+2H2O=Na++2OH-+H2↑ |
| C、铜片插入硝酸银溶液中 Cu+Ag+=Cu2++Ag |
| D、碳酸钙溶于稀盐酸中 CaCO3+2H+=Ca2++H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等体积混合浓度均为0.2mol/L的AgNO3溶液和CH3COONa溶液不一定产生CH3COOAg沉淀 |
| B、将0.001mol/L的AgNO3溶液滴入0.001mol/L的KCl和0.001mol/L的K2CrO4溶液中先产生Ag2CrO4沉淀 |
| C、在Mg2+为0.12mol/L的溶液中要产生Mg(OH)2沉淀,溶液的pH至少要控制在9以上 |
| D、向饱和AgCl水溶液中加入NaCl溶液,KSPAgCl变大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
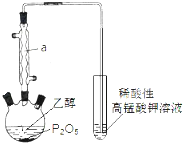 已知用P2O5作催化剂,加热乙醇可制备乙烯,反应温度为80℃~210℃.某研究性小组设计了如下的装置制备并检验产生的乙烯气体(夹持和加热仪器略去).
已知用P2O5作催化剂,加热乙醇可制备乙烯,反应温度为80℃~210℃.某研究性小组设计了如下的装置制备并检验产生的乙烯气体(夹持和加热仪器略去).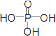 )
)查看答案和解析>>
科目:高中化学 来源: 题型:
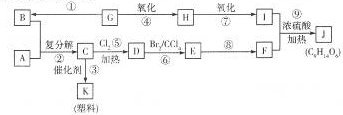
 CH2=CH2+R1CH=CHR2
CH2=CH2+R1CH=CHR2查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 某学生为了使过滤操作能自动添加液体,设计了“自动加液过滤器”,如图所示.在倒置的烧瓶中盛放待过滤的液体,液体从“液体流出管”流入漏斗.为使液体顺利流下,还需插入“空气导入管”与大气相通.
某学生为了使过滤操作能自动添加液体,设计了“自动加液过滤器”,如图所示.在倒置的烧瓶中盛放待过滤的液体,液体从“液体流出管”流入漏斗.为使液体顺利流下,还需插入“空气导入管”与大气相通.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com