
实验室也可用KMnO4固体和浓盐酸反应制氯气,反应方程式如下:2KMnO4+16HCl(浓)===2KCl+2MnCl2+8H2O+5Cl2↑。回答下列问题:
(1)该反应中氧化剂是__________,还原产物是____________。
(2)若参加反应的高锰酸钾为7.9 g,被氧化的HCl的物质的量是多少?把生成的氯气全部通入足量氢氧化钠溶液中,生成次氯酸钠多少克?
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
向一定量的Cu、Fe2O3的混合物中加入100 mL 1 mol·L-1的盐酸,恰好使混合物完全溶解,所得溶液中不含Fe3+,若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量为( )
A.3.2 g B.2.4 g C.1.6 g D.0.8 g
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是某学校实验室买回的硫酸试剂标签的部分内容。判断下列说法正确的是( )
| 硫酸化学纯(CP)(500 mL) 品名:硫酸 化学式:H2SO4 相对分子质量:98 密度:1.84 g·cm-3 质量分数:98% |
A.该硫酸的浓度为9.2 mol·L-1
B.配制200 mL 4.6 mol·L-1的稀H2SO4需该H2SO450 mL
C.该硫酸与等体积水混合质量分数变为49%
D.取该硫酸100 mL,则浓度变为原来的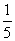
查看答案和解析>>
科目:高中化学 来源: 题型:
海水中含有的氯化镁是镁的重要来源之一。从海水中提取镁,可按如下步骤进行:①把贝壳制成石灰乳 ②在引入的海水中加入石灰乳,沉降、过滤,洗涤沉淀物 ③将沉淀物与盐酸反应,结晶过滤,干燥产物 ④将得到的产物熔融后电解。关于提取镁,下列说法不正确的是( )
A.此法的优点之一是原料来源丰富
B.进行①②③步骤的目的是从海水中提取MgCl2
C.以上提取镁的过程中涉及的反应都是非氧化还原反应
D.以上提取镁的过程中涉及的反应有分解反应、化合反应和复分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
分别用一种试剂除去下列各物质中的杂质(括号内为杂质),并写出离子方程式。
(1)BaCl2溶液(HCl)
试剂:________;离子方程式:__________________________ ______________________________________________。
(2)CO2(HCl)
试剂:________;离子方程式:__________________________ ______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
有些科学家提出硅是“21世纪的能源”,这主要是由于作为半导体材料的硅在太阳能发电过程中具有重要的作用。下列有关硅的说法中,不正确的是
A. 高纯度的硅广泛用于制作计算机
B. 硅可由二氧化硅还原制得
C. 低温时,硅与水、空气和酸不反应,但能与氢氟酸反应
D. 自然界中硅的储量丰富,自然界中存在大量的单质硅
查看答案和解析>>
科目:高中化学 来源: 题型:
下列表示对应化学反应的离子方程式正确的是
A. 电解饱和NaCl溶液:2Cl-+2H+ H2↑+Cl2↑
B.向Na2SO3溶液中滴加足量NaClO溶液:SO+ ClO-= SO+ Cl-
C.向FeBr2溶液中通入足量Cl2:2Fe2++Cl2=2Fe3++2Cl-
D.向Ca(OH)2溶液中加少量NaHCO3溶液:
2 HCO+Ca2++2OH-=CaCO3↓+ CO+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
用CH4催化还原NOx可以消除氮氧化物的污染。已知CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1,CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g) ΔH=-1 160 kJ·mol-1。若在标准状况下4.48 L CH4恰好能将一定量NO2还原成N2和H2O(g),则整个过程中放出的热量为( )
A.114.8 kJ B.232 kJ
C.368.8 kJ D.173.4 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
①CaCO3(s)===CaO+CO2(g) ΔH=177.7 kJ
②C(s)+H2O(s)===CO(g)+H2(g)
ΔH=-131.3 kJ/mol
③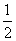 H2SO4(l)+NaOH(l)===
H2SO4(l)+NaOH(l)===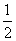 Na2SO4(l)+H2O(l)
Na2SO4(l)+H2O(l)
ΔH=-57.3 kJ/mol
④C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ/mol
⑤CO(g)+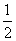 O2(g)===CO2(g) ΔH=-283 kJ/mol
O2(g)===CO2(g) ΔH=-283 kJ/mol
⑥HNO3(aq)+NaOH(aq)===NaNO3(aq)+H2O(l)
ΔH=-57.3 kJ/mol
⑦2H2(g)+O2(g)===2H2O(l) ΔH=-517.6 kJ/mol
(1)上述热化学方程式中,不正确的有________,不正确的理由分别是_______________________________________________________________。
(2)根据上述信息,写出C转化为CO的热化学方程式_____________。
(3)上述反应中,表示燃烧热的热化学方程式有________________;表示中和热的热化学方程式有________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com