
分析 生成0.5molD,v(D)=$\frac{\frac{0.5mol}{1s}}{5s}$=0.1mol/(L•s),又知C的平均反应速率是0.1mol/(L•s),由速率之比等于化学计量数之比可知,p=2,则
3A(g)+B(g)?2 C(g)+2D(g)
开始 2.5 1.25 0 0
转化 0.75 0.25 0.5 0.5
平衡 1.75 1 0.5 0.5
结合v=$\frac{△c}{△t}$、转化率=$\frac{转化的量}{开始的量}$×100%及物质的量比等于压强比计算.
解答 解:生成0.5molD,v(D)=$\frac{\frac{0.5mol}{1s}}{5s}$=0.1mol/(L•s),又知C的平均反应速率是0.1mol/(L•s),由速率之比等于化学计量数之比可知,p=2,则
3A(g)+B(g)?2 C(g)+2D(g)
开始 2.5 1.25 0 0
转化 0.75 0.25 0.5 0.5
平衡 1.75 1 0.5 0.5
①A的转化率为$\frac{0.75mol}{2.5mol}$×100%=30%,答:A的转化率为30%;
②A的平均反应速率为$\frac{\frac{0.75mol}{1s}}{5s}$=0.15mol/(L.s),答:A的平均反应速率为0.15mol/(L.s);
③由上述分析可知p=2,故答案为:p为2;
④反应前后的物质的量相同,则达到平衡时的压强和开始时压强的1倍,故答案为:达到平衡时的压强和开始时压强的1倍.
点评 本题考查化学平衡的计算,为高频考点,把握化学平衡三段法、转化率和速率的计算为解答的关键,侧重分析与计算能力的考查,注意利用速率与化学计量数的关系确定p,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 给盛有液体的烧瓶加热时,需要加碎瓷片或沸石 | |
| B. | NaCl溶液蒸发结晶时,蒸发皿中有晶体析出并剩余少量液体即停止加热 | |
| C. | 不慎将少量浓硫酸溅到皮肤上,应立即用水冲洗,然后涂抹10%的NaOH溶液 | |
| D. | 中和滴定实验时,不必润洗锥形瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3OH | B. | C2H5OH | C. | HO-CH2CH2-OH | D. | CH3CH2CH2OH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | ①②都属于加成反应 | |
| B. | 在通常条件下,①②都能自发进行 | |
| C. | ①吸热、②放热的事实说明苯环中含有的并不是碳碳双键 | |
| D. | ①②中的所有有机物均可使溴水层褪色,但褪色原理不完全相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 普通盐酸的酸性太强 | |
| B. | 普通盐酸具有挥发性 | |
| C. | 普通盐酸和月球岩石中的碳化物无法反应 | |
| D. | 无法区别岩石中原来含有的是碳化物,还是碳氢化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X的正反应速率是Y的逆反应速率的$\frac{m}{n}$倍 | |
| B. | 通入稀有气体使压强增大,平衡将正向移动 | |
| C. | 降低温度,混合气体的平均相对分子质量变小 | |
| D. | 若平衡时X、Y的转化率相等,说明反应开始时X、Y的物质的量之比为n:m |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫的还原性 | B. | 硫的漂白性 | ||
| C. | 二氧化硫的还原性 | D. | 二氧化硫的漂白性 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
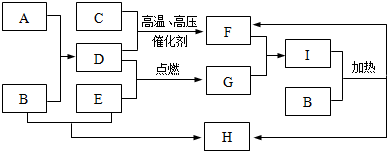
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com