
| 成分 | CaO | SiO2 | Al2O3 | Fe2O3 | MgO | CaS | 其它不溶于酸的物质 |
| 质量分数(%) | 65~66 | 3.5~5.0 | 1.5~3.5 | 0.2~0.8 | 0.2~1.1 | 1.0~1.8 | 23~26 |
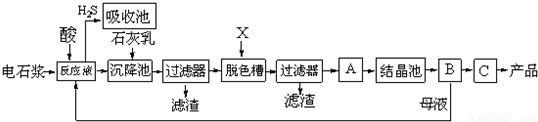


科目:高中化学 来源: 题型:阅读理解
 (2011?宁波模拟)“化学与技术”模块
(2011?宁波模拟)“化学与技术”模块
| ||
| ||
查看答案和解析>>
科目:高中化学 来源:云南省昆明八中2012届高三上学期期中考试化学试题 题型:022
[化学选修2——化学与技术模块]
水处理技术在生产、生活中应用广泛.
(1)含有较多________离子的水称为硬水.硬水加热后产生碳酸盐沉淀的离子方程式为________(写出一个即可)
(2)将RH型阳离子交换树脂和ROH型阴离子交换树脂串接来软化天然硬水,应先使硬水通过________(填“RH”或“ROH”)型离子交换树脂,原因是________.
(3)通过施加一定压力使水分子通过半透膜而将大分子或离子截留,从而获得纯净水的方法称为________.电渗析法净化水时,使离子通过半透膜的推动力是________.
(4)检验蒸馏水的纯度时,最简单易行的方法是测定水的________.水处理技术在生产、生活中应用广泛.
查看答案和解析>>
科目:高中化学 来源: 题型:
《化学与技术》模块(选考题)
28.目前下列工艺过程没有直接使用离子交换技术的是
A.硬水的软化 B. 电解饱和食盐水制造NaOH
C.电渗析淡化海水 D.海水中提取金属Mg
查看答案和解析>>
科目:高中化学 来源:宁波模拟 题型:问答题

查看答案和解析>>
科目:高中化学 来源:2011年浙江省宁波市高考化学模拟试卷(解析版) 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com